Для цитирования:
Диаб Х.М., Дайхес Н.А., Бакаев А.А., Пащинина О.А., Михалевич А.Е. Хирургическое лечение интратемпоральных поражений лицевого нерва. Голова и шея. Российский журнал=Head and neck. Russian Journal. 2020;8(4):52–59
Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
For citation:
Diab Kh.M., Daikhes N.A., Bakaev A.A., Paschinina O.A., Mikhalevich A.E. Surgical treatment of intratemporal lesions of the facial nerve. Head and neck. Russian Journal. 2020;8(4):52–59 (In Russian). The authors are responsible for the originality of the data presented and the possibility of publishing illustrative material – tables, figures, photographs of patients.
В статье проведен краткий анализ данных литературы по интратемпоральным поражениям лицевого нерва (ЛН) различной этиологии. Описаны методики хирургического лечения пациентов с интратемпоральными поражениями ЛН, а именно: нейрорафия нерва конец в конец, а также использование вставки аутографта икроножного нерва. Представлены предварительные результаты реабилитации пациентов с данной патологией.
Цель работы: повышение эффективности лечения пациентов с интратемпоральными поражениями ЛН.
Материал и методы. На базе ФГБУ НМИЦО ФМБА России в оториноларингологическом отделении (патологии уха и основания черепа) за период с 2014 по 2020 г. обследованы и пролечены 115 пациентов с периферическим парезом мимической мускулатуры (ММ), вызванным интратемпоральным поражением ЛН. Все пациенты были обследованы с помощью общепринятых оториноларингологических методов, также включающих аудиологическое обследование с целью уточнения состояния слуховой функции, для диагностики состояния ЛН и ММ проводили электромиографию, электронейромиографию. Применяли лучевые методы исследования, включающие МСКТ височных костей и МРТ головы в режимах Т1, Т2, DWI, Т1 с контрастным усилением. В зависимости от места и протяженности поражения ЛН пациентам выполнялось хирургическое лечение в объеме декомпрессии ЛН, пластики конец в конец либо с использованием аутографта икроножного нерва.
Результаты и их обсуждение. Декомпрессия ЛН выполнена 60 (52,2%) пациентам, нейрорафия нерва конец в конец – 37 (32,2%) пациентам, реконструкция аутографтом икроножного нерва – 18 (15,6%) пациентам. За период наблюдения в течение 12 месяцев и более ни у одного из пациентов не было выявлено ни одного осложнения, связанного с проведением хирургического лечения. Полученные результаты в разных группах отличались и напрямую зависели от степени поражения нерва и от длительности заболевания. Неудовлетворительные результаты были связаны, в основном, с длительностью паралича ММ в анамнезе заболевания более 2–3 лет.
Заключение. Эффективность хирургического лечения интратемпоральных поражений ЛН связана со своевременным выявлением патологического процесса, основанном на лучевых методах исследования, а также с распространенностью поражения нерва и длительностью паралича. Определение правильной тактики хирургического лечения позволяет получать хорошие и удовлетворительные результаты в послеоперационном периоде. Функциональные результаты напрямую зависят от давности пареза ММ (тяжелая мышечная атрофия и частичная деградация концевых сегментов двигательных нейронов происходит уже через 2 года).
Ключевые слова: лицевой нерв, декомпрессия лицевого нерва, нейрорафия лицевого нерва конец в конец, аутографт икроножного нерва
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов. Финансирование. Работа выполнена без спонсорской поддержки
The article provides a brief literature data analysis on intratemporal facial nerve lesions of different etiology. The article describes the improved methods of surgical treatment of patients with intratemporal facial nerve lesions, such as end-to-end neurorrhaphy, as well as using the sural nerve autograft. The preliminary results of the rehabilitation of patients with this pathology are presented. According to world literature, facial nerve lesions (injuries, tumors, inflammations) rank second in the peripheral nervous system pathology frequency and rank first in the cranial neuropathy (number of cases varies from 8 to 240 patients per 100,000 population), equally among men and women.
According to authors’ monitoring results, the main causes of facial nerve dysfunction are: fractures of the petrous part of temporal bone (road traffic accident, home accident, criminal act), iatrogenic injuries (as a result of previous sanitizing operations), tumor lesions of the nerve and of the adjacent anatomical structures, destructive processes in the temporal bones (cholesteatoma, cholesterol granuloma, etc.). In treating facial nerve dysfunction, both conservative and surgical methods should be considered.
All patients, without exception, underwent examination according to generally accepted otorhinolaryngological methods, which also included an audiological examination in order to clarify the state of the auditory function; to diagnose the condition of the facial nerve and facial muscles, electromyography and electroneuromyography were performed among objective research methods. Mandatory in the diagnosis of the causes of damage to the facial nerve is to carry out radiological research methods, including MSCT of the temporal bones and MRI of the head in the modes T1, T2, DWI, T1 with contrast enhancement.
Surgical treatment in the amount of decompression at the present stage of otosurgery does not cause difficulties, it is relatively easy to perform, provided that the otosurgeon has the appropriate skills and good knowledge of the microanatomy of the temporal bone. But the issue of performing FN plasty, especially with its extended lesions of 5–7 (for example, from labyrinth to mastoid segments) mm or more in the temporal bone, has not yet been properly covered in the available domestic literature.
Objective: to improve the treatment effectiveness in patients with intratemporal facial nerve lesions.
Material and methods. During the period from 2014 to 2020, 115 patients with peripheral MM paresis caused by intratemporal lesion of the FN were examined and treated in the FSBI NMRCO FMBA of Russia (Ear Diseases Department), which included: benign tumors of the temporal bone – 64 (55.7%) patients, of which 23 (36%) patients with temporal bone paraganglioma and 41 (64%) with schwannoma of the facial nerve; chronic suppurative otitis media (CHS) complicated by cholesteatoma – 32 (27.8%) patients; traumatic injuries of FN due to fracture of the temporal bones – 8 (6.9%) patients; iatrogenic injuries of the FN during sanitizing operations on the ear – 11 (9.6%) patients, of which 4 (36.4%) cases had a tympanic segment trauma and 7 (63.6%) cases – mastoidal segments trauma. Depending on the location and extent of the FN lesion, patients underwent surgical treatment in the amount of FN decompression, end-to-end plasty, or using an autograft of the sural nerve. FN decompression was performed in 60 (52.2%) patients, end-to-end neurorraphy of the nerve was performed in 37 (32.2%) patients, reconstruction of the sural nerve autograft was performed in 18 (15.6%) patients.
Results and discussions. During the follow-up period of 12 months or more, no patient had a single complication associated with surgical treatment. The results obtained in different groups differed and directly depended on the degree of nerve damage and on the duration of the disease. When performing FN decompression, an improvement in nerve function was noted as early as a month after surgery. In 43 (71.7) patients, FN function recovered completely, in 8 (13.3%) patients, FN function improved to grade II in HB, in 6 (10%) patients, FN function improved to grade II in HB, and only in 3 (5%) patients had no result from the operation. With endto-end nerve plasty, improvement in function was noted after 6 to 9 months. In 12 (32.4%) patients, FN function improved to grade III in HB, in 16 (43.3%) to IV in HB, in 7 (18.9%) to grade V, in 2 (5.4% ) patients had no effect from the operation for 15 months or more. When using the insertion of the sural nerve graft during FN plasty, improvement in function was observed after 9–15 months. Good results (improvement of function to grade III) were observed in 6 (33.3%) patients, satisfactory results (improvement in function to grade IV–V) – in 5 (27.8%) patients, unsatisfactory (no result) – in 7 (38.9%). Unsatisfactory results were mainly associated with the duration of MM paralysis in the history of the disease for more than 2–3 years.
Conclusion. The success of surgical treatment of intratemporal facial nerve lesions depends on an early pathological process detection based on X-ray methods of diagnostics, as well as the nerve lesion extension and the paralysis duration. Determining the correct tactics of surgical treatment allows to get the satisfactory results in the post-surgical period. Functional results directly depend on the mimic muscles paresis duration (severe muscle atrophy and partial deterioration of the terminal segments of the motor neurons appear after 2 years).
Key words: facial nerve, decompression of the facial nerve, end-to-end facial nerve neurorraphy, sural nerve graft
Conflicts of interest. The authors have no conflicts of interest to declare.
Введение
Нарушение функции лицевого нерва (ЛН) не только влияет на черты лица, но и приводит к серьезным нарушениям адаптации пациента в социальном, психологическом и экономическом аспектах его жизни.
По данным мировой литературы, поражения (травмы, опухоли, воспаления) ЛН занимают второе место по частоте среди патологии периферической нервной системы и первое место среди поражений черепных нервов (заболеваемость варьируется от 8 до 240 больных на 100 тыс. населения в разных странах), в равной степени среди мужчин и женщин [1]. Основными причинами, вызывающими нарушение функции ЛН, являются переломы пирамиды височной кости (дорожно-транспортные просшествия, бытовые или криминальные травмы); ятрогенные повреждения ЛН (в результате предшествующих санирующих операций); опухолевые поражения либо самого нерва, либо смежных анатомических структур; деструктивные процессы в височной кости (холестеатома, холестериновая гранулема и т.д.) [2].
Несмотря на то что нет единого «золотого» стандарта или универсальной общепринятой системы оценки функции ЛН, Комитет Американской Академии оториноларингологии хирургии головы и шеи по изучению поражений ЛН в 1985 г. принял модифицированную классификацию House-Brackmann Grading System (шкала HB) в качестве стандартного метода оценки функции ЛН, которая различает 6 степеней нарушения его функции (I–VI степени), где I степень – норма, VI степень – полное отсутствие движений мимической мускулатуры (ММ) [3]. Этой классификации придерживаются и большинство отечественных специалистов, занимающихся хирургией уха.
В диагностике поражений ЛН электродиагностические тесты оценивают состояние нерва и определяет степень его дисфункции. Электронейромиография (ЭНМГ) и электромиография (ЭМГ) являются наиболее точными и объективными методами при оценке поражения ЛН [4].
ЭНМГ оценивает сохранность функции нервных волокон, подвергнутых тому или иному поражению вследствие травмирующего или воспалительного фактора, либо в более редких случаях перерождению их вследствие роста доброкачественных новообразований височной кости. Предпочтительнее проводить исследование между 4-ми и 21-ми сутками от начала полного паралича, т.к. валеровская дегенерация развивается в течение трех суток, и поэтому нецелесообразно проводить ЭНМГ ранее четвертых суток [5]. ЭНМГ не используется после 3-й недели паралича, т.к. может наблюдаться ложноотрицательный феномен, когда в ответ на стимул асинхронно стимулируются восстанавливаемые или регенерируемые волокна. Вследствие дефекта синхронизации не регенерируется составной мышечный потенциал действия, несмотря на наличие восстановления в волокнах [6].
ЭМГ выявляет потенциалы действия во время мышечного сокращения с функционирующего нерва. Мышца, которая была денервирована, отображает фибрилляции, в то время как мышца, которая находится в процессе реинервации, демонстрирует полифазный потенциал. Отсутствие потенциалов, связанных с давним параличом ЛН (по разным данным более 2 лет после повреждения), указывает на тяжелую мышечную атрофию и деградацию концевых сегментов двигательных нейронов. ЭМГ проводится в случаях длительного (более трех недель) паралича ЛН или в случаях обнаружения при ЭНМГ 90% и более перерождения нервных волокон [7].
Обязательным в диагностике причин поражения ЛН является проведение лучевых методов исследования. Результаты спиральной компьютерной томографии (СКТ) височных костей дают подробную картину костной анатомии канала ЛН, его деструктивных изменений, а также изменений кости вокруг коленчатого узла или расширение его лабиринтного сегмента. При проведении мультиспиральной компьютерной томографии (МСКТ) височных костей в случае поражения ЛН шванномой или параганглиомой можно увидеть увеличение коленчатого узла, также может быть выявлено увеличение лабиринтного или барабанного сегментов. Как правило, на срезах томограмм это может выглядеть как эрозия костей с нерегулярными границами [8].
Магнитно-резонансная томография (МРТ) головы в режимах Т1, Т2, DWI, Т1 с контрастным усилением обеспечивает получение высококачественного изображения структур не только головного мозга, но и опухолевых образований височной кости и внутреннего слухового прохода, в т.ч. помогает провести дифференциальную диагностику между холестеатомным и неопластическим процессами [9].
После выполнения необходимых уточняющих исследований проводится топическая диагностика патологического процесса в височной кости и уровень поражения ЛН, что в свою очередь определяет дальнейшую тактику ведения пациента, предоперационную подготовку, выбор доступа к патологическому процессу, ход и объем хирургического вмешательства.
При лечении нарушений функции ЛН в зависимости от вида и степени поражения в мировой литературе рассматриваются как консервативные, так и хирургические методы, которые направлены либо на купирование и/или уменьшение воспалительных явлений в самом нерве и тканях вокруг, либо на восстановление нервной проводимости по ЛН, утраченной в результате его компрессии, полного пересечения, разрушения ствола ЛН на протяжении [10–12].
Предпосылкой эффективной реабилитации пациентов с поражениями ЛН является возможность в максимально кратчайшие сроки провести хирургическое лечение, направленное на восстановление целостности ствола нерва, что выполнимо при условии отсутствия гнойных осложнений в ране. Авторы, которые предпочитают хирургическое лечение, едины во мнении, что принципиальным сроком проведения хирургического лечения больных, после которого можно рассчитывать на максимальное восстановление функции нерва, являются первые 2 месяца после пареза мимических мышц (ММ), при этом используются различные доступы в зависимости от локализации и протяженности поражения [13–15].
В зависимости от сроков вмешательства различают первичный, первично отсроченный и поздний (вторичный) шов нерва, что более актуально при его травматических повреждениях. Более раннее восстановление нерва дает лучший результат восстановления ММ лица. Первично отсроченный шов накладывают спустя 1–2 месяца после первичной хирургической обработки или операции, когда достигнута полная санация раны или устранены препятствия к наложению шва нерва. Поздний (вторичный) шов накладывают спустя 5–6 месяцев после выявленного повреждения или позже. Хотя полного восстановления функции ММ при позднем наложении шва ожидать сложно, оно все равно показано, т.к. это улучшает трофику тканей и, следовательно, общее состояние пациента. При отсроченной операции легче определить размеры необходимой резекции нерва, и шов его более прочен, т.к. спустя 3 недели и более после травмы происходит утолщение эпиневрия, при этом сшитый нерв окружается неизмененными тканями, т.е. при этом меньше риск образования вокруг него рубцов.
Основными этапами восстановления ЛН являются: освобождение проксимального и дистального концов нерва в зоне повреждения, невролиз (освобождение от рубцов), осмотр и определение границ резекции нерва, резекция поврежденных участков нервного ствола в пределах неизмененных тканей (неврома в проксимальном конце, глиома в дистальном конце) острым способом, чтобы линия среза была предельно ровной, нейрорафия, дополнительная изоляция ствола нерва в зоне шва аутотканями.
Техника шва нерва широко представлена в отечественной и зарубежной литературе. Не останавливаясь на подробностях, следует отметить, что в случае сшивания нерва в барабанной полости (вследствие работы в ограниченном костными стенками пространстве отделов среднего уха) целесообразно прибегать к технике периневрального шва, который имеет преимущество по сравнению с эпиневральным, что создает более оптимальные условия для регенерации нервных волокон. Идеальным же считается их сочетание, т.е. наложение эпи-периневрального шва. Следует отметить, что это возможно при небольших поперечных повреждениях ЛН с диастазом концов не более 1–2 мм. Наилучшие результаты достигаются при отсутствии натяжения ЛН в области шва, т.к. это не приводит к нарушению перфузии крови в зону поражения и не нарушает нейронную регенерацию. Зачастую при обнаружении обширных дефектов ЛН (более 8–10 мм) даже после проведения полной деканализации (декомпрессии) нерва на всем протяжении тимпаномастоидального сегмента не всегда удается сопоставить конец в конец дистальный и проксимальный отрезки нерва. В данной ситуации перед отохирургом стоит задача восстановления нервной проводимости посредством пластики нерва аутографтом большого ушного или икроножного нервов. При поражении ЛН на уровне шилососцевидного отверстия возможно проведение контралатеральной (ветвями ЛН другой стороны) или ипсилатеральной реинервации ветвями подъязычного, жевательного, добавочного нервов, имеющих двигательные волокна, но это уже является объектом исследования нейро- или челюстно-лицевой хирургии. С точки зрения отонейрохирургии (относительно молодое новое направление оториноларингологии), занимающейся патологией височной кости, внутреннего слухового прохода, области мостомозжечкового угла и латерального основания черепа, поражения ЛН от уровня внутреннего слухового прохода до уровня выхода из шилососцевидного отверстия представляют собой достаточно сложную проблему, решение которой порой требует нестандартного подхода.
Проведение декомпрессии ЛН на современном этапе отохирургии не вызывает сейчас трудностей, она относительно легко выполнима при условии наличия у отохирурга соответствующих навыков и хорошего знания микроанатомии височной кости. А вот вопрос с проведением пластики ЛН, особенно при протяжен- ных его поражениях 5–7 мм и более (например, от лабиринтного до мастоидального сегментов) в височной кости в доступной отечественной литературе до сих пор как следует не освещен.
Цель работы: повышение эффективности хирургического лечения пациентов с интратемпоральными поражениями ЛН.
Материал и методы
На базе ФГБУ НМИЦО ФМБА России в оториноларингологическом отделении (патологии уха и основания черепа) за период с 2014 по 2020 г. обследованы и пролечены 115 пациентов с периферическим парезом ММ, вызванным интратемпоральными поражениями ЛН, которые включали: доброкачественные опухоли височной кости – 64 (55,7%) пациента, из них 23 (36%) пациента с параганглиомой височной кости и 41 (64%) с шванномой ЛН (ШЛН); хронический гнойный средний отит (ХГСО), осложненный холестеатомой – 32 (27,8%) пациента; травматические повреждения ЛН вследствие перелома височных костей – 8 (6,9%) пациентов; ятрогенные повреждения ЛН при проведении санирующих операций на ухе – 11 (9,6%) пациентов, из них в 4 (36,4%) случаях имела место травма тимпанального сегмента и в 7 (63,6%) случаях травма мастоидального сегмента.
Всем без исключения пациентам проводилось обследование по общепринятым оториноларингологическим методам, включающим аудиологическое обследование с целью уточнения состояния слуховой функции, а также лучевые методы исследования: МСКТ височных костей и МРТ головы в режимах Т1, Т2, DWI, Т1 с контрастным усилением (гадолиний). На основании полученных данных проводилась топическая диагностика уровня поражения ЛН: меатальный, супрагеникулярный, инфрагеникулярный, инфрастапедиальный, инфрахордальный и инфрафораменальный сегменты. Такое разделение ЛН принято в нейрохирургической практике. В отохирургической же практике для удобства принято разделение нерва на меатальный, лабиринтный, тимпанальный, мастоидальный и экстратемпоральный сегменты.
После определения этиологии и уровня поражения ЛН всем обследованным пациентам проводилось хирургическое лечение, направленное на санацию патологического очага или удаление доброкачественного новообразования височной кости с одномоментным хирургическим этапом с целью улучшения/ восстановления сниженной или утраченной функции ЛН. В зависимости от места и протяженности поражения ЛН пациентам выполнялось хирургическое лечение в объеме декомпрессии ЛН, пластики конец в конец либо с использованием аутографта икроножного нерва.
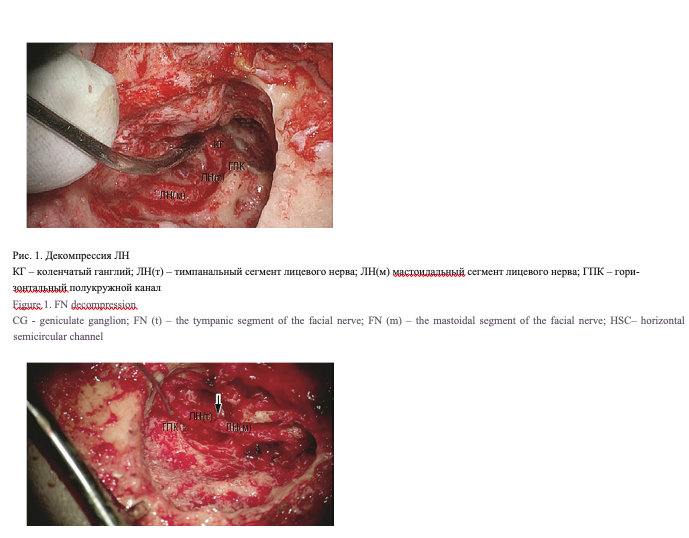
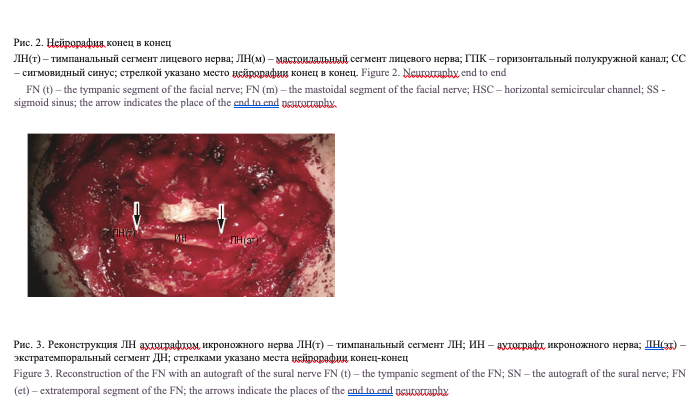
Декомпрессия ЛН (рис. 1) была выполнена 60 (52,2%) пациентам с поражением ЛН, из которых у 23 (38,3%) была параганглиома височной кости, у 25 (41,7%) – ХГСО с холестеатомой, у 12 (20%) – травма височной кости. Функция ММ до операции варьировалась от III до V степени по шкале HB. В ходе операции при извлечении ЛН из канала не обнаруживалось повреждения ствола последнего. Во всех случаях при опухолевых поражениях (шваннома, параганглиома) удавалось удалить опухоль единым блоком, отделив ее от ствола нерва. При поражении ЛН на фоне ХГСО не было выявлено данных о сдавлении ствола нерва матриксом холестеатомы, но при этом были обнаружены дигисценции ЛН в тимпанальном отделе, ствол нерва в данной зоне был отечным, что свидетельствовало о длительном воспалении вследствие эрозивного процесса. При травмах височной кости чаще всего обнаруживалась линия перелома, проходящая через канал ЛН в области второго колена, при этом полного пересечения нерва не отмечалось, а имело место сдавление нерва костными отломками, которые удалялись по ходу операции. Нейрорафия нерва «конец в конец» (рис. 2) была выполнена 37 (32,2%) пациентам, из которых у 26 (70,3 %) была ШЛН, у 4 (10,8%) – ХГСО с холестеатомой пирамиды височной кости, у 7 (18,9%) – травма височной кости. Функция ММ до операции варьировалась от IV до VI степени по шкале HB. В ходе операции при выполнении деканализации нерва обнаруживалось поражение его целостности, в связи с чем патологический процесс, вызывающий нарушение функции последнего, устранялся при удалении пораженного сегмента нерва. Протяженность дефекта нерва варьировалась от 3 мм до 12 мм. При этом у 14 (39,5%) пациентов с опухолями протяженность дефекта ЛН составляла более 5 мм, но не более 12. У остальных 23 (60,5%) пациентов протяженность поражения ЛН была 5 мм и менее. В данной группе хирургическое лечение было направлено на восстановление целостности ствола ЛН путем сшивания нерва конец в конец эпи-периневральным швом.
Стоит отметить, что сшивание нерва при длине его поражения 5 мм и менее не представляет трудностей и данные методики представлены в отечественной и зарубежной литературе. В таких случаях удавалось сопоставить концы нерва без натяжения, выполнив деканализацию последнего. По-другому обстояли дела при величине поражения нерва более 6 мм. В данной ситуации произвести сшивание концов без натяжения нерва, даже выполнив полную декомпрессию (деканализацию), не представлялось возможным, а в мировой литературе нет четких рекомендаций, как поступать в данной ситуации. Поэтому решение этого вопроса требовало нестандартного подхода. Данным пациентам проводили полную деканализацию ЛН, что по нашим наблюдениям (измерениям), могло обеспечить сближение концов сшиваемого нерва примерно на 5 мм, что обычно и выполнялось на первом этапе. Если данный этап операции не давал желаемого эффекта (сопоставления концов нерва без натяжения), то удаляли верхушку сосцевидного отростка, вскрывали шилососцевидный канал и выделяли ЛН до инфрафораменального (экстратемпорального) сегмента. Данный прием давал возможность сместить дистальный конец нерва еще на 2–3 мм. Далее проводилась мобилизация ствола ЛН ниже шилососцевидного отверстия до уровня отхождения шейной ветви, которую при необходимости пересекали. Утрата вследствие данной манипуляции функции движения подкожной мышцы шеи на стороне операции в ближайшем и отдаленном послеоперационных периодах не вызывала ухудшения качества жизни пациентов. Данный прием давал возможность сместить дистальный конец нерва в направлении барабанной полости еще на 2–3 мм. Далее при необходимости производилась деканализация ЛН на уровне лабиринтного сегмента, борами вдоль горизонтального полукружного канала высверливался желобок с удалением костной ткани в области нижней стенки наружного слухового прохода, что в конечном итоге давало возможность сблизить концы нерва еще на 2 мм. Суммарно, все вышеописанные приемы давали возможность сблизить сшиваемые концы нерва без натяжения на 11–12 мм. Нерв сшивали по общепринятым методикам эпи-периневральным швом с использованием шовного материала Prolen 8-0.
Реконструкция аутографтом икроножного нерва (рис. 3) была выполнена 18 (15,6%) пациентам, из которых с ШЛН – 15 (83,3%) пациента, ХГСО с холестеатомой пирамиды височной кости – 3 (16,7%) пациента. Функция ММ до операции была VI степени по шкале HB. В ходе операции при выполнении деканализации нерва обнаруживалось поражение его целостности, в связи с чем патологический процесс, вызывающий нарушение функции последнего устраняли при удалении пораженного сегмента нерва. Протяженность дефекта нерва была более 12 мм, что было связано с распространенностью опухолевого процесса, иногда с прорастанием через шилососцевидное отверстие на шею. В связи с невозможностью сшивания нерва конец в конец в данной ситуации проводилась пластика нерва с использованием аутографта икроножного нерва.
Результаты и их обсуждение
За период наблюдения в течение 12 месяцев и более ни у одного из пациентов в послеоперационном периоде не было выявлено ни одного осложнения, связанного с проведением непосредственно хирургического вмешательства. Полученные результаты напрямую зависели от степени поражения ЛН, применяемой методики и длительности заболевания, предшествующего операции.
После декомпрессии ЛН улучшение функции нерва было отмечено уже через месяц: у 43 (71,7) пациентов функция ЛН восстановилось полностью, у 8 (13,3%) – улучшилась до II степени по HB, у 6 (10%) – до II степени и лишь у 3 (5%) пациентов результат от операции отсутствовал.
При пластике нерва конец в конец улучшение функции отмечалось через 6–9 месяцев. У 12 (32,4%) пациентов функция ЛН улучшилась до III степени по HB, у 16 (43,3%) – до IV степени, у 7 (18,9%) – до V степени, у 2 (5,4%) пациентов не было эффекта от операции на протяжении 15 месяцев и более.
При использовании во время пластики ЛН вставки графта икроножного нерва улучшение функции наблюдалось через 9–15 месяцев. Хорошие результаты (улучшение функции до III степени) отмечались у 6 (33,3%) пациентов, удовлетворительные результаты (улучшение функции до IV–V степени) – у 5(27,8%) пациентов, неудовлетворительные (отсутствие результата) – у 7 (38,9%). Неудовлетворительные результаты были связаны в основном с длительностью паралича ММ в анамнезе заболевания более 2–3 лет.
Повторные операции проводились в основном пациентам с хроническим гнойным средним отитом (ХГСО), что было связано не с ухудшением функции ЛН, а с необходимостью проведения повторной ревизионной операции (повторная санация, репозиция оссикулярного протеза, слухоулучшающий этап) на основании результатов лучевых методов исследования и аудиологических данных. Из 32 (27,8%) пациентов с ХГСО повторно были оперированы 19 (59,4%) пациентов, из которых только у 9 (47,4%) был выявлен рецидив ограниченной холестеатомы в виде 1 или нескольких жемчужин (по ходу ЛН, инфралабиринтный клеточный тракт, супралабиринтные клетки, область внутреннего слухового прохода).
Из 41 (64%) пациента с опухолями ЛН ревизионные операции были проведены только 3 (7,3%) пациентам, что было связано, по нашему мнению, с радикальностью первой операции, это в дальнейшем подтверждалось данными лучевых методов исследования (СКТ, МРТ с контрастированием). Из них у одного пациента в последующем через 1 год после первой операции была выполнена резекция остаточной опухоли с пораженным сегментом ЛН и далее проведена его пластика аутографтом икроножного нерва (достигнуто улучшение функции нерва до IV степени через 15 месяцев). У второго пациента через 6 месяцев после первой операции была проведена ревизия ствола нерва после удаления опухоли, рецидива опухоли не было, по данным интраоперационного нейромониторинга, проведение электрического стимула по стволу нерва восстановлено, однако улучшения движения ММ не наблюдалось, что мы связываем с длительностью поражения более 3 лет, что привело к тяжелой мышечной атрофии и частичной деградации концевых сегментов двигательных нейронов. У третьего пациента проведена повторная операция по поводу возникшего рецидива опухоли (шваннома), при этом при повторной операции удалось удалить последнюю с сохранением ствола нерва и в последующем улучшить функцию нерва с V степени до III степени по шкале HB.
Заключение
Эффективность хирургического лечения интратемпоральных поражений ЛН напрямую зависит от своевременности выявления патологического процесса, а также от распространенности поражения ЛН и длительностью паралича ММ. Определение правильной тактики хирургического лечения позволяет получать хорошие и удовлетворительные результаты в послеоперационном периоде. Функциональные результаты напрямую зависят от давности пареза ММ (тяжелая мышечная атрофия и частичная деградация концевых сегментов двигательных нейронов происходит уже через 2 года).
ЛИТЕРАТУРА/REFERENCES
- Svistushkin V.M., Slavsky A.N. Facial nerve neuropathy: modern approaches to diagnosis and treatment. Breast cancer. Otorhinolaryngol. 2016;4:280–5. [Свистушкин В.М., Славский А.Н. Невропатия лицевого нерва: современные подходы к диагностике и лечению. РМЖ. Оториноларингология. 2016;4:280–5. (In Russ.)].
- Hato N., Nota J., Hakuba N., Gyo K., Yanagihara N. Facial nerve decompression surgery in patients with temporal bone trauma: analysis of 66 cases. Trauma. 2011;71(6):1789–93. doi: 10.1097/TA.0b013e318236b21f.
- House J.W., Brackmann D.E. Facial nerve grading system. Otolaryngol. Head and Neck Surg. 1985;93:146–7.
- Savitskaya N.G., Nikitin S.S., Ivanova-Smolenskaya I.A. Clinical and neurographic analysis of recurrent facial neuropathy. Modern approaches to the diagnosis and treatment of nervous and mental diseases: Materials of the jubilee. Petersburg: VMAA. 2000. Р. 448–9. [Савицкая Н.Г., Никитин С.С., Иванова-Смоленская И.А. Клинико-нейрографический анализ рецидивирующей невропатии лицевого нерва. Современные подходы к диагностике и лечению нервных и психических заболеваний: Материалы юбил. науч. конф. СПб., 2000. Р. 448–9. (In Russ.)].
- Komantsev V.N., Zabolotnykh V.A. Methodological foundations of clinical electroneuromyography: a guide for doctors. Petersburg, 2001. 350 p. [Команцев В.Н., Заболотных В.А. Методические основы клинической электронейромиографии: руководство для врачей. СПб., 2001. 350 с. (In Russ.)].
- Fish U. Maximal nerve excitability testing vs electroneuronography. Otolaryngol. 1980;106(6):352–7.
- Di Bella P., Logullo F., Lagalla G. Reproducibility of normal facial motor nerve conduction studies and their relevance in the electrophysiological assessment of peripheral facial paralysis. Clin. 1997;4:300–8.
- Mayer T.E., Brueckmann H., Siegert R., Witt A., Weerda H. High-resolution CT of the temporal bone in dysplasia of the auricle and external auditory canal. AJNR Am. J. Neuroradiol. 1997;18(1):53–65.
- Anderson R.E., Laskoff J.M. Ramsay Hunt syndrome mimicking intracanalicular acoustic neuroma on contrast-enhanced MR. J. Nucl. Radiol. 1990;11(2):409.
- Jahrsdoerfer R. A., Lambert P. R. Facial nerve injury in congenital aural atresia surger. J. Otolaryngol. 1988;19(3):283–7.
- Davidson H.C. Imaging of the temporal bone. Magn. Reson. Imaging Clin. N. Am. 2002;10(4):573–613. doi: 10.1016/s1064-9689(02)00019-3.
- Diab Kh.M., Nazhmudinov I.I., Karayan A.S., Kondratchikov D.S., Orlova E.V., Yusifov K.D.O. Surgical treatment of intratemporal facial nerve
- Doctor. 2018;29(3):49–54. doi: 10.29296/25877305-2018-03-12. [Диаб Х.М, Нажмудинов И.И, Караян А.С, Кондратчиков Д.С, Орлова Е.В., Юсифов К.Д.О. Хирургическое лечениеинтратемпоральных опухолей лицевого нерва. Врач. 2018;29(3):49–54. doi: 10.29296/25877305-2018-0312. (In Russ.].
- Kahinga A.A., Han J.H., Moon I.S. Total Transcanal Endoscopic Facial Nerve Decompression for Traumatic Facial Nerve Palsy. Yonsei Med. J. 2018;59(3):457–60. doi: 10.3349/ymj.2018593.
- Cannon R.B., Gurgel R.K., Warren F.M., Shelton C. Facial nerve outcomes after middle fossa decompression for Bell’s palsy. Neurotol. 2015;36(3):513–8. doi: 10.1097/MAO0000 000000000513.
- Guntinas-Lichius O., Silver C.E., Thielker J., Bernal-Sprekelsen M., Bradford C.R., De Bree R., Kowalski L.P., Olsen K.D., Quer M., Rinaldo A., Rodrigo J.R., Sanabria A., Shaha A.R., Takes R.P., Vander Poorten V., Zbären P., Ferlito A. Management of the facial nerve in parotid cancer: preservation or resection and reconstruction. Arch. Otorhinolaryngol. 2018;275(11):2615–26.
doi: 10.1007/s00405-018-5154-6.
- Kalina V.O., Schuster M. A Peripheral facial paralysis. : Medicine, 1970. 206 p. [Калина В.О., Шустер М.А. Периферические параличи лицевого нерва. М., 1970. 206 c. (In Russ.)].
- Aly A., Avila E., Cram A.E. Endoscopic plastic surgery. Surg. Clin. North. Am. 2000;80(5):1373–82. doi: 10.1016/s0039-6109(05)70234-6.
- Neuropathy: A Guide for Physicians. N.M. Zhuleva. SPb., 2005.416 p. [Невропатии: Руководство для врачей. Под ред. Н.М. Жулева. СПб., 2005. 416 с. (In Russ.)].
- Jiang X., Lim S.H., Mao H.Q., Chew S.Y. Current applications and future perspectives of artificial nerve conduits. Neurol. 2010;223(1):86–101. d oi: 10.1016/j.expneurol.2009.09.009.
- Kimata Y., Sakuraba M., Hishinuma S., Ebihara S., Hayashi R., Asakage T. Free vascularized nerve grafting for immediate facial nerve reconstruction. 2005;115(2):331–6. doi: 10.1097/01.mlg.000 0154753.32174.24.
Поступила 28.03.20
Принята в печать 06.07.20
Received 28.03.20
Accepted 06.07.20
Вклад авторов: Дайхес Н.А. – разработка дизайна исследования, научное редактирование текста статьи. Диаб Х.М. – разработка дизайна исследования, научное редактирование текста статьи, проведение операций. Бакаев А.А., Михалевич А.Е., Пащинина О.А. – обзор публикаций по теме статьи, получение данных для анализа, анализ полученных данных, написание текста статьи.
Authors’ contributions: N.A. Daikhes – research design development, scientific editing of the article text. Diab Kh.M. – development of research design, scientific editing of the text of the article, performing the operations. Bakaev A.A.,
Mikhalevich A.E., Pashchinina O.A. – review of publications on the topic of the article, obtaining data for analysis, analyzing the data obtained, writing the text of the article.
Информация об авторах:
Х.М.А. Диаб – д.м.н., заместитель директора по международной деятельности, главный научный сотрудник ФГБУ НМИЦО ФМБА, Москва;
e-mail: Hasandiab@mail.ru https://orcid.org/0000-0002-2790-7900
Н.А. Дайхес – д.м.н., профессор, член-корр. РАН, директор ФГБУ НМИЦО ФМБА России, Москва; e-mail: admin@otolar.ru https://orcid.org/0000-0003-2674-4553
А.А. Бакаев – соискатель ученой степени к.м.н., научно-клинического отдела заболеваний уха ФГБУ НМИЦО ФМБА России, Москва; e-mail: amirbakaev1990@gmail.com
О.А. Пащинина – к.м.н., руководитель и заведующая отделением научноклинического отдела заболеваний уха ФГБУ НМИЦО ФМБА России, Москва; e-mail: Olga83@mail.ru https://orcid.org/0000-0002-3608-2744
А.Е. Михалевич – к.м.н., младший научный сотрудник научно-клинического отдела заболеваний уха ФГБУ НМИЦО оториноларингологии ФМБА России, Москва; e-mail: MikhalevichAE@mail.ru
Information about the authors:
K.M. Diab – Doctor of Medical Sciences, Deputy Director for International Affairs, Chief Researcher of the Federal State Budgetary Institution The National Medical Research Center for Otorhinolaryngology of the Federal Medico-Biological Agency of Russia, Russia, Moscow; e-mail: Hasandiab@mail.ru https://orcid.org/0000-0002-2790-7900
N.A. Daikhes – Associate Member of the Russian Academy of Sciences, Doctor of Medical Sciences, Professor, Director of the Federal State Budgetary Institution The National Medical Research Center for Otorhinolaryngology of the Federal Medico-Biological Agency of Russia, Russia, Moscow; e-mail: admin@otolar.ru https://orcid.org/0000-0003-2674-4553
А.А. Bakaev – PhD applicant, Department of the Ear Diseases, FSBI NMRCO of the FMBA of Russia, Moscow; e-mail: amirbakaev1990@gmail.com
O.A. Paschinina –PhD, Head of the Branch of the Clinical Research Department of the Ear Diseases, FSBI NMRCO of the FMBA of Russia, Moscow; e-mail: Olga83@mail.ru
https://orcid.org/0000-0002-3608-2744
A.E. Mikhalevich – PhD, Junior Researcher, Clinical Research Department of the Ear Diseases, FSBI NMRCO of the FMBA of Russia, Moscow; e-mail: MikhalevichAE@mail.ru
Рецензия на статью
Актуальность статьи не вызывает сомнений. Это связано с тем, что хотя холестеатома пирамиды височной кости является довольно редкой патологией, она является локально агрессивным образованием, разрушающим костную ткань и окружающие ее структуры и может распространяться в подвисочную ямку, в среднюю и/или заднюю черепную ямку, вызывая тяжелейшие внутричерепные осложнения, которые могут приводить к летальным исходам. Кроме того, близость патологического процесса к лабиринту и лицевому нерву ставит под угрозу как слух, так и функцию лицевого нерва. Работ, посвященных этой проблеме в литературе встречается немного, в связи с чем представление результатов лечения супралабиринтной и супралабиринтной апикальной форм холестеатомы пирамиды височной кости является весьма актуальным и важным для врачей, занимающихся хирургией головы и шеи.
Review on the article
The relevance of the article is beyond doubt. This is due to the fact that despite the rarity of the cholesteatoma of the temporal bone pyramid, it is a locally aggressive tumor that destroys bone tissue and its surrounding structures, and can spread into the infratemporal fossa, into the middle and / or posterior cranial fossa, causing severe intracranial complications that can be fatal. In addition, the proximity of the pathological process to the labyrinth and the facial nerve endangers both hearing and the function of the facial nerve. There are not many works devoted to this problem in the literature, and therefore the presentation of the results of treatment of supralabyrinthine and supralabyrinthine apical forms of cholesteatoma of the temporal bone pyramid is very relevant and important for doctors involved in head and neck surgery.