Для цитирования: Мамедов У.С., Дустов Ш.Х. Возможности хирургического удаление гигантского метастатического лимфоузла шеи. Голова и шея Head and neck Russian Journal. 2019;7(2):38–41
For citation: Mamedov U.S., Dustov Sh.Kh. The opportunities for surgical removal of a giant metastatic cervical lymphnode. Head and neck Russian Journal. 2019;7(2):38–41 (in Russian).
Doi: 10.25792/HN.2019.7.2.38–41
По мнению большинства исследователей, пациенты с плоскоклеточным раком головы и шеи (ПРГШ) с ограниченными, небольшого размера опухолями могут быть излечены при использовании хирургического и/или лучевого методов лечения. Однако среди впервые выявленных больных ПРГШ более чем в 60% наблюдений диагностируют распространенные формы заболевания, характеризующиеся опухолью значительного размера с распространением в окружающие структуры шеи, с/без метастазов в регионарные лимфатические узлы и/или с отдаленными метастазами, хотя последние наблюдаются реже. Наличие у больных опухолями головы и шеи регионарных метастазов ухудшает прогноз лечения и показатели выживаемости. Основными методами лечения регионарных метастазов ПРГШ являются в основном хирургический, лучевой, химиотерапевтический методы либо их комбинация. В данной статье описан клинический пример удаления гигантской метастатической опухоли шеи плоскоклеточного рака пищевода.
Ключевые слова: плоскоклеточный рак головы и шеи, метастаз, хирургическое лечение
Авторы заявляют об отсутствии конфликта интересов. Источник финансирования. Не указан.
Для цитирования: Мамедов У.С., Дустов Ш.Х. Возможности хирургического удаление гигантского метастатического лимфоузла шеи. Голова и шея Head and neck Russian Journal. 2019;7(2):38–41
Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
According to most researchers, patients with squamous cell carcinoma of the head and neck (HNSCC) with localized, small-sized tumors can be cured by using surgical and / or radiation treatments. However, among newly diagnosed patients with HNSCC more than 60% of them are diagnosed with locally advanced tumors spreading to the surrounding structures, with or without metastases to regional lymph nodes and/or distant metastases, although the latter are less common. The presence of regional metastases in patients with head and neck tumors worsens the treatment prognosis and survival rates. The main methods of regional HNSCC metastases treatment are mainly surgery, radiation, chemotherapy, or a combination of them. This article describes a clinical example of removal of a giant squamous cell carcinoma that metastasized from esophagus.
Keywords: squamous cell carcinoma of the head and neck, metastasis, surgical treatment
Source of financing: not specified.
For citation: Mamedov U.S., Dustov Sh.Kh. The opportunities for surgical removal of a giant metastatic cervical lymphnode. Head and neck Russian Journal. 2019;7(2):38–41 (in Russian).
The authors are responsible for the originality of the data presented and the possibility of publishing illustrative material – tables, figures, photographs of patients.
В структуре онкологической заболеваемости злокачественные опухоли головы и шеи составляют 6% [3]. Наиболее часто диагностируют плоскоклеточный рак слизистой оболочки полости рта, ротоглотки, носоглотки и придаточных пазух [4]. По мнению большинства исследователей, пациенты плоскоклеточным раком головы и шеи (ПРГШ) с ограниченными, небольшого размера опухолями могут быть излечены при использовании хирургического и/или лучевого методов лечения. Однако среди впервые выявленных больных ПРГШ более чем в 60% наблюдений диагностируют распространенные формы заболевания, характеризующиеся опухолью значительного размера с распространением в окружающие структуры шеи, с/без метастазов в регионарные лимфатические узлы, реже с отдаленными метастазами (III–IVстадийи по классификации TNM) [5]. Отдаленные результаты лечения пациентов этой группы остаются неудовлетворительными, поскольку 5-летняя выживаемость при III стадии составляет 20–50%, при IV стадии не превышает 10–30% [4]. По данным Centre Oscar Lambret [6] из Франции (5161 больной) 3- и 5-летняя выживаемость больных раком полости рта составляет 41 и 30%, раком ротоглотки – 24 и 14%, раком гортаноглотки – 19 и 12%, раком гортани – 50 и 40% соответственно. Медиана выживаемости, рассчитанная у 3714 больных ПРГШ была следующей: в I стадии – 89 месяцев, II стадии – 46 месяцев, III стадии – 19 месяцев, IV стадии – 11 месяцев. Пятилетняя выживаемость больных ПРГШ в зависимости от стадии колеблется в следующих пределах: I стадия – 75–90%, II стадия – 40–70%, III стадия – 20–50%, IV стадия – 10–30% [7].
Традиционное лечение больных распространенным ПРГШ предполагает хирургическое удаление опухоли и/или химиолучевую терапию, которая при невозможности выполнения операции используется как самостоятельный метод. В частности, предоперационная радиотерапия способна помочь удалению больших опухолевых масс, но это не значит, что объем последующего хирургического вмешательства может быть уменьшен [7]. В случае комбинированного лечения 5-летняя выживаемость выше – 65–80%, но у больных нерезектабельным ПРГШ, подвергавшихся только лучевой терапии, этот показатель не превышает 18%, а медиана выживаемости – 13,3 месяца. В 60–70% наблюдений после проведенного ранее хирургического или лучевого лечения у больных ПРГШ развиваются рецидивы и/или отдаленные метастазы [8]. Однако другим важным прогностическим фактором при опухолях ПРГШ является, по мнению J.L. Lefebvre и соавт. [6], наличие пальпируемых лимфатических узлов на шее, что уменьшает ожидаемую 5-летнюю выживаемость наполовину. Имеет большое прогностическое значение также число сосудов в лимфатическом узле и эстракапсулярное распространение опухоли.
Наличие у больных злокачественными опухолями головы и шеи регионарных метастазов ухудшает прогноз лечения и показатели выживаемости [9–15]. По данным А.Х. Гейдарова [1], показатель 2-летней выживаемости в группе больных без метастазов составляет 56,8%, при метастазах, соответствующих N1–3, – 18,8%.
При этом наличие метастазов, соответствующих N1, не отражается на благоприятных результатах лечения при адекватном лечении первичного очага. В то же время наличие двусторонних и спаянных с окружающими тканями узлов (N2–3) является абсолютно неблагоприятным фактором прогноза [2]. Основным методом лечения ПРГШ с наличием регионарных метастазов является комбинированный метод [16].
Клинический случай
В отделение хирургии филиала Бухарского Республиканского специализированного научно-практического медицинского центра онкологии и радиологии поступил больной с жалобами на опухолевидное образование в области правой боковой поверхности шеи, динамическое увеличение опухоли, дискомфорт в этой области и ограничение движений шеи. Из анамнеза: пациент считает себя больным несколько месяцев и неоднократно обращался к врачам по месту жительству. С учетом динамического увеличения опухоли больной был направлен в Областной онкологический диспансер на обследование. Больному в стационарных условиях были проведены все методы обследования и осмотр специалистами: ЛОР органы – без патологии, эзофагогастродуоденоскопия – онкопатологии нет, R-графия грудной клетки и ультразвуковое исследование брюшной полости – онкопатологии нет. Осмотр онкоурологом – онкопатологии не выявлено. Мультиспиральная компьютерная томография (МСКТ) шеи – объемное образование правой поверхности шеи и надключичной области размерами 18×15×20 см, с нечеткими краями, соолидного характера. Смещение гортани и трахеи влево. Костно-деструктивных изменений не выявлено (рис. 1 а, б, в, г). Опухоль прорастает в окружающие мягкие ткани. Кровоток во внутренней яремной вене отсутствует, в общей сонной артерии (ОСА) кровоток сохранен.
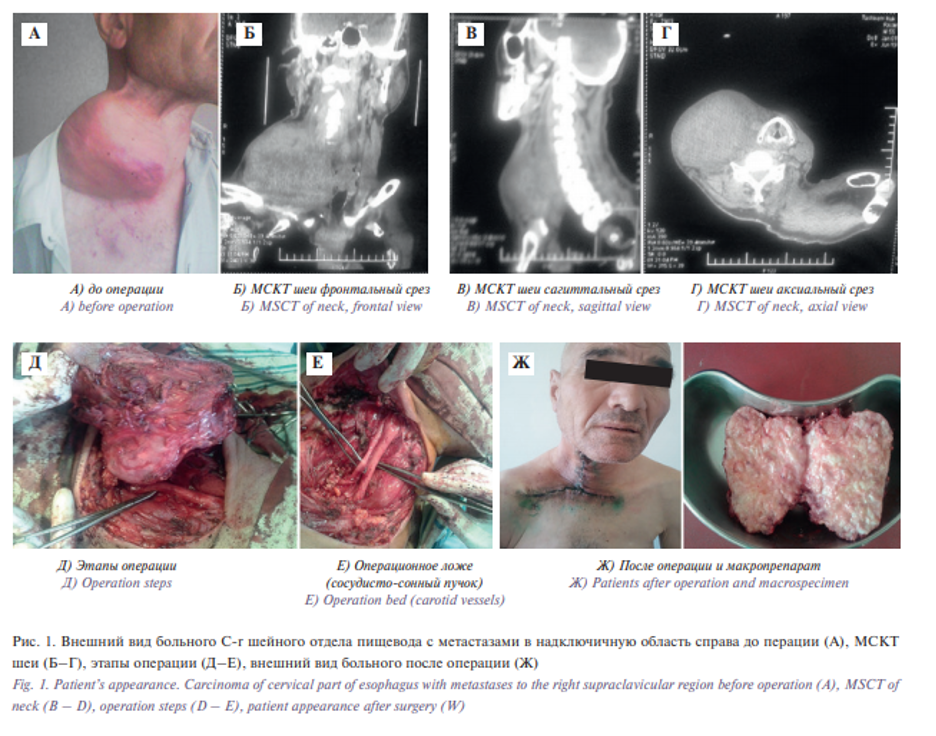
После обследования был установлен клинический диагноз: «метастазы в лимфатические узлы шеи справа без выявленного первичного очага». Учитывая размер и неуклонный рост опухолевого узла с признаками возможного распада, была выполнена операция в объеме: «расширенная лимфаденэктомия шеи справа».
Под термином «расширенные шейные диссекции» понимается дополнительное удаление лимфатических групп или не-лимфатических структур, которые не входят в объем стандартной радикальной шейной диссекции (A. Kruk-Zagajewska, Z. Szmeja, M. Wierzbicka, 2000.). Этот термин был впервые использован в 1968 г. Lipshutz и Stetzer. В литературе имеется существенно меньше информации об использовании новых подходов хирургического лечения при метастатических поражениях лимфатических узлов шеи при злокачественных опухолях области головы и шеи.
Опухоль занимала правую боковую и надключичную области шеи с вовлечением внутренней яремной вены и блуждающего нерва. Блуждающий нерв и ОСА были отделены от опухоли (рис. 1 д. е). Гистологическое заключение: «метастаз плоскоклеточного рака». Операция прошла без осложнений, и рана зажила первичным натяжением.
В сроке наблюдения до 4 месяцев больной поступил с жалобами на дисфагию во время приема пищи. При фиброгастроскопии была обнаружена опухоль верхней трети пищевода. Произведена биопсия опухоли – плоскоклеточный рак. Учитывая вышеизложенное обстоятельство, больному был поставлен диагноз: «C-r шейного отдела пищевода с метастазами в надключичную область справа. T2N0M1. Состояние после операции». Больному в дальнейшем произведена дистанционная гамматерапия+полихимиотерапия.
Больной находится под постоянным динамическим наблюдением у онколога без признаков рецидива и метастазов.
Заключение
Таким образом, распространенность регионарных метастазов и признаки их инвазивного роста, а также выход раковых клеток за пределы капсулы лимфатического узла в зоне бифуркации сонной артерии при обычном удалении приводят к высокой частоте рецидива метастазов. Накопленные новые знания о путях и закономерностях метастазирования рака в лимфоузлы шеи являются предпосылкой к усовершенствованию методики хирургического удаления лимфоузлов на шее и улучшению результатов хирургического лечения и реабилитации больных опухолями орофаренгиальной области с регионарными метастазами в лимфатические узлы шеи за счет разработки новой методики, расширенной лимфаденэктомии с резекцией сосудисто-нервных структур шеи.
ЛИТЕРАТУРА/REFERENCES
- Гейдаров А.Х. Превентивные методы воздействия на зоны регионарного метастазирования при комбинированном лечении рака подвижной части языка II–III стадии (T2N0M0-T3N0M0). Дисс. канд. мед. наук. М., 1994. [Heydarov A.Kh. Preventive treatment of regional metastasis in the combined treatment of cancer of the movable part of the tongue II – III stage (T2N0M0- T3N0M0). Diss. Cand. med. sciences. M., 1994].
- Любаев В.Л. Тактика хирургических вмешательств на регионарных зонах при местнораспространенном раке слизистой оболочки полости рта и ротоглотки с регионарными метастазами. Стоматология. 1988;67(2):43–5. [Lyubayev V.L. Tactics of surgical interventions in the regional areas with locally advanced cancer of the oral mucosa and oropharynx with regional metastases. Dentistry. 1988; 67 (2): 43–5].
- Ferlay J., Bray F., Pisani P., Parkin D.M. GLOBOCAN 2000: Cancer Incidence, Mortality and Prevalence. Worldwide, Version IARC CancerBase No. 5. Lyon, IARC Press, 2001. Limited version available from: URL: http://www_dep.iarc. fr/ globocan.htm. Last updated on 03/02/2001.
- Schantz S.P., Harrison L.B., Forastiere A.A. Tumors of the nasal cavity and paranasal sinuses, nasopharynx, oral cavity,and oropharynx, in Devita VT Jr/Hellman S, Rosenberg SA (eds): Cancer: Principles and Practice of Oncology. Philadelphia, PA: Lippincott Williams & Wilkins, 2001. P. 797–860.
- TNM Classification of malignant tumors, UICC International Union against Cancer, 5th edition. New York: Willey Liss. Inc., 1997.
- Lefebvre J.L., Lartigau E., Kara A.,Sarini J. Oral Cavity, Pharynx and Larynx Cancer. Prognostic Factors in Cancer 2 ed. Ed. M.K. Gospodarowicz, et al. New York: A. John Wiley and sons. 2001. P. 151–66.
- Laramore G.E., Coltrera M.D., Karen J.H. Tumors of Head and Neck. Cliniсal Oncology. 8th ed. Ed. Rubin Ph. Philadelphia: W.B. Saunders compani, 2001. P. 405–61.
- Marcial V.A., Pajak T.F. Radiation therapy alone or in combination with surgery оn head and neck cancer. Cancer. 1985;55(Suppl. 9): 2259–65.
- Ferlito A., Rinaldo A., Devaney K., et al. Prognostic significance of microscopic and macroscopic extracapsular spread from metastatic tumor in the cervical lymph nodes. Oral Oncol. 2002;38:747–51.
- Johansen L.V., Grau C., Overgaard J. Nodal control and surgical salvage after primary radiotherapy in 1782 patients with laryngeal and pharyngeal carcinoma. Acta Oncol. 2004;43(5):486–94.
- Jose J., Coatesworth A.P., Johnston C., et al. Cervical node metastases in squamous cell carcinoma of the upper aerodigestive tract: The significance of extracapsular spread and soft tissue deposits. Head Neck 2003; 25:451–6.
- Layland M.K., Sessions D.G., Lenox J. The influence of lymph node metastasis in the treatment of squamous cell carcinoma of the oral cavity, oropharynx, larynx and hypopharynx: N0 versus N+. Laryngoscope. 2005;115(4):629–39.
- Li X.M., Di B., Shao Y.L., et al. Clinical pathology feature and prognostic factors of cervical lymph node metastases in hypopharyngeal carcinoma. Zhonghuar Bi Yan Hou Ke Za Zhi 2004;39(12):741–5.
- Pimenta Amaral T.M., Da Silva Freire A.R., Carvalho A.L., et al. Predictive factors of occult metastasis and prognosis of clinical stages I and II squamous cell carcinoma of the tongue and floor of the mouth. Oral Oncol. 2004; 40(8):780–6.
- Rinaldo A., Devaney K.O., Ferlito A. Immunohistochemical studies in the identification of lymph node micrometastases in patients with squamous cell carcinoma of the head and neck. ORL. 2004;66(1):38–41. 16. Laramore G.E., Coltrera M.D., Karen J.H. Tumors of Head and Neck. Clinical Oncology 8-th ed. Ed. Rubin Ph. Philadelphia: W.B. Saunders compani. 2001;405–61.
Инфoрмация об авторах:
Ш.Х. Дустов – заместитель директора по лечебным вопросам Бухарского филиала Республиканского специализированного научно-практического медицинского центра онкологии и радиологии, Бухара, Узбекистан; e-mail: sherali_doc@mail.ru.
У.С. Мамедов – к.м.н., заведующий кафедрой онкологии, радиологии и лучевой диагностики Бухарского государственного медицинского института, Бухара, Республика Узбекистан; e-mail: umid_doc@mail.ru.
About the authors:
Sh.Kh. Dustov – Deputy Director for Medical Issues, Branch of the Republican Specialized Scientific and Practical Medical Center of Oncology and Radiology in Bukhara, Uzbekistan; e-mail: sherali_doc@mail.ru.
U.S. Mamedov – MD, PhD, Head of the Department of Oncology and Radiology, Bukhara State Medical Institute, Bukhara, Republic of Uzbekistan; e-mail: umid_doc@mail.ru.
