Для цитирования:
Поляков Д.П., Дайхес Н.А., Юнусов А.С., Карнеева О.В., Кондратьева Е.И., Петров А.С., Белавина П.И., Рязанская А.Г., Молодцова Е.В. Риносинусохирургия у детей с муко- висцидозом. Голова и шея. Российский журнал=Head and neck. Russian Journal. 2021;9(1):35–44 Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
Doi: 10.25792/HN.2021.9.1.35–44
Муковисцидоз (МВ) – моногенное наследственное заболевание, обусловленное мутацией гена трансмем- бранного регулятора МВ и характеризующееся поражением всех экзокринных желез, а также жизненно важных органов и систем. Одним из проявлений МВ является поражение околоносовых пазух (ОНП) в форме хронического риносинусита (ХРС), преимущественно полипозно-гнойного. ОНП рассматрива- ются как основной резервуар патогенной бактериальной и грибковой флоры и источник нисходящего инфицирования бронхов и легких. Зачастую на первое место выступает хирургическое лечение, призван- ное в т.ч. обеспечить анатомические условия для последующей доставки средств топической терапии. До настоящего времени не выработаны стандартизированные подходы к хирургическому лечению. Цель исследования. Оптимизация и оценка возможности стандартизации риносинусохирургического лечения ХРС у детей с МВ.
Материал и методы. Для анализа были отобраны 43 пациента в возрасте от 2 до 17 лет (средний воз- раст 7,9±3,73 года), оперированные в период с 2018 по 2020 г. после выработки стандартизированного в отношении верхнечелюстной пазухи (ВЧП) протокола операции в объеме удаления практически всей медиальной стенки и всей слизистой оболочки ВЧП единым блоком, передней этмоидотомии. Хирурги- ческая тактика в отношении других групп ОНП определялась данными компьютерной томографии (КТ). У 3 пациентов имелись явления вторичного стеноза слезных путей на фоне полипозной трансформации передних клеток решетчатого лабиринта. Дети были разделены на 2 группы в соответствии с субфе- нотипом ХРС: 1-я – 11 (25,6%) пациентов с псевдомукопиоцеле одной или обеих ВЧП, 2-я– 32 (74,4%) пациента с полипозно-гнойным полисинуситом с назальным полипозом II–III степеней по Johansen. Оценивали возраст пациентов, время и объем операции, учитывали случаи плохо контролируемых интраоперационных кровотечений в свете предоперационной подготовки. Эффективность лечения оценивали по потребности в реоперации в сроки катамнестического наблюдения от 6 до 34 месяцев. Результаты. В группе детей с псевдомукопиоцеле ВЧП (возраст пациентов 4,2±1,54 года) выполнялась только эндоскопическая модифицированная максиллэктомия по указанному выше протоколу в комби- нации с передней этмоидотомией. В группе пациентов с полипозно-гнойным полисинуситом (возраст 9,4±3,65 года) объем хирургического лечения был в основном дополнен задней этмоидотомией (27 детей) и сфеноидотомией (22 ребенка), операция на лобной пазухе была выполнена у 8 пациентов, аденотомия – у 5, септопластика – у 4. У 36 (86%) пациентов, по данным интраоперационного фиброскопического осмотра передне-нижних отделов ВЧП, предложенная методика позволила удалить слизистую оболочку единым блоком. Среднее время операции отличалось в двух группах: 43±12,1 и 103±26,2 минуты в I и II группах соответственно (р=0,044). У 3 пациентов была выполнена эндоскопическая дакриоцисторино- стомия, слезоотведение было восстановлено. Обратило на себя внимание возникновение плохо контр олируемых диффузных интраоперационных кровотечений в 7 случаях, 4 из которых пришлись на детей, не получавших витамин К. За время катамнестического наблюдения у 1 (2,3%) пациента потребовалось повторное хирургическое лечение.
Выводы. Разделение ХРС на фоне МВ на 2 субфенотипа представляется рациональным с точки зрения планирования оперативного вмешательства (время, объем). Тем не менее разница в среднем возрасте позволяет предположить, что субфенотипы являются стадиями одного процесса. Предложенный способ модифицированной медиальной максиллэктомии с полным удалением слизистой оболочки ВЧП единым блоком является, на наш взгляд, способом избежать раннего рецидива и превосходит по эффективности стандартный объем FESS, описанный нами в предшествующих публикациях. При наличии показаний синус-хирургия может быть дополнена аденотомией, септопластикой. Впервые в доступной литерату- ре описано выполнение эндоскопической дакриоцисториностомии у детей с МВ. Наблюдения случаев плохо контролируемых интраоперационных диффузных кровотечений у пациентов, не получавших пре- параты витамина К, доказывают необходимость их включения в схему предоперационной подготовки. Одномоментное выполнение всех требуемых этапов ринохирургического лечения в т.ч. преследует цель сокращения числа эпизодов и суммарной продолжительности общей анестезии у пациентов с потен- циально скомпрометированными функциями легких и печени. Описанная группа пациентов находится под дальнейшим катамнестическим наблюдением, что позволит оценить эффективность лечения ХРС на фоне МВ в отдаленном периоде.
Ключевые слова: муковисцидоз, кистозный фиброз, хронический риносинусит, псевдомукопиоцеле, эндоскопическая хирургия околоносовых пазух, септопластика, дакриоцисториностомия, витамин К
Cystic fibrosis (CF) is a monogenic hereditary disease caused by a mutation of the cystic fibrosis transmembrane regulator (CFTR) gene and characterized by exocrine dysfunction and multi-organ lesion. Chronic rhinosinusitis (CRS), mainly purulent-polypoid, is one of the CF manifestations. Paranasal sinuses are considered as a main reservoir of pathogenic flora and as a source of descending bronchial and lung infection. Surgery sometimes become a first-step treatment. It makes possible to deliver topical drugs. Until now, there are no any standard surgical approaches.
Aim. To optimize and standardize of rhinosinusosurgery for CRS in children with CF.
Methods. Forty-three patients aged 2 to 17 years (average age 7.9±3.73 years) operated in the period from 2018 to 2020 were included. For all patients standardized protocol for the maxillary sinus surgery (removal of almost the entire medial wall and the whole mucosa of the maxillary sinus in a single block, anterior ethmoidotomy) was performed. Surgical tactics concerning other paranasal sinuses was determined by computed tomography (CT) data. In three patients there was a secondary lacrimal stenosis caused by polypoid transformation of the anterior ethmoid. The children were divided into 2 groups according to the CRS subphenotype: 11 (25.6%) patients with pseudomucopyocele of one or both maxillary sinus and 32 (74.4%) patients with purulent-polypoid CRS with nasal polyposis stage II– III (by Johansen). The age of the patients, the surgery duration and site, cases of poorly controlled intraoperative bleeding were evaluated. The effectiveness of treatment was assessed by the need for re-operation in the period of follow-up from 6 to 34 months.
Results. In pseudomucopyocele group (age 4.2±1.54 years) only endoscopic modified maxillectomy and anterior ethmoidectomy were performed according to protocol mentioned above. In group of children with purulent-polypoid CRS (age 9.4±3.65 years) surgery besides mentioned included posterior ethmoidectomy in 27 children, sphenoidectomy – 22, frontotomy – 8, adenoidectomy – 5, septoplasty – 4. In 36 (86%) of patients the suggested technique enabled to remove mucosa fully as fibreoptic control showed. Surgery duration had a significant difference (43±12.1 and 103±26.2 minutes, p=0.044) in two groups. In 3 patients successful endoscopic dacryocystorhinostomy was performed. Poorly controlled intraoperative bleeding cases correlated with an absence of vitamin K injections in preoperative treatment scheme (4 non-treated with vitamin K patients from 7 bleeding cases). One (2.3%) patient needed re-surgery during follow-up period.
Conclusion. Division of CRS in CF into two subphenotype seems to be efficient in terms of surgery planning. Nevertheless the average age difference between the groups can suspect that such a subphenotypes are only the stages of the disease. The suggested technique of modified medial maxillectomy with whole mucosa removal is a way to prevent an early need for re-surgery and on our mind is more effective than standard FESS we published before. In presence of indications, sinus-surgery can be complemented with adenoidectomy, septoplasty. For the first time we described endoscopic dacryocystorhinostomy in children with CF. Cases of poorly controlled intraoperative bleeding once more time showed the necessity of vitamin K in preoperative treatment scheme. Simultaneous rhinosurgery steps performing is rational because of reducing of number and total duration of anesthesia in patients with potentially compromised lung and liver function. The groups are still under the prolonged follow-up to evaluate the CRS treatment effectiveness in children with CF in long-term period.
Key words: cystic fibrosis, chronic rhinosinusitis, pseudomucopyocele, endoscopic sinus surgery, septoplasty, dacryocystorhinostomy, vitamin K
Введение
Муковисцидоз (МВ) (или кистозный фиброз, cystic fibrosis) – аутосомно-рецессивное моногенное наследственное заболева- ние, обусловленное мутацией гена трансмембранного регулятора муковисцидоза (СFTR) и характеризующееся поражением всех экзокринных желез, а также жизненно важных органов и систем [1].
Распространенность МВ колеблется среди представителей европеоидов от 1:600 до 1:17 000 новорожденных. В Российской Федерации частота МВ составляет, по данным ФГБНУ «Медико- генетический научный центр им. акад. Н.П. Бочкова», 1:9000 новорожденных [2], что не позволяет считать его орфанным заболеванием и выводит на лидирующие позиции среди всех наследственных болезней. В настоящий момент сформирован Регистр больных МВ, в котором по состоянию на конец 2018 г. состоит 3142 пациента, из них 2366 – дети [3].
Одним из проявлений МВ является поражение околоносовых пазух (ОНП) в форме хронического риносинусита (ХРС), преимуще- ственно полипозно-гнойного, в основе патогенеза которого лежит сгущение секрета желез слизистой оболочки ОНП с неизбежным хроническим бактериальным воспалением на фоне вторичной цилиарной дискинезии и невозможности осуществления адек- ватного местного иммунного ответа. По данным разных источ- ников, частота развития ХРС при МВ составляет от 18,7 до 100% и, несомненно, увеличивается с возрастом ребенка [4].
Еще несколько десятков лет назад все внимание врачей-педи- атров (пульмонологов, гастроэнтерологов), осуществлявших ведение детей с МВ, было приковано исключительно к прогрес- сирующим дыхательной, сердечной, печеночной и панкреатиче- ской недостаточности как основным причинам ранней гибели пациентов. Однако определенные успехи в лечении больных данной категории (внедрение генной терапии, трансплантация легких и печени) в значительной мере позволили уделять вни- мание считавшимся ранее второстепенным проявлениям, в т.ч. поражению ОНП. Тем не менее роль поражения синоназальной области при МВ сложно переоценить: во-первых, ОНП, по дан- ным большинства исследований, служат источником нисхо- дящей бактериальной (а иногда и грибковой) контаминации бронхов и легких, приводя к прогрессивной смене патогенов в сторону более агрессивных возбудителей [5, 6]; во-вторых, проявления ХРС снижают качество жизни пациентов; в-третьих, постоянное ротовое дыхание вследствие хронической назальной обструкции оказывает прямое повреждающее действие на ском- прометированную бронхолегочную систему за счет отсутствия адекватного физиологического кондиционирования воздуха в полости носа и ОНП [7]; в-четвертых, сопровождающие ХРС обонятельные расстройства потенциально могут влиять на пищевое поведение пациентов и тем самым усугублять име- ющиеся нарушения нутритивного статуса [8].
ХРС на фоне МВ по многим характеристикам (возрасту дебю- та, патогенезу, микробиологии, изменениям, выявляемым при КТ, и др.) значительно отличается от поражения ОНП в отсут- ствии данного системного заболевания, что было признано в последней редакции Европейского согласительного документа по синуситам и назальному полипозу (EPOS, 2020), выделивше- го его в отдельный фенотип ХРС – т.н. «вторичный диффузный (двусторонний) механический» хронический риносинусит [9]. Это свидетельствует и об особой тактике лечения подобного рода патологии синоназальной области.
Основными направлениями топической терапии, помимо привычных в лечении ХРС ирригационной терапии, интраназаль ных глюкокортикостероидов, является местное использование антибактериальных средств (аминогликозиды, колистиметат натрия), дорназы-альфа. Тем не менее эффективность подоб- ной терапии очевидно значительно снижается или эффект вовсе отсутствует при механической непроходимости полости носа и соустий ОНП, на содержимое и слизистую оболочку которых она направлена. Системная же антибактериальная, противо- воспалительная и муколитическая терапия также оказывается недостаточной в связи со снижением пенетрации препаратов в условиях фиброзных изменений слизистой оболочки ОНП и повышенной вязкости секрета [9, 10].
Таким образом, в случае выраженного «блокирующего» полипозно-гнойного процесса в ОНП на фоне МВ на первое место выступает хирургическое лечение, призванное не излечить от ХРС, а в т.ч. обеспечить анатомические условия для последу- ющей доставки средств топической терапии, которая в свою оче- редь, по мнению Z. Zheng и соавт., становится адъювантной [11].
Хирургическому лечению, по данным анализа работы 29 крупнейших педиатрических клиник в США, подвергаются от 1 до 24% детей с МВ [12], а по данным Z. Zheng и соавт., от 20 до 60% пациентов с МВ требуют ринохирургического лечения [11].
Несмотря на возрастающее число публикаций, посвященных риносинусохирургии при МВ, до сих пор отсутствует какой- либо стандартизированный подход как к определению сроков и показаний, так и к объему (радикальности) вмешательства. Об этом свидетельствует и публикация «Working towards consensus in the management of pediatric chronic rhinosinusitis in cystic fibrosis», вышедшая в августе 2020 г., в которой ведущие миро- вые эксперты в области МВ и оториноларингологии не смогли прийти к согласию по подавляющему числу вопросов [13].
Еще в 1998 г. в Бельгии состоялся Консенсус, определяющий показания к функциональным эндоскопическим вмешательст- вам на околоносовых пазухах (FESS – Functional Endoscopic Sinus Surgery) у детей, который поставил формулировку «Полная назальная обструкция за счет полипоза или медиализации латеральной стенки полости носа на фоне муковисцидоза» на первое место среди 9 абсолютных показаний. С тех пор эндоскопический доступ к ОНП у детей с МВ считается методом выбора, однако вплоть до последнего времени в нашей стране сохранялись сторонники «открытой» хирургии по типу Caldwell- Luc, рекомендуя выполнение радикальной операции на верх- нечелюстных пазухах (ВЧП) и клетках решетчатого лабиринта при возрасте пациентов с МВ старше 5 лет, а в более младшем возрасте предлагая полипотомию носа как максимальный объем возможного хирургического лечения [14].
Эффективность FESS у пациентов данной группы к насто- ящему времени подтверждена тремя крупными систематиче- скими обзорами [15–17] и не вызывает сомнений. Критерии эффективности, помимо клинической симптоматики самого ХРС, эндоскопической картины и влияния на качество жизни, обычно включают снижение частоты обращений/госпитализаций по поводу обострений бронхолегочного процесса, снижение выделения патогенной флоры из верхних и нижних дыхательных путей и влияние на показатели функции внешнего дыхания. При этом воздействие FESS на последний параметр до сих пор остается противоречивым.
Предлагаемый в современной литературе объем хирургиче- ского лечения ХРС на фоне МВ колеблется от стандартной эндо- скопической полисинусотомии до радикальных вмешательств в объеме эндоскопической медиальной максиллэктомии (EMM) и даже радикальную пансинусотомию с полным удалением передней и нижней стенок клиновидной пазухи, резекцией средних носовых раковин и операцией на лобных пазухах типа Draf III/Lathrop [18]. Сторонники более расширенных эндоско- пических операций справедливо апеллируют к необходимости максимального дренирования ВЧП (как наибольшей по объему) в полость носа. В силу известных анатомических особенно- стей – расположения естественного соустья в верхних отделах синуса – неизбежным становится повторное скопление густого секрета в прооперированных в меньшем объеме ВЧП в силу отсутствия мукоцилиарного клиренса. Поэтому главной целью операции в данном случае становится не вентиляция пазухи, а объединение ее с полостью носа для пассивного дренирования и создания наиболее благоприятных анатомических условий для инструментальной санации в амбулаторных условиях и, как было отмечено выше, доступа лекарственных веществ [19]. В связи с этим предложен термин «gravity-dependent drainage surgery» (т.е. хирургическое создание гравитационно-зависимого дре- нажа ОНП) [11], что опять же в силу указанных анатомических свойств ставит во главу угла ВЧП.
Ряд авторов предлагают т.н. модифицированную медиальную максиллэктомию (MEMM) с удалением практически всей меди- альной стенки ВЧП (ее марсупиализацию), однако с сохранением головки нижней носовой раковины и слезных путей [20].
Противники расширенных вмешательств на ОНП в свою очередь обосновывают меньшую инвазивность лечения все возрастающей продолжительностью жизни пациентов с МВ, что увеличивает число вмешательств на ОНП и при многократных операциях создает риск выраженного спаечного и/или атрофи- ческого процесса и развития синдрома «пустого носа». Более того, потеря основных внутриносовых ориентиров затрудняет проведение последующих процедур и повышает риск осложне- ний при ревизионных вмешательствах [21].
К сожалению, зачастую независимо от радикальности про- веденного хирургического лечения, частота рецидивирования и потребность в повторном хирургическом лечении в течение 4 лет после первичной операции составляют 46–100% [22, 23]. По-видимому, необходимость повторных вмешательств – крайне многофакторная проблема, включающая в себя и тип мутации гена CFTR, и микробиологический статус, и степень привержен- ности послеоперационному лечению.
Еще одним аспектом является безопасность хирургии, которая в соответствии с некоторыми исследованиями, значительно усту- пает таковой у пациентов без МВ. Если частота осложнений при FESS в педиатрической популяции больных составляет 1,4% [24], то на фоне МВ, по данным F.D. Albritton и T.T. Kingdom, достигает 11,5% [25]. Объяснение большей распространенности ослож- нений при МВ может быть связано с несколькими факторами. Во-первых, кровотечения могут быть обусловлены наличием _ у многих пациентов коагулопатии за счет дефицита витамин-К- зависимых факторов свертывания на фоне панкреатической недо- статочности и нарушения всасывания жиров. Во-вторых, вероят- ность интраоперационных осложнений возрастает при выраженном ремоделировании внутриносовых структур, характерном для МВ, а также послеоперационных изменениях в случае ревизионной хирургии после радикальных эндоназальных операций.
В имеющихся на данный момент многочисленных исследова- ниях, посвященных риносинусохирургии у детей с МВ, на наш взгляд, есть и ряд недостатков: отсутствие внимания к смежным анатомическим областям (внутриносовые структуры, носоглот- ка) и предоперационной подготовке, отсутствие попытки класси- фицировать состояние ОНП и стандартизировать в соответствии с ними хирургический протокол, оценка результатов лечения в разнородных по объему вмешательства группах.
Цель исследования. Оптимизация и оценка возможности стандартизации риносинусохирургического лечения ХРС у детей с МВ.
Материал и методы
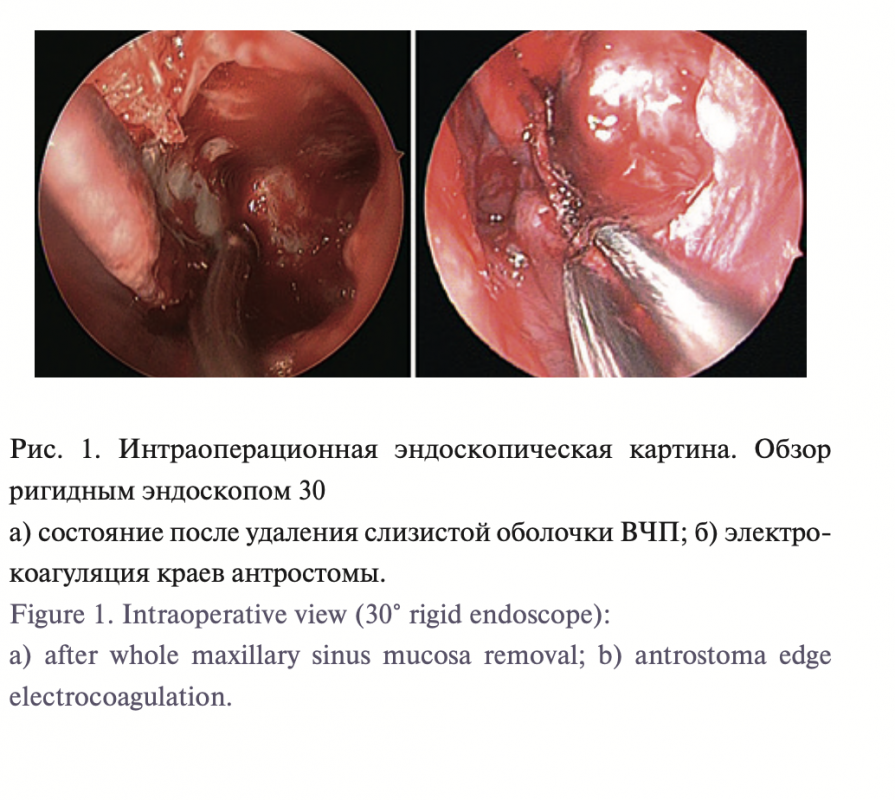
За период с 2006 по 2020 г. коллективом авторов проконсуль- тированы более 300 пациентов с МВ, выполнено 107 операций у 73 пациентов. Для данного анализа были отобраны 43 паци- ента в возрасте от 2 до 17 лет (средний возраст 7,9±3,73 года), оперированные в период с 2018 по 2020 г. после выработки стандартизированного в отношении ВЧП протокола операции в объеме удаления практически всей медиальной стенки от уровня задней ее стенки сзади, орбитальной стенки сверху, лобного отростка верхней челюсти (слезных путей без их пере- сечения) спереди, нижней носовой раковины с частичным уда- лением ее остова и сохранением переднего конца снизу (в наи- большей степени соответствует «консервативной» MME I типа по C. Georgalas и M. Tsounis [26] или MEMM IIa типа по P. Thulasidas и V. Vaidyanathan [27]). Обязательным услови- ем являлось удаление слизистой оболочки ВЧП с началом ее отсепаровки на уровне границы задней, медиальной и орбиталь- ной стенок с отделением ее от надкостницы последовательно в латеральном, переднем и нижнем направлениях. Кроме того, во всех случаях выполнялась электрокоагуляция слизистой оболочки по периметру образованной мегаантростомы, а также передняя этмоидотомия (рис. 1).
Хирургическая тактика в отношении задних клеток решет- чатого лабиринта, лобных и клиновидных пазух определялась данными КТ ОНП.
Дети принципиально были разделены на 2 группы в соответ- ствии с характером патологии ВЧП, отраженным на КТ:
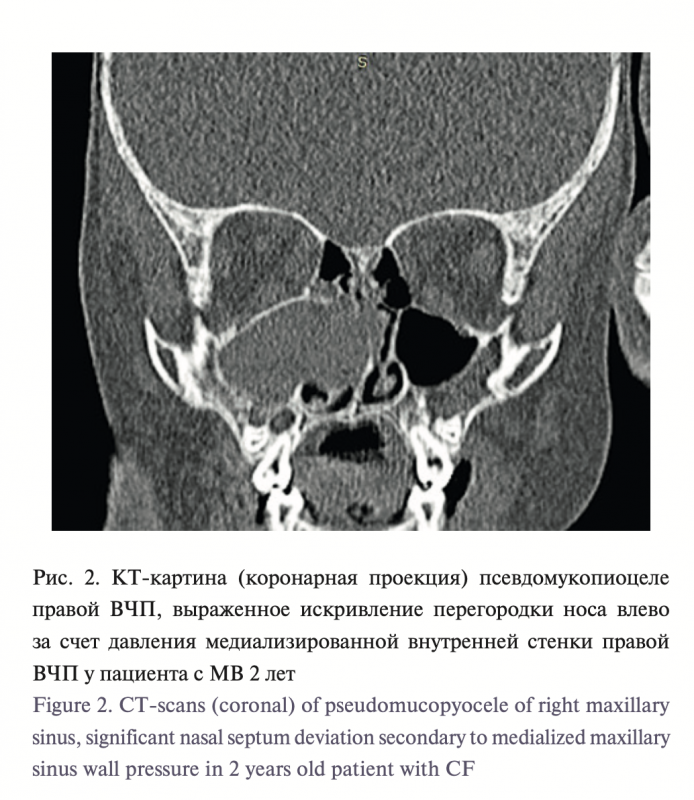
1. Псевдомукопиоцеле одной или обеих ВЧП (состояние ВЧП, характерное для МВ; в отличие от мукоцеле пути дренажа синуса сохранены, однако они недостаточны в силу высокой вязкости секрета, что приводит к аналогичной таковой при мукоцеле деформации ее стенок, прежде всего, медиальной) – 11 (25,6%) пациентов (рис. 2).
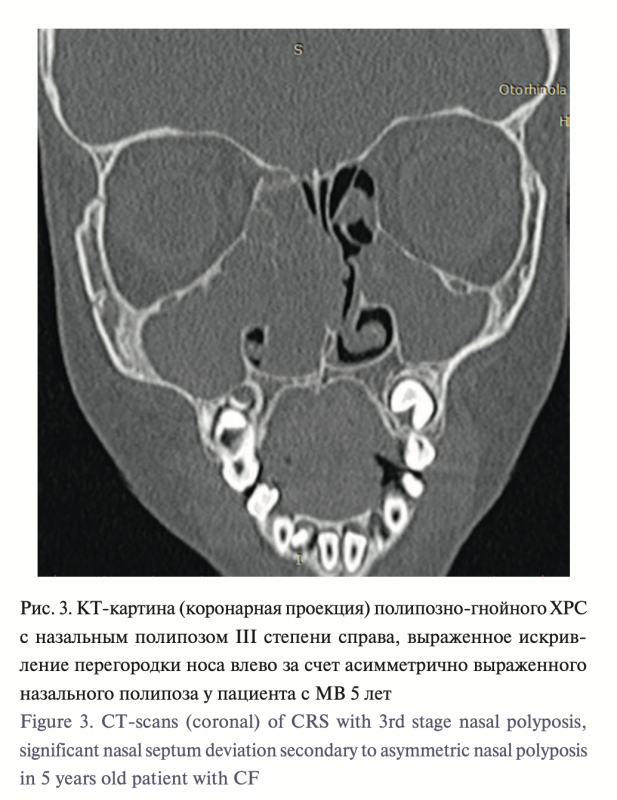
2. Полипозно-гнойный полисинусит, сопровождающийся назаль- ным полипозом II–III степеней по L.V. Johansen – 32 (74,4%) пациента (рис. 3).
У 38 (88,4%) пациентов были выполнены первичные опера- ции, у 5 (11,6%) имелся анамнез ринохирургического лечения (как «открытых», так и эндоскопических операций).
Кроме того, у 3 пациентов имелись явления односторонне- го хронического дакриоцистита, обусловленного вторичным стенозом слезных путей на фоне расширения и полипозной трансформации передних клеток решетчатого лабиринта.
Оценивали наличие и степень искривления перегородки носа, гипертрофии глоточной миндалины и потребность в соответ- ствующем хирургическом лечении. Учитывали случаи плохо контролируемых интраоперационных кровотечений в свете предоперационной подготовки, а именно назначения препарата витамина К.
Эффективность лечения оценивалась, прежде всего, по кли- нической потребности в реоперации в сроки катамнестического наблюдения от 6 до 34 месяцев. К сожалению, возможность оценки эффективности риносинусохирургии по более объективным показателям, принятым для ХРС в общей популя- ции, таким как динамика качества жизни по валидированным опросникам (SN-5, SNOT-22 и др.) и сравнения КТ-изменений по шкалам (Lund-Mackay, Lund-Kennedy), по данным многих исследователей, остается крайне противоречивой именно в группе пациентов с МВ [28–31].
Результаты
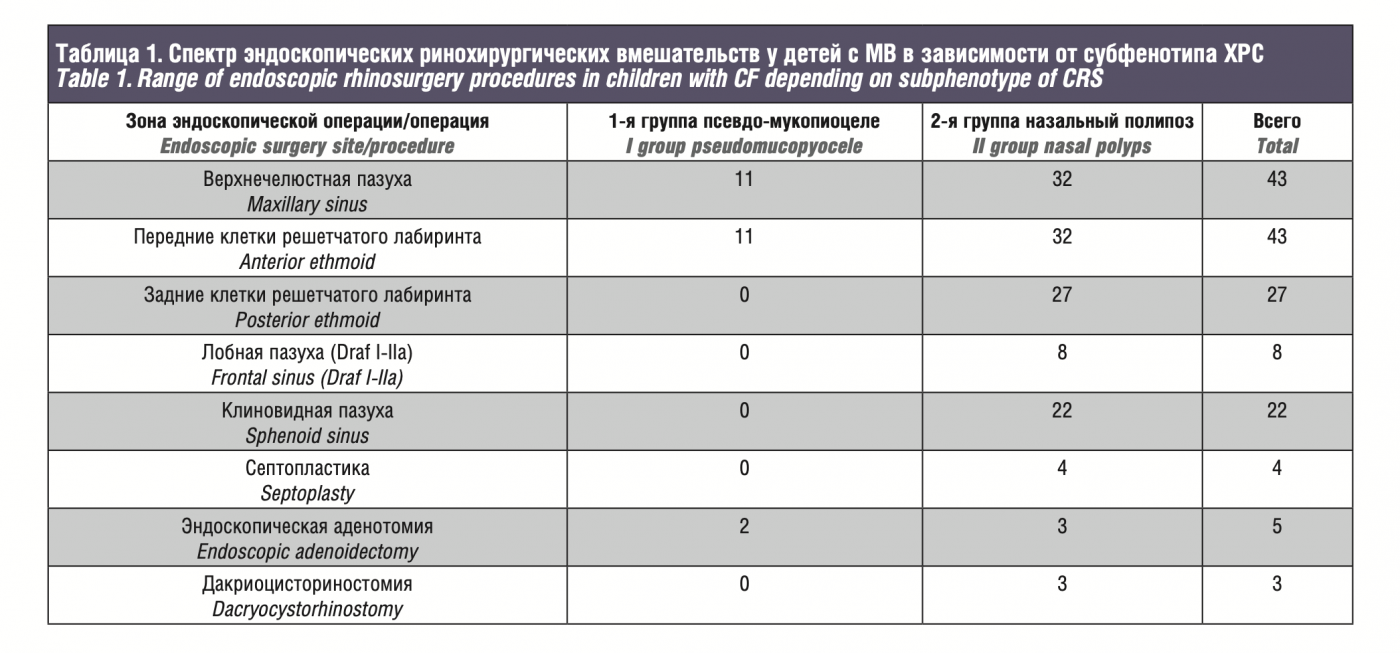
Объем эндоскопической операции в 2 группах представлен в таблице.
Закономерно в группе детей с псевдомукопиоцеле ВЧП (сред- ний возраст пациентов 4,2±1,54 года) выполнялась только эндо скопическая модифицированная максиллэктомия по указанному выше протоколу в комбинации с передней этмоидотомией. В группе пациентов с полипозно-гнойным полисинуситом (сред- ний возраст 9,4±3,65 года) объем хирургического лечения был в основном дополнен задней этмоидотомией и сфеноидотомией, а операция на лобной пазухе была выполнена всего у 8 пациен- тов. Учитывая объем выборки, несмотря на видимые возрастные различия в двух группах, они оказались недостоверными (р=0,197).
У 36 (86%) пациентов, по данным интраоперационного фибро- скопического осмотра передненижних отделов ВЧП (обычно недоступных для визуализации с помощью стандартных угло- вых ригидных эндоскопов), предложенная методика позволи- ла удалить слизистую оболочку полностью единым блоком («мешком»).
У 5 пациентов в обеих группах в связи с выраженной гипер- трофией глоточной миндалины, верифицированной на основа- нии эндоскопии, одномоментно была выполнена эндоскопиче- ская шейверная аденотомия. К септопластике для обеспечения доступа к ОНП мы были вынуждены прибегнуть в 4 случаях у пациентов 2-й группы. Ранние гнойные и отсроченные ослож- нения септопластики отсутствовали.
Среднее время операции составило 87,4±35,17 минут и зна- чительно отличалось в двух группах: 43±12,1 и 103±26,2 минуты в 1-й и 2-й группах соответственно (р=0,044).
За время катамнестического наблюдения у 1 (2,3%) пациента с полипозно-гнойным полисинуситом и двусторонним назальным полипозом III степени по Johansen через 13 месяцев после первичного вмешательства, выполненного в возрасте 4 лет, в связи с рецидивом была выполнена реоперация.
У 3 пациентов с «вторичным риногенным» дакриоциститом при вскрытии расширенных и деформированных передних клеток решетчатого лабиринта был обнаружен дефект кост- ного ложа слезного мешка, который во избежание рецидива дакриоцистита на фоне дальнейшего течения ХРС был расши- рен кпереди, слезный мешок вскрыт, его слизистая оболочка вывернута на латеральную стенку полости носа по классической методике эндоназальной эндоскопической дакриоцисторино- стомии. Слезный мешок тампонировался на 2 недели гемоста- тическим материалом, стентирование не выполнялось. У всех пациентов непосредственно после операции было восстановлено слезоотведение, при катамнезе от 13 до 30 месяцев рецидива не наступило, при контрольных эндоскопических осмотрах функция стомы сохранена.
Большинство пациентов в плане предоперационной подго- товки парентерально получали препарат витамина К (менадиона натрия бисульфит), однако у 6 пациентов подобная терапия по разным причинам не проводилась. При этом обратило на себя внимание возникновение плохо контролируемых диффузных интраоперационных кровотечений в 7 случаях, 4 из которых пришлись именно на детей, не получавших витамин К. Иных интра- и послеоперационных осложнений зарегистрировано не было.
Обсуждение
В свете выделения в EPOS2020 ХРС на фоне МВ в отдель- ный фенотип, что в силу особенностей этиологии и патогене- за представляется абсолютно обоснованным, предложенная группировка по характеру процесса в ОНП на 2 субфенотипа – псевдомукопиоцеле и полипозно-гнойный ХРС с назальным полипозом – с практической точки зрения несет в себе дифференцированный подход к планированию хирургического вмешательства (достоверно отличается длительность операции, объем). С другой стороны, полученные возрастные различия в этих группах – средний возраст составил 4,2±1,54 и 9,4±3,65 года соответственно (недостоверные, вероятно, из-за неболь- шого объема выборки) могут свидетельствовать о том, что эти 2 вида изменений в ОНП являются стадиями одного процесса, растянутого во времени.
Предложенный способ модифицированной медиальной максиллэктомии с полным удалением слизистой оболочки ВЧП единым блоком является, на наш взгляд, способом избе- жать раннего рецидива и превосходит по эффективности стандартный объем FESS, описанный нами в предшествую- щих публикациях [32, 33]. Подобное выделение и удаление слизистой оболочки единым блоком становится возможным, по-видимому, в силу выраженного ее утолщения и фиброза и позволяет избежать более травматичных доступов, таких как премаксиллярный или комбинированный (эндоскопический и сублабиальный). Такой подход противоречит принципам функциональности эндоскопической синус-хирургии, однако сохранение слизистой оболочки представляется нецелесоо- бразным в связи с имеющейся при МВ вторичной цилиарной дискинезией, а формирование новой эпителиальной выстилки, наиболее вероятно, сопряжено с меньшей представленностью слизистых желез, что требует, однако, дальнейших гистологи- ческих исследований. Операции на лобной пазухе выполняются реже всего по причине ее гипоплазии у большинства пациентов с МВ, а объем операции обычно не превышает Draf IIa в соот- ветствии с принципом создания гравитационно-зависимого дренажа ОНП.
Кроме того, полный объем риносинусохирургического лече- ния, помимо синусотомий, по показаниям может включать аденотомию, септопластику, а также дакриоцисториностомию, что не отражено ни в одной из изученных нами публикаций. При этом, по нашим наблюдениям, искривление перегород- ки носа имеет место у большинства пациентов с ХРС при МВ за счет механического давления на фоне асимметричного патологического процесса в ОНП (медиализация внутренней стенки ВЧП, назальный полипоз). Принимая во внимание риски бактериальных осложнений при одномоментной септо- пластике и дренировании ОНП, являющихся источником пато- генной, зачастую полирезистентной, флоры, в ряде случаев операция на перегородке носа является неизбежным этапом хирургического лечения в связи с невозможностью доступа к латеральной стенке полости носа. Тем не менее в описан- ной нами серии наблюдений на фоне адекватной периопера- ционной антибактериальной терапии подобные осложнения отсутствовали.
Одномоментное выполнение всех требуемых этапов рино- хирургического лечения представляется рациональным, в т.ч. и с целью сокращения числа эпизодов и суммарной про- должительности общей анестезии у пациентов с потенциально скомпрометированными функциями легких и печени.
Наблюдения случаев плохо контролируемых интраопераци- онных диффузных кровотечений у пациентов, не получавших препараты витамина К для парентерального введения, еще раз доказывают необходимость их включения в схему предопера- ционной подготовки. Описанная группа пациентов находится под дальнейшим катамнестическим наблюдением, что позволит в дальнейшем оценить эффективность лечения ХРС на фоне МВ в более отдаленном периоде.