Для цитирования: Кузнецов М.С., Воронов А.В., Савелло А.В., Дворянчиков В.В., Гофман В.Р., Киреев П.В. Клинический случай диагностики и лечения эпителиоидной гемангиоэндотелиомы синоназальной локализации. Голова и шея. Российский журнал Head and neck Russian Journal. 2020;8(2):59–64
For citation: Kuznecov M.S., Voronov A.V., Savello A.V., Dvorjanchikov V.V., Kireev P.V. Diagnosis and treatment of epitelioid hemangioedothelioma of synonasal localization: clinical case. Head and neck Russian Journal. 2020;8(2):59–64 (in Russian).
Введение.
Эпителиоидная гемангиоэндотелиома – редкая сосудистая эндотелиальная опухоль низкой степени злокачественности, которая поражает взрослых всех возрастных групп и локализуется, как правило, в мягких тканях, печени, легких и костях. О поражении данной опухолью полости носа и околоносовых пазух имеются единичные публикации. Редкость этого новообразования, необычное анатомическое расположение и неспецифические симптомы создают проблемы для диагностики и лечения. В постановке диагноза основную роль играют иммуногистохимические и молекулярно-генетические методы исследования. Лечение заключается в радикальном хирургическом удалении опухоли и последующем наблюдении для контроля рецидива.
Клинический случай. Пациентка 60 лет, предъявляла жалобы на периодические носовые кровотечения, затруднение носового дыхания в течение 6 месяцев. По результатам эндоскопического осмотра, данных КТ и МРТ исследований с контрастированием, эндоваскулярной ангиографии была обнаружена хорошо васкуляризованная опухоль синоназальной локализации размерами 65×60×47 мм, вызывающая костную деструкцию стенок верхнечелюстных пазух, решетчатого лабиринта, медиальной стенки левой орбиты с проникновением в нее, крыло-небную и подвисочную ямки слева. После выполнения эмболизации сосудистой сети опухоли выполнена эндоназальная эндоскопическая резекция опухоли под контролем электромагнитной навигационной стации с использованием ринохирургического инструментария, лазерной техники. После проведения гистологического и иммуногистохимического анализов диагноз «эпителиодная гемангиоэндотелиома» подтвержден. При контрольном МРТ исследовании ткань опухоли не определялась.
Заключение. Эндоназальная эндоскопическая резекция эпителиоидной гемангиоэндотелиомы синоназальной локализации является методом выбора лечения данной опухоли. В диагностике необходимо использовать иммуногистохимические и молекулярно-генетические методы исследования.
Ключевые слова: эндоскопическая ринохирургия, эпителиодная гемангиоэндотелиома, лазер, электромагнитная навигация Конфликт интересов.
Авторы заявляют об отсутствии конфликта интересов. Финансирование. Работа выполнена без спонсорской поддержки.
Для цитирования: Кузнецов М.С., Воронов А.В., Савелло А.В., Дворянчиков В.В., Гофман В.Р., Киреев П.В. Клинический случай диагностики и лечения эпителиоидной гемангиоэндотелиомы синоназальной локализации. Голова и шея. Российский журнал Head and neck Russian Journal. 2020;8(2):59–64
Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
Introduction. Epithelioid hemangioendothelioma is a rare vascular endothelial tumor, of low malignancy, which affects adults of all age groups and is mostly often localized in soft tissues, liver, lungs and bones. There is а few number of publications about this tumor lesion in the nasal cavity and paranasal sinuses. The rarity of this tumor, unusual anatomical location and nonspecific symptoms create problems for diagnosis and treatment. Immunohistochemical and moleculargenetic research methods play a major role in the diagnosis. Treatment consists of radical surgical removal of the tumor and follow-up to control relapse
Clinical case. Рatient of 60 years was troubled by complaints of nosebleeds, difficulty in nasal breathing for 6 months. According to the results of endoscopic examination, contrast-enhanced CT and MRI examinations, and endovascular angiography, a well-vascularized tumor of sinonasal localization with dimensions of 65×60×47 mm was detected, causing bone destruction of the walls of the maxillary sinuses, the ethmoid bone, the medial wall of the left orbit with penetration into it, left pterygopalatine and infratemporal fossae. After embolization of the tumor vessels, endonasal endoscopic resection of the tumor was performed under the control of electromagnetic navigation station using rhinosurgical instruments, laser technology. After histological and immunohistochemical analysis, the diagnosis of epithelial hemangioendoteoioma was confirmed. In control MRI examination, tumor tissue is not determined.
Conclusion. Endonasal endoscopic resection of epithelioid hemangioendothelioma of synonasal localization is the method of choice in the treatment of this tumor. It is necessary to use immunohistochemical and molecular-genetic methods of research in diagnosis of the disease.
Key words: endoscopic rhinosurgery, epithelial hemangioendothelioma, laser, electromagnetic navigation
Conflicts of interest. The authors have no conflicts of interest to declare.
Funding. There was no funding for this study.
For citation: Kuznecov M.S., Voronov A.V., Savello A.V., Dvorjanchikov V.V., Kireev P.V. Diagnosis and treatment of epitelioid hemangioedothelioma of synonasal localization: clinical case. Head and neck Russian Journal. 2020;8(2):59–64 (in Russian).
The authors are responsible for the originality of the data presented and the possibility of publishing illustrative material – tables, figures, photographs of patients.
Введение
Эпителиоидная гемангиоэндотелиома (ЭГЭ) впервые описана в 1982 г. S. Weiss и F. Enzinger [1]. Она состоит из округлых или слегка веретенообразных эозинофильных эндотелиальных клеток с округлыми ядрами и выраженной цитоплазматической вакуолизацией. Клетки группами окружают хорошо сформированные сосудистые каналы [2]. Опухоль часто ошибочно интерпретируют как карциному, в отличие от которой для ЭГЭ характерно отсутствие плеоморфизма и митотической активности, а также наличие очаговых сосудистых каналов [3]. Она является сосудистой эндотелиальной опухолью низкой степени гистологической злокачественности, поражает взрослых всех возрастных групп, обоих полов и локализуется, как правило, в мягких тканях, печени, легких и костях [4–8]. Дифференциальную диагностику ЭГЭ проводят с карциномой, миоэпителиальной опухолью, эпителиоидной саркомой, мезотелиомой, миксоидной хондросаркомой, миксоидной липосаркомой и особенно с другими сосудистыми опухолями, такими как эпителиоидная гемангиома, кожный эпителиоидный ангиоматозный узел, эпителиоидная ангиосаркома и псевдомиогенная гемангиоэндотелиома. Огромную роль в этом играет использование иммуногистохимического и молекулярно-генетического методов исследования [9]. Синоназальная локализация опухоли крайне редка, что представляет несомненный интерес в плане диагностики и лечения.
Клинический случай
Пациентка 60 лет поступила в клинику оториноларингологии ВМедА в ноябре 2019 г. Считала себя больной около 6 месяцев, когда стала отмечать постепенное затруднение носового дыхания через левую половину носа, около 3–4 месяцев отмечала периодические кровотечения из левой половины носа. Обследована по месту жительства, был установлен диагноз «Сосудистая опухоль левой половины носа с поражением левой верхнечелюстной пазухи, клеток решетчатого лабиринта слева. Рецидивирующие носовые кровотечения». Результат гистологического исследования при поступлении: сосудистая опухоль с эрозированием. Дифференциальный диагноз между гиперпластической гемангиомой и гемангиоперицитомой без отчетливых признаков злокачественности.
При осмотре с помощью эндоскопической оптики в левой половине носа визуализировалось образование розово-фиолетового цвета с инъецированными сосудами, ровной, гладкой поверхностью, плотно-эластичной консистенции, кровоточащее при дотрагивании зондом, смещающее перегородку носа вправо. Задние отделы носа необозримы. При пальцевом исследовании носоглотки образование заполняет ее просвет, плотно-эластичной консистенции, смещаемо. В правой половине носа слизистая оболочка розовая, бледная. Просвет общего носового хода сужен за счет отека и смещения перегородки носа вправо. Носовое дыхание затруднено.
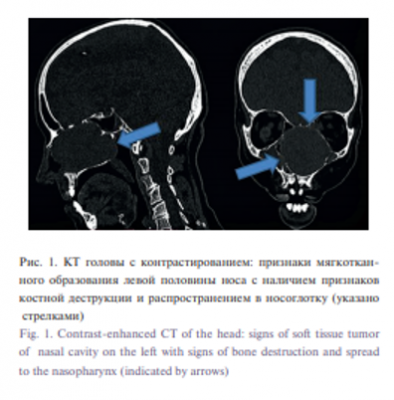
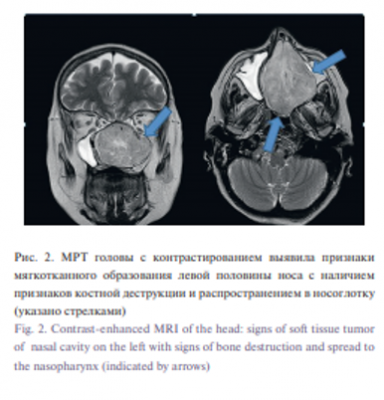
По результатам компьютерной томографии (КТ) с введением контрастного вещества, определялось объемное образование округлой формы, размерами 65×60×47 мм, с ровными четкими контурами, которое компримировало и оттесняло медиальные стенки верхнечелюстных пазух латерально, перегородку носа вправо. Отмечалась деструкция бумажной пластинки слева с пролабированием опухоли в полость орбиты. Образование ремоделировало и истончало переднюю стенку клиновидной и нижнюю стенку лобной пазухи. Активно накапливало контрастное вещество больше по периферии, слабее в центральных отделах (рис. 1). По результатам магнитно-резонансной томографии (МРТ) с введением контрастного вещества определялось объемное образование округлой формы, размерами 65×60×47 мм, с ровными четкими контурами. Структура образования неоднородная, сигнал изогиперинтенсивный на T2 взвешенных изображениях, изогипоинтенсивный на Т1 взвешенных изображениях, диффузия не ограничена. Отмечалось негомогенное интенсивное накопление образованием контрастного вещества с наличием центрального неправильной формы дефекта контрастирования. На изображениях, взвешенных по Т2, в структуре образования выявлялись прерывистые тонкие линейные гипоинтенсивные участки, вероятно, сосуды (рис. 2).
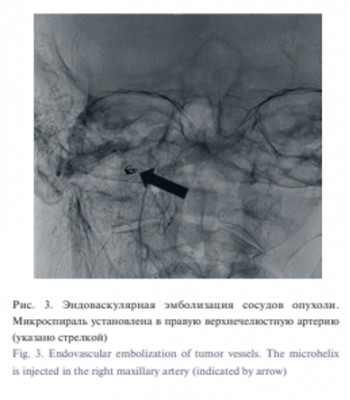
По данным ангиографии выявлено, что источником кровоснабжения опухоли являлись ветви верхнечелюстных артерий с обеих сторон и этмоидальных артерий слева. В связи с этим выполнена эмболизация собственной сосудистой сети опухоли микрочастицами слева, в правую верхнечелюстную артерию установлена микроспираль (рис. 3).
Перед операцией пациентка проконсультирована нейрохирургом и офтальмологом. Принято решение о выполнении эндоскопической навигационно-ассистированной операции по удалению опухоли.
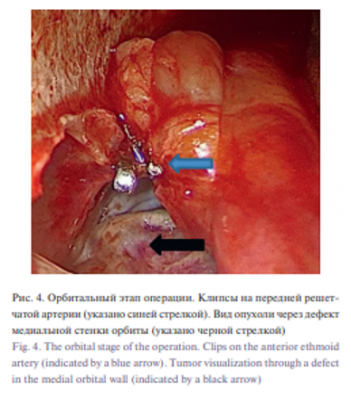
Операция включала ряд этапов. На первом для предотвращения развития кровотечения из опухоли выполнена орбитотомия наружным доступом. Осуществлен разрез по надбровной дуге длиной 4 см, периорбита отделена от медиальной стенки орбиты, под эндоскопическим контролем визуализированы передняя и задняя решетчатые артерии, с помощью клип-апликатора на каждый из сосудов наложено по две клипсы, сосуды коагулированы, пересечены. Визуализирован дефект медиальной стенки орбиты, через который пролабировала опухоль (рис. 4).
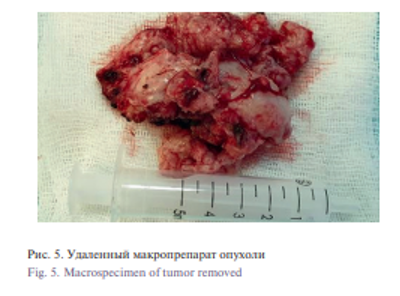
На втором этапе под эндоскопическим контролем выполнялась вапоризация опухолевой ткани с применением CO2 -лазера и обработка стромы опухоли с использованием диодного лазера для создания достаточного операционного коридора. На третьем этапе с помощью техники «в четыре руки» под контролем электромагнитной навигационной стации с применением ринохирургического инструментария, биполярных коагуляционных щипцов, диодного лазера опухоль была выделена и удалена через ротоглотку (рис. 5).
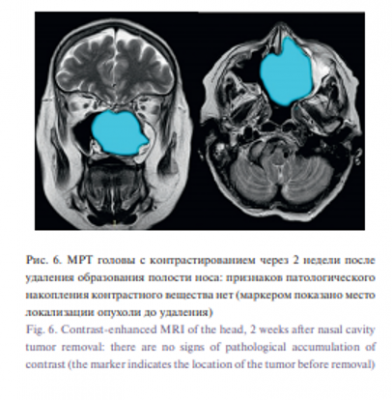
Пациентка перенесла операцию хорошо. Кровопотеря составила около 100 мл. При проведении гистологического и иммуногистохимического анализов удаленного материала использовали следующие реакции и окраски: Vimentin, Flyl, Ki67, BCL2, CD34, Caldesmon, S100, AelAe3. При микроскопическом анализе определялась эпителиодоклеточная опухоль солидного строения, с большим количеством тонкостенных сосудов и сосудистых щелей, зонами папиллярного строения. Степень ядерной атипии низкая. Митотические фигуры единичные, не атипические. По результатам морфологических исследований установлен окончательный диагноз: «эпителиодная гемангиоэпителиома». По данным МРТ с контрастированием, выполненной через 2 недели после операции, опухоль удалена радикально, участков патологического накопления контрастного вещества не определялось (рис. 6).
Обсуждение
ЭГЭ относится к редким сосудистым опухолям, морфологические особенности которой могут быть ошибочно приняты за эпителиальные опухоли, включая карциному, меланому и мезотелиому [10, 11]. Дифференциальную диагностику необходимо проводить с высокоагрессивной сосудистой злокачественной опухолью – эпителиальной ангиосаркомой [12]. В отличие от нее ЭГЭ свойственны только местные рецидивы при нерадикальном хирургическом удалении [13]. Однако имеются сообщения о случаях ее агрессивного течения [14]. В постановке правильного диагноза первостепенное значение имеют иммуногистохимическое и молекулярно-генетическое исследования [15, 16]. Определяется положительный ответ опухоли на такие иммуногистохимические маркеры, как виментин, CD31, CD34, слабоположительный ответ на сосудистый эндотелиальный фактор роста (VEGF) [17]. Для верификации опухоли важно распознавать экспрессию сосудистых маркеров (Fli-1 и CD31), а также микроскопические признаки сосудистой дифференцировки [18]. ЭГЭ (90%) проявляют специфическую реципрокную хромосомную транслокацию t(1;3) (p36;q23-25), которая связана с синтезом белка WWTR1/CAMTA1 [19]. Однако поиск специфических диагностических критериев ЭГЭ продолжается [20].
Локализация ЭГЭ в синоназальной области крайне редка [21]. На 2017 г. в англоязычных источниках описано лишь 7 случаев данной опухоли, которая имела следующую локализацию: средняя носовая раковина и средний носовой ход в 3 случаях, перегородка носа в 1 случае, полость носа в 3 случаях [22]. Основным методом лечения, по мнению большинства авторов, является хирургический. Одни из них применяют эндоназальные эндоскопические резекции [22–25]. Другие используют как эндоназальный, так и транскраниальный подход для радикального удаления опухоли [26]. В случае невозможности удаления опухоли хирургически предлагается применение лучевых методов лечения и химиотерапии [27, 28]. В отечественной литературе данных о лечении ЭГЭ данной локализации мы не нашли, хотя сообщения об эндоскопических подходах к удалению обширных опухолей околоносовых пазух, вызывающих костную деструкцию, имеются [29, 30]. Таким образом, выбранная нами тактика соответствует имеющимся на настоящий момент представлениям о лечении и диагностике ЭГЭ синоназальной локализации.
Заключение
Интерес представленного клинического случая заключается в тщательном анализе результатов диагностических исследований и успешном эндоскопическом эндоназальном удалении обширной ЭГЭ синоназальной локализации, сопровождающейся очагами костной деструкции и проникновением в орбиту. Особенностями операции явилось использование на дооперационном этапе эндоваскулярной эмболизации сосудистой сети опухоли, а во время операции – лазерного оборудования и навигационной техники. ЭГЭ является редкой опухолью полости носа и околоносовых пазух, для дифференциальной диагностики которой обязательно необходимо использовать иммуногистохимический и молекулярно-генетический методы исследования.
ЛИТЕРАТУРA/REFERENCS
- Weiss S.W., Enzinger F.M. Epithelioid hemangioendothelioma: a vascular tumor often mistaken for a carcinoma. Cancer. 1982;50(Suppl. 5):970–81.
- Humphrey Peter A., Dehner Louis P., Pfeifer John D. The Washington Manual of Surgical Pathology (2nd ed.). Lippincott Williams & Wilkins; 2012. 141 р. ISBN 978-1-4511-1436-2.
- Zheng J., Li P., Ma S., Geng M. Epithelioid hemangioendothelioma of the meninges mimicking metastatic carcinoma: a case report. Clin. Neuropathol. 2013;32(4):324–7. doi: 10.5414/NP300584.
- Arai J., Shimozuma Y., Otoyama Y., et al. Three cases of histologically proven hepatic epithelioid hemangioendothelioma evaluated using a second-generation microbubble contrast medium in ultrasonography: case reports. BMC. Gastroenterol. 2019;19(1):187. doi: 10.1186/s12876-019-1113-y.
- Xian J., Righi A., Vanel D., et al. Epithelioid hemangioma of bone: A unique case with multifocal metachronous bone lesions. J. Clin. Orthop. Trauma. 2019;10(6):1068–72. doi: 10.1016/j.jcot.2019.03.009.
- Gong Q.X., Fan Q.H., Ding Y., et al. Atypical epithelioid hemangioendothelioma: a clinicopathological analysis of eight cases Zhonghua Bing Li Xue Za Zhi. 2019;48(8):620–5. doi: 10.3760/cma.j.issn.0529-5807.2019.08.007.
- Zhou X., Li P., Gu X., et al. A case report of right atrial epithelioid hemangioendothelioma with multiple pulmonary metastases. Clin. Respir. J. 2020;14(2):173–8. doi: 10.1111/crj.13121.
- Zeng Y., Leng X., Chen P., et al. Imaging diagnosis of epithelioid hemangioendothelioma in thoracic vertebrae and liver. Ann. Thorac. Surg. 2019. pii: S0003-4975(19)31822-3. doi: 10.1016/j.athoracsur.2019.10.034.
- Flucke U., Vogels R.J., de Saint Aubain Somerhausen N., et al. Epithelioid Hemangioendothelioma: clinicopathologic, immunhistochemical, and molecular genetic analysis of 39 cases. Diagn. Pathol. 2014;9:131. doi: 10.1186/1746- 1596-9-131.
- Murali R., Zarka M.A., Tazelaar H.D., et al. Cytologic features of epithelioid hemangioendothelioma. Am. J. Clin. Pathol 2011;136(5):739–46. doi: 10.1309/ AJCP5NK0FJCGHTFM.
- Bahrami A., Allen T.C., Cagle P.T. Pulmonary epithelioid hemangioendothelioma mimicking mesothelioma. Pathol. Int. 2008;58(11):730–34. doi: 10.1111/j.1440- 1827.2008.02301.x.
- Hart J., Mandavilli S. Epithelioid angiosarcoma: a brief diagnostic review and differential diagnosis. Arch. Pathol. Lab. Med. 2011;135(2):268–72. doi: 10.1043/1543-2165-135.2.268.
- Naqvi J., Ordonez N.G., Luna M.A., et al. Epithelioid hemangioendothelioma of the head and neck: role of podoplanin in the differential diagnosis. Head Neck Pathol. 2008;2(1):25–30. doi: 10.1007/s12105-007- 0035-0.
- Lytle M., Bali S.D., Galili Y., et al. Epithelioid Hemangioendothelioma: A Rare Case of an Aggressive Vascular Malignancy. Am. J. Case Rep. 2019;20:864–7. doi: 10.12659/AJCR.915874.
- Rosenberg A., Agulnik M. Epithelioid Hemangioendothelioma: Update on Diagnosis and Treatment. Curr. Treat. Options Oncol. 2018;19(4):19. doi: 10.1007/s11864-018-0536-y.
- Duzer S., Akyigit A., Arslan Solmaz O., et al. An Epithelioid Hemangioendothelioma of the Head and Neck. J. Craniofac. Surg. 2017;28(7):e638–40. doi: 10.1097/SCS.0000000000003749.
- Patnayak R., Jena A., Reddy M.K., et al. Epithelioid hemangioendothelioma of nasal cavity. J. Lab. Physicians. 2010;2(2):111–3. doi: 10.4103/0974- 2727.72214.
- Sardaro A., Bardoscia L., Petruzzelli M.F., et al. Epithelioid hemangioendothelioma: an overview and update on a rare vascular tumor. Oncol. Rev. 2014;8(2):259. doi: 10.4081/oncol.2014.259.
- Cousin S., Le Loarer F., Crombé A., et al. Epithelioid hemangioendothelioma. Bull Cancer. 2019;106(1):73–83. doi: 10.1016/j.bulcan.2018.11.004.
- Wiwanitkit V. CAMTA1 immunostaining is not useful in differentiating epithelioid hemangioendothelioma from its potential mimickers. Turk. Patol. Derg. 2015;31(1):80. doi: 10.5146/tjpath.2014.01287.
- Wong H.T., Mun K.S., Zulkiflee A.B., et al. Malignant epithelioid haemangioendothelioma of the maxillary sinus. Pathology. 2016;48(1):95–6. doi: 10.1016/j.pathol.2015.11.022.
- Navalón-Ramon E., Pérez-Garrigues T., Meseguer-Garcia P., et al. Epithelioid haemangioendothelioma of the nasal cavity in a woman. Acta Otorrinolaringol. Esp. 2017;68(6):369–71. doi: 10.1016/j.otorri.2016.10.003.
- Avadhani V., Loftus P.A., Meltzer D., et al. Epithelioid Hemangioendothelioma of the Maxillary Sinus. Head Neck Pathol. 2016;10(2):229–32. doi: 10.1007/ s12105-015-0633-1.
- Hanege F.M., Uzun L., Yavuz C., et al. Epithelioid hemangioendothelioma of the nasal septum. B-ENT. 2016;12(2):155–7.
- Tseng C.C., Tsay S.H., Tsai T.L., et al. Epithelioid hemangioendothelioma of the nasal cavity. J. Chin. Med. Assoc. 2005;68(1):45–8.
- Ogita S., Endo T., Nomura K., et al. Nasal cavity epithelioid hemangioendothelioma invading the anterior skull base. Surg. Neurol. Int. 2016;7:53. doi: 10.4103/2152-7806.181902.
- Chaouki A., Mkhatri A., Ballage A., et al. Extensive epithelioid hemangioendothelioma of the maxillary sinus: A case report. Int. J. Surg. Case Rep. 2019;58:70–3. doi: 10.1016/j.ijscr.2019.04.013.
- Batista K.P., Gómez G.L., Quintana E.M., et al. Giant cranionasal epithelioid haemangioendothelioma with invasive growth pattern mimicking a skull base chondrosarcoma. Contemp. Oncol. (Pozn). 2018;22(2):118–23. doi: 10.5114/ wo.2018.76235.
- ГайдуковС.С., БалакинаЛ.В., НауменкоА.Н. Особенностиэндоскопического удаления гигантских остеом околоносовых пазух, сопровождающихся деструкцией костных структур переднего отдела основания черепа. Рос. оториноларингология. 2015;3(76):27–31. [Gaidukov S.S., Balakina L.V., Naumenko A.N. Features of endoscopic removal of giant osteomas of the paranasal sinuses, accompanied by destruction of the bone structures of the anterior section of the base of the skull. Ros. otorinolaringologiya. 2015;3(76):27–31. (In Russ.)].
- Авербух В.М., Бебчук Г.Б., Джафарова М.З. Альтернативные доступы к верхнечелюстной пазухе. Головаи шея. 2016;4:47. [Averbukh V.M., Bebchuk G.B., Dzhafarova M.Z. Alternative accesses to the maxillary sinus. Golova i sheya. 2016; 4: 47.. (In Russ.)].
Поступила 22.01.20 Принята в печать 25.03.20 Received 22.01.20 Accepted 25.03.20
Вклад авторов: В.В. Дворянчиков – концепция и дизайн исследования, оценка результатов исследования. М.С. Кузнецов – анализ полученных данных, оценка результатов исследования, написание текста рукописи. А.В. Воронов, П.В. Киреев – обзор публикаций по теме статьи, сбор данных. А.В. Савелло, В.Р. Гофман – редактирование текста рукописи.
Contribution of the authors: V.V. Dvoryanchikov – concept and design of the study, evaluation of the results of the study. M.S. Kuznetsov – analysis of the data obtained, evaluation of the results of the study, writing the text of the manuscript. A.V. Voronov, P.V. Kireev – review of publications on the topic of the article, data collection. A.V. Savello, V.R. Gofman — manuscript text editing
Информация об авторах:
М.С. Кузнецов – к.м.н., преподаватель кафедры оториноларингологии ФГБВОУВО Военно-медицинская академия им. С.М. Кирова МО РФ, Санкт-Петербург, Россия; e-mail:mskuznecov2@mail.ru; ORCID: orcid http:// orcid.org/0000-0002-5057-3486
А.В. Воронов – к.м.н., начальник хирургического отделения клиники оториноларингологии ФГБВОУВО Военно-медицинская академия им. С.М. Кирова МО РФ, Санкт-Петербург, Россия; e-mail: voronovdoc@mail.ru; ORCID: orcid http://orcid.org/0000-0003-4030-8571
А.В. Савелло – д.м.н., профессор, заместитель начальника кафедры нейрохирургии ФГБВОУВО Военно-медицинская академия им. С.М. Кирова МО РФ, Санкт-Петербург, Россия; e-mail: alexader.savelnlo@gmail.ru; ORCID: orcid http://orcid.org/0000-0002-1680-6119
В.В. Дворянчиков – д.м.н., профессор, заслуженный врач РФ, начальник кафедры оториноларингологии кафедры оториноларингологии ФГБВОУВО Военно-медицинская академия им. С.М. Кирова МО РФ, Санкт-Петербург, Россия; e-mail:vmedalor@mail.ru; ORCID: http://orcid.org/0000-0002-0925- 7596
В.Р. Гофман – д.м.н. профессор кафедры оториноларингологии ФГБВОУВО Военно-медицинская академия им. С.М. Кирова МО РФ, Санкт-Петербург, Россия; ORCID: http://orcid.org/0000-0002-3111-2887
П.В. Киреев – врач-отоларинголог клиники оториноларингологии ФГБВОУВО Военно-медицинская академия им. С.М. Кирова МО РФ, Санкт-Петербург, Россия; e-mail: pkireev@mail.ru; ORCID: http://orcid. org/0000-0001-9575-745Х
Information about the authors
M.S. Kuznetsov – PhD, lecturer of the Department of Otorhinolaryngology, FSBMEI HE Military Medical Academy n.a. S.M. Kirov of the Ministry of Defense of Russian Federation, St. Petersburg, Russia; e-mail: mskuznecov2@mail.ru; ORCID: orcid http://orcid.org/0000-0002-5057-3486
A.V. Voronov – PhD, head of the surgical department of the clinic of otorhinolaryngology FSBMEI HE Military Medical Academy n.a. S.M. Kirov of the Ministry of Defense of Russian Federation, St. Petersburg, Russia; e-mail: voronovdoc@mail.ru; ORCID: orcid http://orcid.org/0000-0003-4030-8571
A.V. Savello – Doctor of Medicine, professor, deputy head of the Department of Neurosurgery, FSBMEI HE Military Medical Academy n.a. S.M. Kirov of the Ministry of Defense of Russian Federation, St. Petersburg, Russia; e-mail: alexader.savelnlo@gmail.ru; ORCID: orcid http://orcid.org/0000-0002-1680- 6119
V.V. Dvoryanchikov – Doctor of Medicine, professor, Honored Doctor of the Russian Federation, Head of the Department of Otorhinolaryngology, FSBMEI HE Military Medical Academy n.a. S.M. Kirov of the Ministry of Defense of Russian Federation, St. Petersburg, Russia; e-mail: vmedalor@mail.ru; ORCID: http:// orcid.org/0000-0002-0925-7596
V.R. Gofmann – Doctor of Medicine, Professor of the Department of Otorhinolaryngology FSBMEI HE Military Medical Academy n.a. S.M. Kirov of the Ministry of Defense of Russian Federation, St. Petersburg, Russia; ORCID: http://orcid.org/0000-0002-3111-2887
P.V. Kireev – MD, otolaryngologist of the clinic of otorhinolaryngology FSBMEI HE Military Medical Academy n.a. S.M. Kirov of the Ministry of Defense of Russian Federation, St. Petersburg, Russia; e-mail: pkireev@mail.ru; ORCID: http://orcid.org/0000-0001-9575-745X