Для цитирования:
Диаб Х.М., Дайхес Н.А., Каибов А.А., Пащинина О.А., Араби А. Хирургическое лечение пациентов с отосклерозом с IV степенью тугоухости и глухотой. Голова и шея. Российский журнал = Head and neck. Russian Journal. 2020;8(3):35–43
Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
Doi: 10.25792/HN.2020.8.3.35–43
Актуальность. На сегодняшний день актуальной проблемой остается лечение отосклероза с тяжелой потерей слуха и глухотой. Отосклероз – наследственное заболевание с двусторонним поражением костной капсулы ушного лабиринта, что может вызвать тугоухость. Прогрессирующее течение отосклеротического процесса костной капсулы лабиринта может привести к двусторонней смешанной или глубокой СНТ вплоть до полной потери слуха, шуму в ушах, вестибулярным нарушениям. Как в мировой литературе, так и в нашей стране нет определенной тактики ведения лечения пациентов с отосклерозом с IV степенью тугоухости и глухотой. Кохлеарная имплантация (КИ) является эффективным методом реабилитации пациентов с IV степенью тугоухости и глухотой. Однако, по данным разных авторов, отмечают частые осложнения при отосклерозе как во время операции, так и на этапе реабилитации слуха.
Материал и методы. На базе ФМБА НКЦО ФМБА России в период с 2016 по 2019 г. была выполнена КИ 60 пациентам. Все пациенты были разделены на 2 группы – основная, 30 больных отосклерозом с IV степенью тугоухости и глухотой; контрольная – 30 пациентов с другими этиологиями (травма и менингит). Пациенты основной группы были подразделены на две подгруппы: I-A – перенесшие ранее стапедопластику –12 пациентов; I-Б – без хирургических вмешательств в анамнезе (без стапедопластики) – 18 пациентов. В I-Б группе у пациентов были сохранены структуры среднего уха (стремя, стременная мышца, подножная пластика), но при этом имелся анкилоз стремени. В связи с этим был предложен метод регистрации стапедиальных рефлексов при анкилозе стремени у пациентов с отосклерозом.
Результаты. По данным проведения регистрации тональных сигналов в свободном звуковом поле пороги слуха стабилизировались уже к 6-му месяцу использования речевого процессора в обеих группах и не имели существенных изменений на протяжении 2 лет эксплуатации речевого процессора.
Заключение. Несмотря на наличие существенных изменений структур внутреннего уха при отосклерозе, КИ обеспечивает хорошие результаты реабилитации пациентов.
Ключевые слова: отосклероз, сенсоневральная тугоухость, глухота, кохлеарная имплантация, реабилитация слуха
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Работа выполнена без спонсорской поддержки
Background. Today, treatment of otosclerosis with severe hearing loss and deafness remains an urgent problem. Otosclerosis is a hereditary disease with a bilateral involvement of the bone capsule of the ear labyrinth, which can cause hearing loss. The progressive otosclerotic process in the labyrinth bone capsule can lead to a bilateral mixed or deep SNHL up to complete hearing loss, tinnitus, vestibular disorders. No specific treatment exists for patients with otosclerosis with grade IV hearing loss and deafness, either in the world literature data or in our country. Cochlear implantation (CI) is an effective method of rehabilitation for patients with grade IV hearing loss and deafness. However, according to various authors, the complications of otosclerosis develop frequently both during surgery and at the stage of hearing rehabilitation.
Material and methods. CI was performed in 60 patients of the FSBI SCCO FMBA of Russia in the period from
2016 to 2019. All patients were divided into 2 groups – the main group, patients with otosclerosis (n=30) with IV degree of hearing loss and deafness; the second group — the control group, patients (n=30) with other etiologies (trauma and meningitis). Patients of the main group (with otosclerosis) were subdivided into two subgroups: I-A – who had previously undergone stapedoplasty (12 patients); I-B – no history of surgery (no stapedoplasty) – 18 patients. In group I-B, the patients had preserved structures of the middle ear (stirrup, stapedius muscle, footplate), but the ankylosis of the stirrup at the same time. In this regard, a method was proposed for registering stapedial reflexes in stapes ankylosis in patients with otosclerosis.
Results. According to the data of the tonal signals registration in the free sound field, the hearing thresholds stabilized by the 6th month of using the speech processor in both groups and did not have significant changes in dynamics when observing the patients for 2 years of the speech processor usage.
Conclusion. Despite the significant changes in the inner ear structures, CI provides good results in patients’ rehabilitation according to CT of the temporal bones in otosclerosis.
Key words: otosclerosis, sensorineural hearing loss, deafness, cochlear implantation, hearing rehabilitation
Conflicts of interest. The authors have no conflicts of interest to declare.
Funding. There was no funding for this study.
Актуальность
Отосклероз – специфическое заболевание, представляющее собой первичное метаболическое двустороннее очаговое остеодистрофическое поражение костной капсулы ушного лабиринта, что приводит к прогрессирующему снижению слуха, вплоть до глухоты. Этиология и патогенез данного заболевания до сих пор не установлены.
В клинической практике оториноларингологии для определения формы отосклероза используют классификацию Н.А. Преображенского (1962) [1]. На основании данных тональной пороговой аудиометрии (ТПА) отосклероз подразделяет на тимпанальную, смешанную и кохлеарную формы. В.С. Корвяков и соавт. (2017) [2] для уточнения нарушений звукопроведения и/или звуковосприятия у больных отосклерозом по данным ТПА, а также из соображений преимущественной локализации патологического процесса на основании компьютерной томографии (КТ) височных костей предложили внести некоторые коррективы в терминологию и классификацию данного заболевания. 1) Фенестральная форма отосклероза – патологическому остеодистрофическому процессу подвержена ниша окна преддверия (анкилоз стремени), поэтому у этих пациентов нарушено только внутритимпанальное звукопроведение за счет неподвижности стремени (во всех случаях характеризуется кондуктивной тугоухостью по данным ТПА).
-
Фенестрально-кохлеарная форма отосклероза – патологическому остеодистрофическому процессу подвержены все отделы костной капсулы лабиринта, в т.ч. и ниша окна преддверия (анкилоз стремени). По данным ТПА, у этих пациентов отмечается смешанная форма тугоухости, причем костно-воздушный интервал (КВИ) во всех случаях обусловлен нарушением внутритимпанального звукопроведения, т.е. является истинным, а у части больных имеет сочетанный характер, когда к внутритимпанальным присоединяются нарушения, связанные с внутрилабиринтным звукопроведением (который автор называет – «ложный» КВИ).
-
При истинной кохлеарной форме отосклероза звукопроведение на уровне среднего уха не страдает, т.к. отсутствует анкилоз стремени. Нарушено только внутрилабиринтное звуковосприятие, т.е. у этих пациентов, по данным ТПА, отмечается сенсоневральная тугоухость (CНТ) в «чистом» виде без КВИ либо смешанная с небольшим КВИ, который является «ложным», т.к. обусловлен изменениями внутрилабиринтного звукопроведения. Следует заметить, что «ложный» КВИ при кохлеарной форме отосклероза отмечается только в случаях нарушения гидродинамики внутреннего уха, а потому не является постоянным [2].
Кохлеарная форма отосклероза впервые была описана H.P. House, J.L. Sheehy (1961). При ней отмечается воздушная проводимость порогов более 85 дБ и неопределенный порог костной проводимости (из-за ограничения возможностей аудиометров) [3].
Прогрессирующее течение отосклеротического процесса костной капсулы лабиринта может привести к двусторонней смешанной или глубокой СНТ вплоть до полной потери слуха, шуму в ушах, вестибулярным нарушениям (W. Arnold, 1999) [3]. Расположение деминерализованных очагов при отосклерозе можно встретить в разных отделах внутреннего уха: в улитке, полукружных каналах, внутреннем слуховом проходе и водопроводе преддверия, что в последующем вызывает тугоухость медленно или быстро прогрессирующего характера с сенсоневральным компонентом. Отосклеротические изменения полукружных каналов, как считается, возможно, являются причиной вестибулярных симптомов, что может быть связано с изменениями биохимического состава перилимфы [4]. Многие авторы указывают на изменения, наблюдаемые у пациентов с кохлеарной формой отосклероза: перикохлеарное расположение очагов, утолщение или истончение костной капсулы за счет деминерализации; сужение просвета улитки из-за единичных или множественных отосклеротических очагов или диффузное поражение [3, 4].
Диагностика и хирургическое лечение отосклероза с IV степенью тугоухости и глухотой остаются актуальной проблемой современной оториноларингологии. На сегодняшний день КТ височных костей высокого разрешения является высокоинформативным объективным методом диагностики отосклероза. Данный метод позволяет проводить точную визуализацию анатомических структур височных костей, выявлять локализацию, распространенность очагов отосклероза и определять степень активности процесса [5, 6], также дает возможность определять в области поражения очаги как пониженной, так и повышенной плотности при отосклерозе (в норме плотность костной ткани улитки составляет от +2000 до +2200 ед. HU), расположенные в области окна преддверия, окна улитки и/ или вокруг улитки (двойное кольцо улитки) [1]. КТ-сканирование височной кости играет значительную роль в предоперационной оценке пациентов с отосклерозом, которым планируется кохлеарная имплантация (КИ) [7]. По данным различных авторов, чувствительность КТ височных костей составляет 80–95%, специфичность – 99,1% [8]. За последние годы в практике оториноларингологии часто начали использовать конусно-лучевую КТ (КЛКТ).
КЛКТ височных костей – инновационная технология, в основе которой лежит применение тонкого прерывистого конического пучка рентгеновского излучения, что позволяет за один оборот вращения отсканировать определенный анатомический объем. Принципиальное отличие КЛКТ от МСКТ заключается в форме рентгеновского луча, также КЛКТ имеет свои преимущества в виде низкой лучевой нагрузки, меньшей стоимости исследования. При этом диагностическая чувствительность КЛКТ составляет 100%, а специфичность – 81% [9, 10].
Также важную информацию дает магнитно-резонансная томография (МРТ) височных костей, в особенности при распространении процесса в просвет лабиринта о состоянии жидкостных сред внутреннего уха, нервов внутреннего слухового прохода, для исключения сопутствующей ретрокохлеарной патологии и изменениях головного мозга [11].
КИ является эффективным методом слухоречевой реабилитации у больных отосклерозом с IV степенью тугоухости и глухотой. КИ зарекомендовала себя как «хороший» вариант восстановления слуха у пациентов с кохлеарной формой отосклероза [12]. При этом некоторые авторы сообщают о неудовлетворительных результатах реабилитации пациентов с кохлеарной формой отосклероза после КИ, наблюдаемых вследствие затруднения введения электрода и других осложнений, связанных с изменениями улитки, на которых мы подробно остановимся ниже [13].
В литературе приведены данные о различной степени выявления интраоперационной оссификации улитки при отосклерозе (от 5 до 51%), которые требуют наложения дополнительной стомы улитки [14]. Из-за отосклеротических изменений улитки часто полное введение электродной решетки затруднено и может требовать специального хирургического подхода. M. Sanna и другие авторы отметили трудность введения электрода или даже неправильную установку его через ложное деминерализованное кольцо кохлеарной оссификации [15].
При гистопатологическом исследовании M. Li и соавт. (2011) проанализировали особенности строения улитки в случаях неполного введения электрода; найдено окостенение, суживающее просвет улитки за счет отосклеротических очагов. Помимо этого, авторы отметили, что статистически значимым признаком, приводящим к неполному введению, является переход электрода в лестницу преддверия к боковой стенке улитки с повреждением спиральной связки, таким образом, неполная вставка зависит от числа электродов, которые перешли из одной лестницы в другую [16]. Введение электрода в вестибулярную лестницу было предложено использовать как дополнительный вариант в случаях полного сужения или окостенения барабанной лестницы без неблагоприятных последствий. Введение электрода может оказаться проблематичным из-за кохлеарного окостенения, сужения улитковых каналов (истончаясь, в стенке улитки может образоваться дефект – «третье окно», что повышает риск попадания электрода за пределы улитки). Такие случаи могут привести к серьезным осложнениям [7].
При выполнении КИ при отосклерозое трудности возникают как на хирургическом этапе, так и на этапе реабилитации (A.H. Marshall, 2005). При подключении процессора через 4–6 недель после КИ у части пациентов возникает проблема – патологическая стимуляция лицевого нерва, помимо этого ухудшение результатов реабилитации связано с шумом и повышенным дискомфортом [17]. Известно, что при отосклерозе значительно чаще встречается патологическая стимуляция лицевого нерва после КИ (с частотой до 75%) [18]. А.H. Marshall и соавт. (2005) наблюдали после КИ у 17% пациентов с отосклерозом СНТ глубокой степени стимуляцию лицевого нерва по сравнению с контрольной группой [7]. Снижение стимуляции слухового нерва может оказать негативное влияние на результаты речевой дискриминации, по крайней мере, на непрерывное чередование разности восприятия речевых стимулов. Усиление силы стимулов для улучшения речевого восприятия может привести к патологической стимуляции слухового нерва, дискомфорту и усилению шума в ушах, что требует выключения электродов на уровне патологической стимуляции. При постоянной и выраженной стимуляции лицевого нерва кохлеарный имплантат практически бесполезен, что приводит к эксплантации или реимплантации [19]. Потенциальная причина стимуляции лицевого нерва, проявляющаяся у одних пациентов и отсутствующая у других при отосклерозе, остается не до конца выясненной.
При выполнении КИ также остается открытым вопрос выбора метода интраоперационной регистрации стапедиального рефлекса у больных отосклерозом с IV степенью тугоухости и глухотой.
Цель исследования: повышение эффективности слухоречевой реабилитации пациентов с отосклерозом с IV степенью тугоухости и глухотой.
Материал и методы
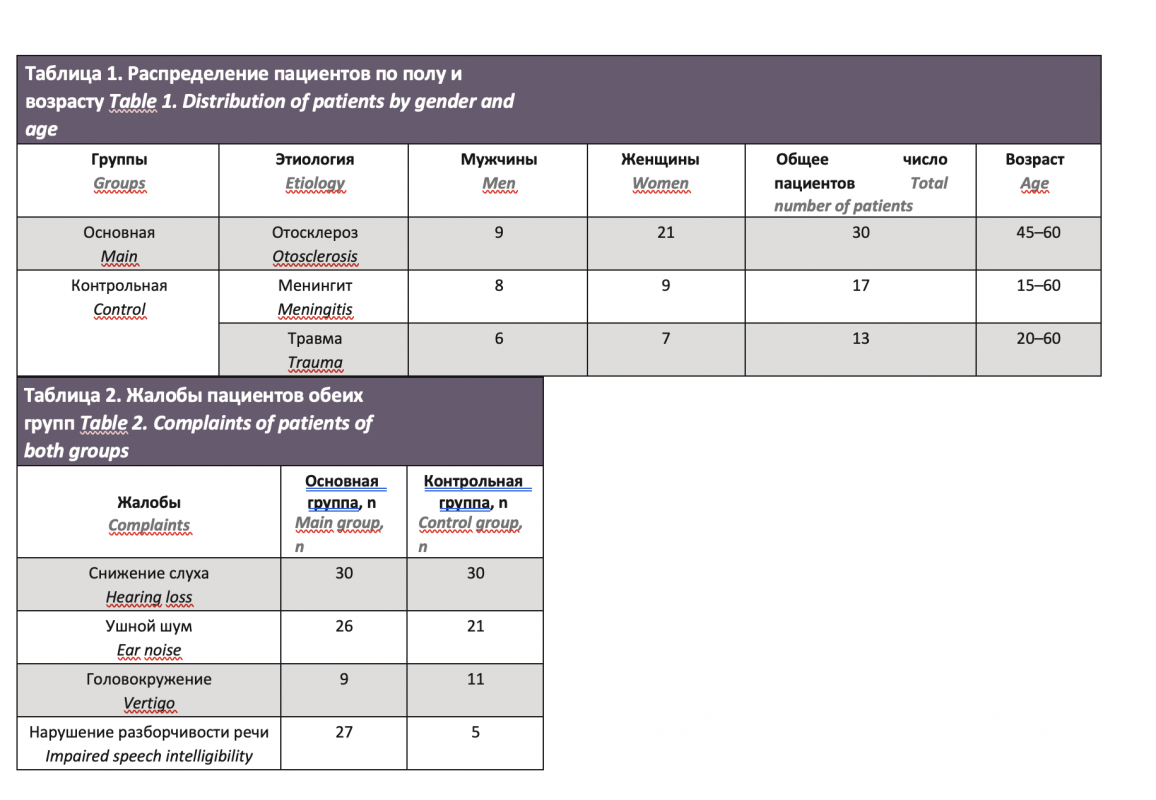
В соответствии с целью исследования были сформированы две группы пациентов, которым выполнена КИ на базе ФМБА НКЦО ФМБА России в период с 2016 по 2019 г.: первая группа – основная, больные отосклерозом (n=30) с IV степенью тугоухости и глухотой; 2) вторая группа
– контр ольная, пациенты (n=30) с другими этиологиями (табл. 1).
Пациенты основной группы были подразделены на следующие две подгруппы:
I-A – перенесшие ранее стапедопластику – 12 пациентов;
I-Б – без хирургических вмешательств в анамнезе (без стапедопластики) – 18 пациентов.
Жалобы пациентов при поступлении в основной и контрольной группах отмечены в табл. 2.
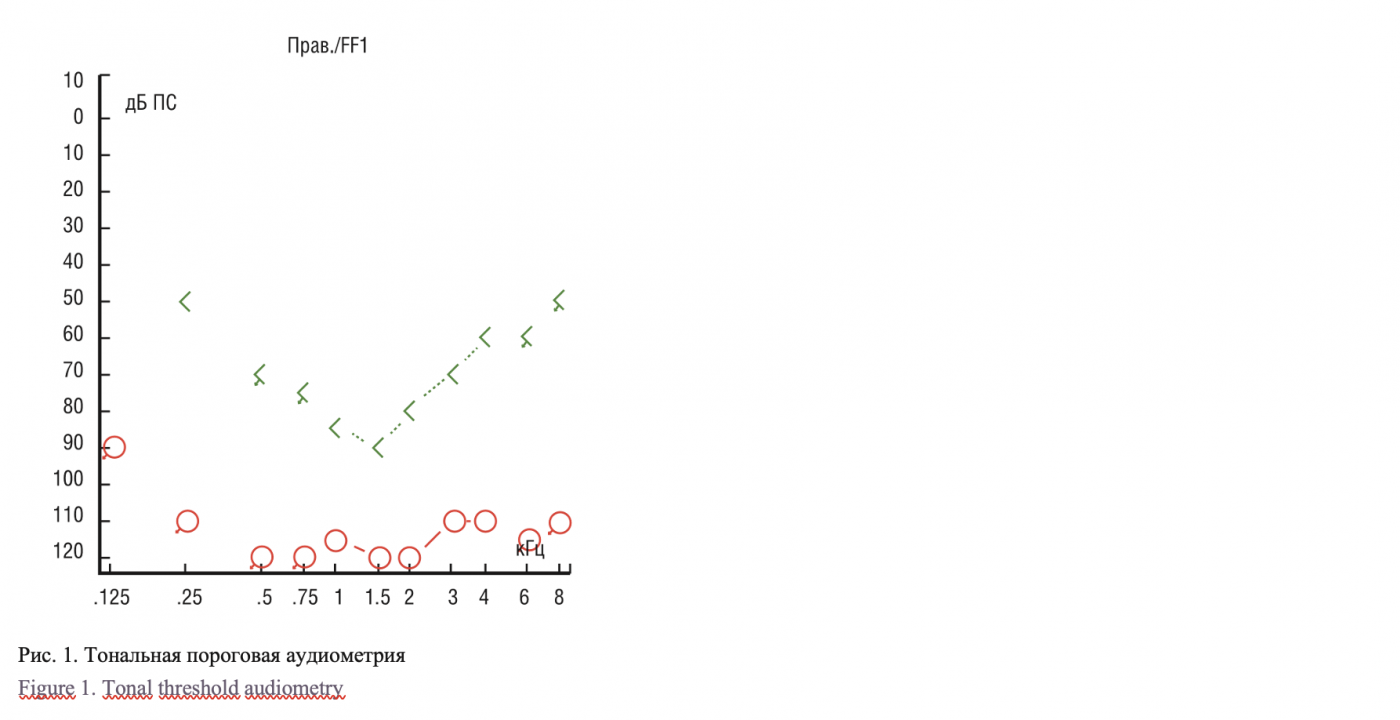
Диагностический этап для обеих групп включал в себя следующие исследования: лучевые методы диагностики (КТ височных костей, МРТ височных костей, головного мозга), аудиологическое обследование (акуметрия, тональная пороговая аудиометрия – рис. 1, акустическая импедансометрия, аудиометрия в расширенном звуковом диапазоне, регистрация коротколатентных слуховых вызванных потенциалов, регистрация задерженной вызванной отоакустической эмиссии, ASSR-тест, тональная пороговая аудиометрия в свободном звуковом поле, речевая аудиометрия в свободном звуковом поле), вестибулологическое обследование (вращательный тест, калорический тест, вестибулометрия – спонтанный нистагм, тест встряхивания головы, тест поворота головы, шаговые пробы), заключение сурдолога (рис. 2) и электроэнцефалография с заключением невролога.
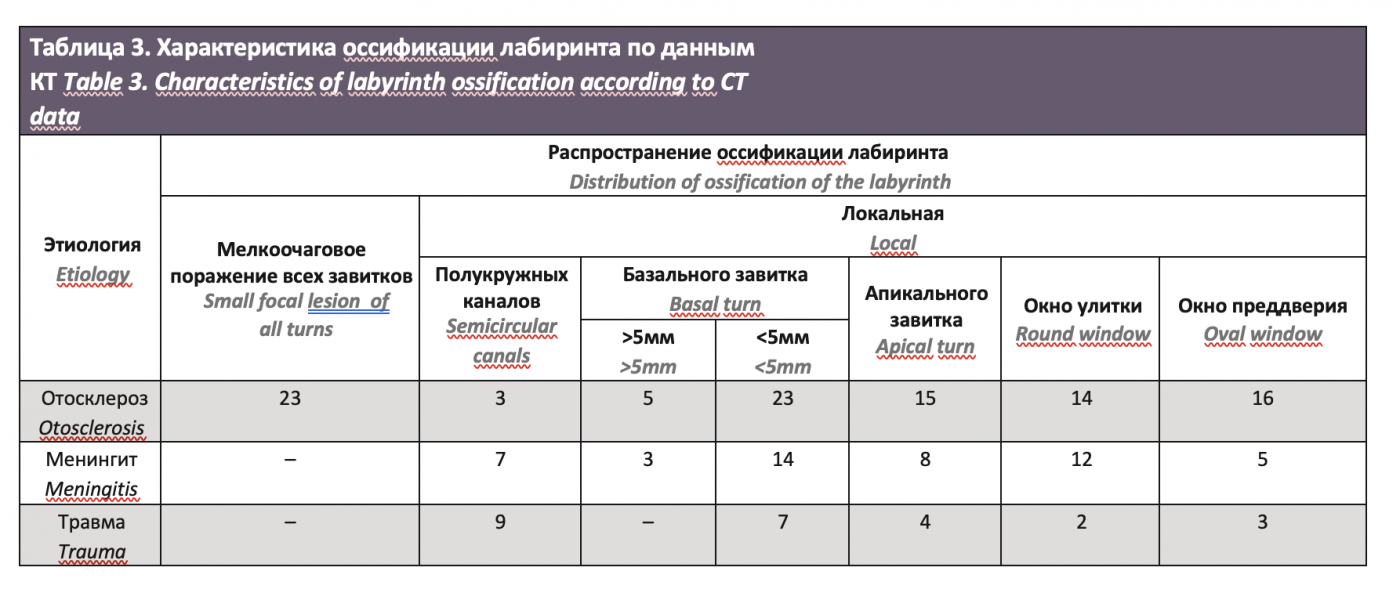
Предоперационные данные КТ височных костей в зависимости от распространения оссификации в основной и контрольной группах представлены в табл. 3.
По данным КТ и МРТ височных костей определяли степень оссификации улитки, вовлеченность в процесс структур среднего и внутреннего уха (рис. 3–8), некоторые данные предоперационных обследований представлены в табл. 4.
При оперативном вмешательстве КИ применяли эндотрахеальный наркоз в основной группе 26 пациентам, в контрольной группе 22 пациентам, местную анестезию в основной группе – 4 пациентам, в контрольной группе – 8 пациентам. Методика выполнения хирургического этапа КИ в I-А и контрольной группах не отличалась.
Операция КИ выполнялась по классической методике, включающей следующие этапы: заушный С-образный разрез, подготовка ложа для имплантата, антромастоидотомия, задняя тимпанотомия, введение активного электрода производили через окно улитки в случаях отсутствия или незначительной оссификации. При наличии оссификации в области окна улитки на протяжении 2–3 мм и по ходу базального завитка расширяли окно улитки и удаляли оссифицированные участки по ходу основного завитка до появления просвета тимпанальной лестницы. После введения электродов производили тщательную тампонаду кохлеостомы фрагментом аутомышцы.
В I-Б группе у пациентов были сохранены структуры среднего уха (стремя), но при этом имелся анкилоз стремени. Предложен метод регистрации стапедиальных рефлексов при анкилозе стремени у пациентов с отосклерозом: заушный разрез, обнажение площадки сосцевидного отростка в пределах треугольника Шипо, надкостницу с мягкими тканями отсепаровывали от костей черепа в заушной области с формированием ложа для имплантата, проводили антромастоидотомию, заднюю тимпанотомию, при ревизии барабанной полости определяли состояние сухожилия стременной мышцы, выраженность пирамидального отростка. Далее алмазным бором производили сглаживание пирамидального отростка в направлении от верхушки до основания – до обнажения собственно стременной мышцы (до 4–6 мм); далее после введения электрода в улитку подавали стимулы на каждый электрод поочередно и одновременно хирург визуально наблюдал за сокращением стапедиальной мышцы с помощью микроскопа (рис. 9). При этом определяли пороги стапедиальных рефлексов, которые в последующем использовались при первичной настройке импланта. Тампонаду ниши окна улитки производили фрагментом аутомышцы и послойное ушивали рану.
Всем пациентам интраоперационно проводили: 1) измерение межэлектродного сопротивления; 2) регистрацию электрически вызванных рефлексов стременной мышцы (при ее наличии); 3) регистрацию ответа вызванного потенциала действия слухового нерва.
В ходе исследования использовали импланты с прямым или перимодиолярным типом активного электрода.
На 1-е сутки после операции выполняли для контроля положения электрода КТ височных костей или КЛКТ. Через 4–6 недель после КИ проводили подключение импланта.
Результаты и обсуждение
В ходе обследования больных отосклерозом с IV степенью тугоухости и/или глухотой были выявлены особенности: в анамнезе имелась перенесенная операция – стапедопластика, выполненная под местной анестезией у 12 пациентов. При проведении тональной пороговой аудиометрии в свободном звуковом поле в основной и контрольной группах получены следующие результаты тестирования. У пациентов основной группы результаты определения тональных сигналов были несколько хуже и пороги находились выше по сравнению с контрольной группой при проведении тестирования в оптимально подобранных слуховых аппаратах. Однако после проведения хирургического этапа КИ в обеих группах при активации речевого процессора данные пороги не имели статистически значимых различий.
При проведении речевой аудиометрии в свободном звуковом поле в слуховых аппаратах до КИ у пациентов основной группы процент разборчивости речи ни в одном из случаев не превышал 57%, а у большинства пациентов данный процент находился в пределах 42%, что свидетельствовало о низкой эффективности применения слуховых аппаратов и являлось прямым показанием для проведения КИ у больных данной категории с целью повышения разборчивости речи.
Особенности хирургического этапа и интраоперационные находки основной группы: слизистая оболочка барабанной полости была без воспалительных процессов (во всех случаях); лицевой нерв расположен в костном канале (во всех случаях); неподвижность стремени (анкилоз) отмечалась в 14 случаях; стапедиальный протез в преддверии улитки – у 12 пациентов (ранее перенесших стапедопластику), в остальных 4 случаях передача на вторичную мембрану была сохранена (стремя подвижно); вторичная мембрана утолщена, изменена. При вскрытии вторичной мембраны окна улитки (в 15 случаях) и при расширении окна улитки (в 8 случаях) отмечались отосклеротические очаги белесоватого цвета, плотные, не кровоточащие. Очаги были удалены микро-крючками, что позволило освободить окно улитки, вход в барабанную лестницу.
На этапе введения электродной решетки (прямой или перимодилярный тип электрода) в тимпанальную лестницу не наблюдалось затруднения или сопротивления, во всех случаях электроды введены полностью.
Возможные интраоперационные осложнения при проведении КИ: кровотечение, ликворея, попадание крови или костной стружки в улитку, стимуляция лицевого нерва при проверке импланта, неполное введение электрода в улитку, ошибочное введение электродной решетки за пределы улитки ни в одном из случаев не наблюдались.
Возможные послеоперационные осложнения при КИ: головокружения наблюдались в 9 случаях в основной группе, из них в 3 случаях длительностью до 6 месяцев, в 2 случаях – до 3 месяцев, в 4 случаях – от 7 до 14 дней, в контрольной группе – в 12 случаях длительностью до 3 месяцев; усиление шума (незначительное усиление шума в 2 случаях, которое сохранялось до 3 месяцев, в 1 случае – до 6 месяцев); патологическая стимуляция лицевого нерва не отмечалась ни в одном из случаев при подключении импланта и за период 3-летнего наблюдения.
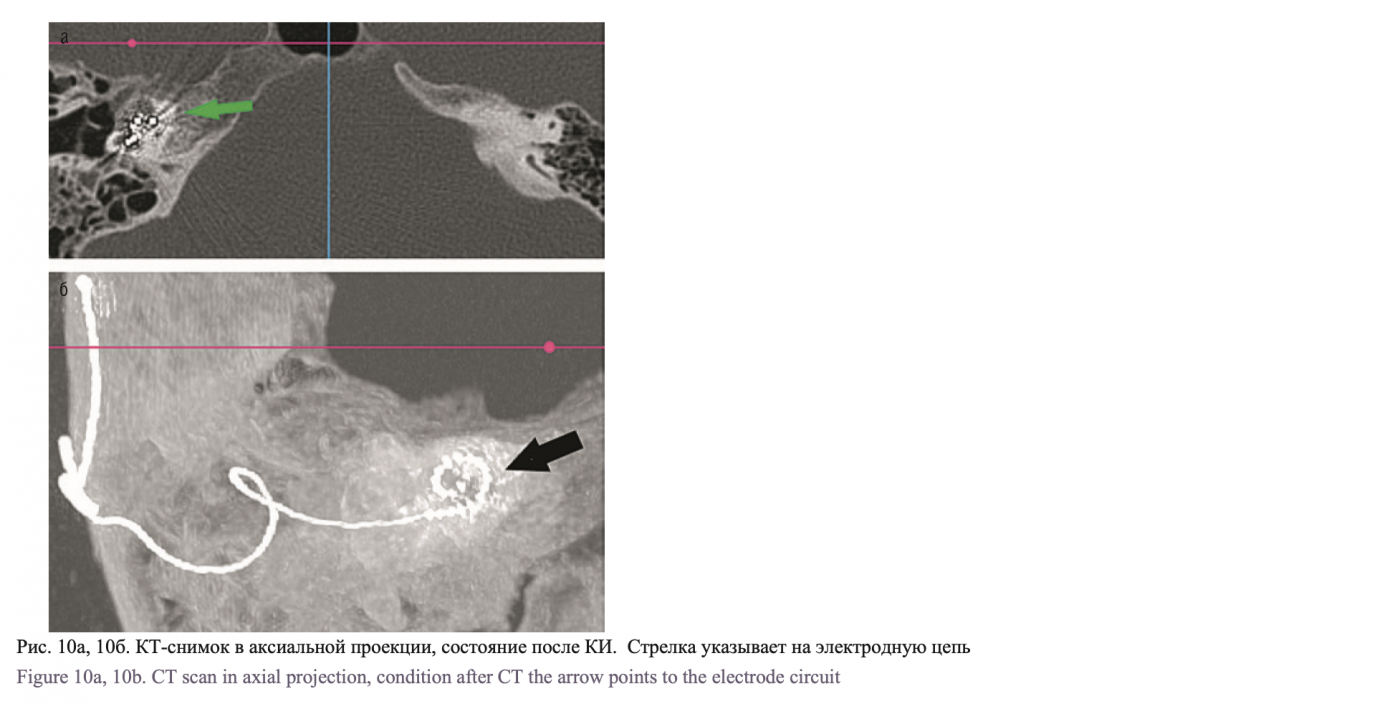
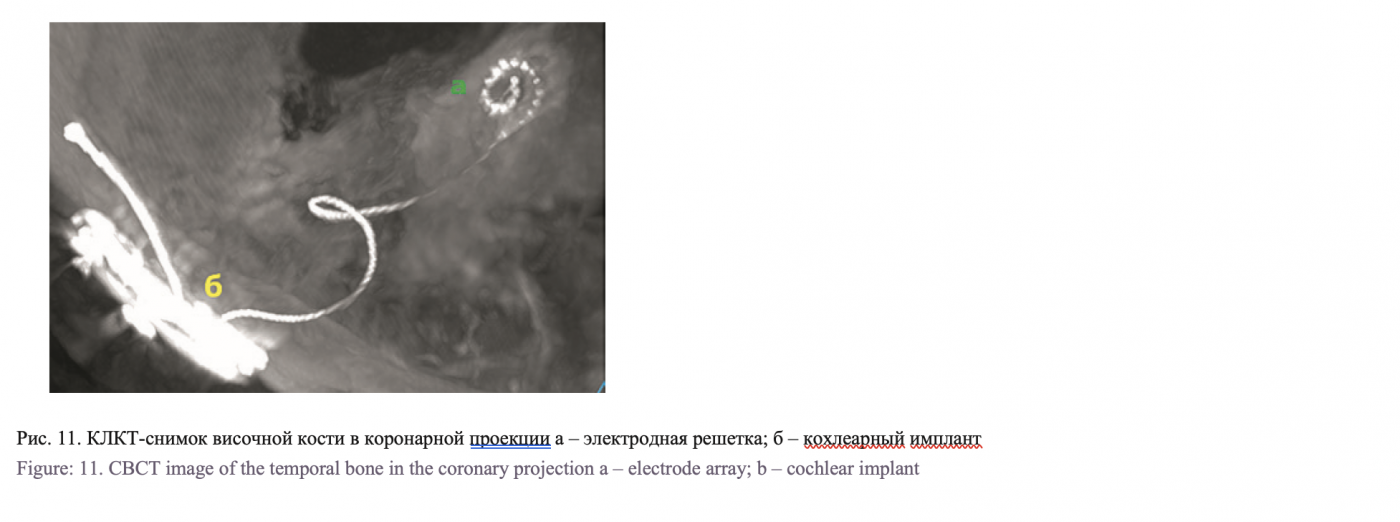
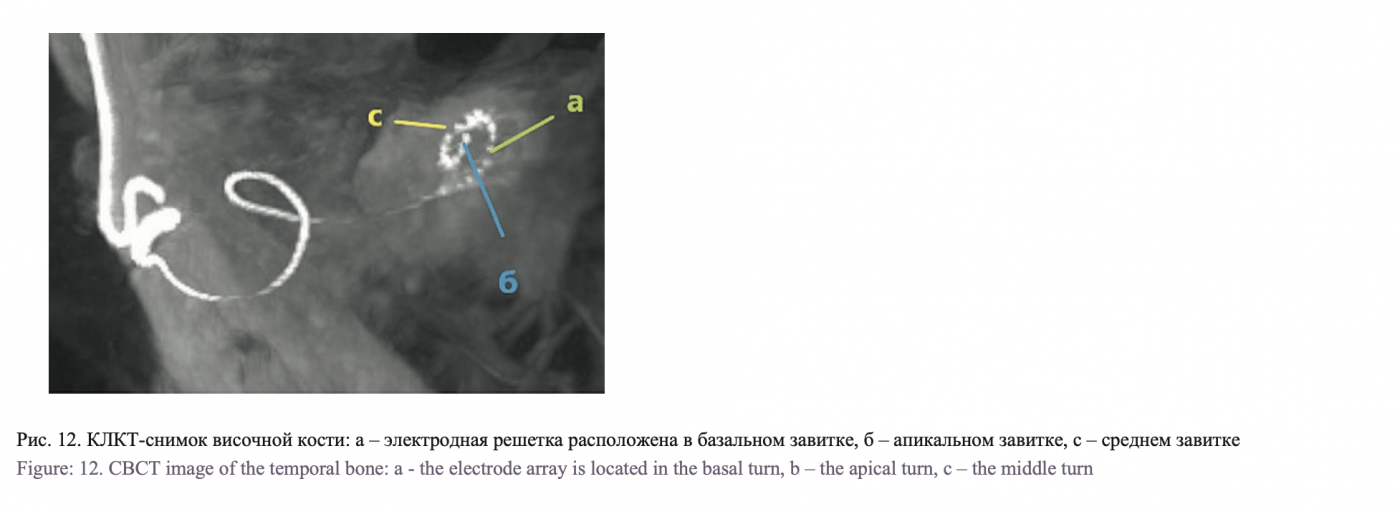
На первые сутки после КИ проведено исследование КТ или КЛКТ височных костей для контроля расположения электродной решетки в динамике (рис. 10–12).
По данным регистрации тональных сигналов в свободном звуковом поле пороги слуха стабилизировались уже к 6-му месяцу использования речевого процессора в обеих группах и не имели существенных изменений динамики при наблюдении за больными на протяжении 2 лет эксплуатации речевого процессора. Однако для большей наглядности, а также способности пациента к общению целесообразно рассмотреть разборчивость речи в свободном звуковом поле на протяжении двух лет использования речевого процессора.
Исходя из данных результатов исследования, к 6-му месяцу пользования речевым процессором достоверных различий между результатами тестирования посредством речевой аудиометрии не выявлено. Пациенты основной и контрольной групп демонстрировали разборчивость речи к 6 месяцам пользования до 80%.
Все вестибулярные нарушение исчезали к 6-му месяцу после операции, нистагм ирритации – в течение 1 месяца после операции.
Заключение
Тщательное изучение данных объективного обследования больных отосклерозом с тяжелой степенью тугоухости и глухотой с учетом всех особенностей структур улитки позволяет успешно проводить хирургический этап КИ с минимальным риском возникновения осложнений, связанных с операцией.
Несмотря на наличие существенных изменений структур внутреннего уха, по данным КТ височных костей при отосклерозе, КИ обеспечивает хорошие результаты реабилитации пациентов.
Исходя из результатов наших исследований, отмечаем, что по данным регистрации тональных сигналов в свободном звуковом поле пороги слуха стабилизировались к 6-му месяцу использования речевого процессора в основной и контрольной группах и не имели отрицательной динамики на протяжении 2 лет эксплуатации речевого процессора.
ЛИТЕРАТУРА / REFERENCES
-
Кryukov A.I., Palchun V.T., Kunelskaya N.L. Treatment and diagnostic algorithm for cochlear otosclerosis. 2010.14 p. / Крюков А.И., Пальчун В.Т., Кунельская Н.Л. Лечебно–диагностический алгоритм кохлеарной формы отосклероза. Методические рекомендации. 2010. 14 с. (In Russ.).
-
Korvyakov V.S., Diab Kh.M., Pashchinina O.A., Akhmedov Sh.M. Surgical treatment of patients with cochlear otosclerosis. Rossijskaya otorinolaringologiya. 2017; 5 (90): 35–43. / Корвяков В.С., Диаб Х.М., Пащинина О.А, Ахмедов Ш.М. Хирургическое лечение больных кохлеарной формой отосклероза. Российская оториноларингология. 2017;5(90):35–43 (In Russ.).
-
Calmels M.N., Viana C., Wanna G. Very far-advanced otosclerosis: stapedotomy or cochlear implantation. Acta Otolaryngol. 2007;127(6):574– 8. doi: 10.1080/00016480600987768.
-
Berrettini S., Burdo S., Forli F. Far advanced otosclerosis: stapes surgery or cochlear implantation. 2004;33(3):165–71.
-
Marx M., Lagleyre S., Escude B., Demeslay J., Fraysse B. Correlation between CT scan findings and hearing thresholds in otosclerosis. Acta Otolaryngol. 2011;131:351–7. doi: 10.3109/00016489.2010.549841.
-
Lee T.C., Aviv R.I., Chen J.M., Nedzelski J.M., Fox A.J., Symons S.P. CT grading of otosclerosis. AJNR Am. J. Neuroradiol. 2009;3:1435–9. Doi: https://doi.org/10.3174/ajnr.A1558.
-
Rotteveel L.J., Proops D.W., Ramsden R.T. Cochlear implantation in 53 patients with otosclerosis: demographics, computed tomographic scanning, surgery, and complication. Neurotol. 2004;25(6):943–52.
-
Astashchenko S.V., Kuzovkov V.E., Ilyin S.N., Sapogovskaya A.S., Pavlova S.S. Cochlear otosclerosis: diagnosis and tactics of surgical treatment. Medicinskoe obozrenie. 2019; 9 (II): 52–4 / Астащенко
С.В., Кузовков В.Е., Ильин С.Н., Сапоговская А.С., Павлова С.С. Кохлеарная форма отосклероза: диагностика и тактика хирургического лечения. РМЖ. Медицинское обозрение. 2019;9(II):
52–4. (In Russ.)..
-
Arweiler-Harbeck D., Mönninghoff C., Greve J., et al. Imaging of Electrode Position after Cochlear Implantation with Flat Panel CT. ISRN Otolaryngol. 2012;1–5. doi: Org/10.5402/2012/728205.
-
Pearl M.S., Roy A., Limb C.J. High-Resolution Secondary Reconstructions with the Use of Flat Panel CT in the Clinical Assessment of Patients with Cochlear Implants. J. Neuroradiol. 2013;35(6):1202–8. doi: Org/10.3174/Ajnr.A3814.
-
Purohit B., Hermans R., Op de beeck K. Imaging in otosclerosis: A pictorial review. Insights Imaging. 2014;5:245–52. doi: 10.1007/s13244-014-0313-9.
-
Diab H.M., Korvyakov V.S., Kaibov A.A. et al. Cochlear implantation in otosclerosis with grade IV hearing loss and deafness (literature review). Rossiyskaya otorinolaringologiya. 2019; 5 (102): 74–81. doi: 10.18692/1810-4800-2019-574-81 / Диаб Х.М., Корвяков В.С., Каибов А.А. и др. Кохлеарная имплантация при отосклерозе с IV степенью тугоухости и глухотой (обзор литературы). Рос. оториноларингология. 2019;5(102):74–81. doi: 10.18692/1810-48002019-5-74-81 (In Russ.).
-
Diab H.M., Daikhes N.A., Pashchinina O.A. et al. Gentle method of introducing a standard electrode in cochlear ossification. Vestnik otorinolaringologii. 2016; 3: 54-6 / Диаб Х.М., Дайхес Н.А., ПащининаО.А. и др. Щадящий способ введения стандартного электрода при оссификации улитки. Вестник оториноларингологии. 2016;3:54–6 (In Russ.).
-
Jaekel K., Aschendorff A., Klenzner T., Laszig R. Results with the Contour cochlear implant in patients with cochlear otosclerosis. 2004;83:457–60.
doi: 10.1055/s-2004-814456.
-
Sanna M., Free R., Merkus P. Surgery for Cochlear and Other Auditory Implants. Stuttgart: Georg Thieme Verlag. 2016. P. 277–84.
-
Lee J., Nadol J.B. Jr., Eddington D.K. Factors associated with incomplete insertion of electrodes in cochlear implant surgery: A histopathologic study. 2011;16:69–81. doi: 10.1159/000316445.
-
Ramsden R., Rotteveel L., Proops D. Cochlear implantation in otosclerotic deafness. Otorhinolaryngol. 2007;65:328–34. doi: 10.1159/000098855.
-
Quaranta N., Bartoli R., Lopriore A. Cochlear implantation in otosclerosis. Neurotol. 2005;26:983–7.
-
Polak M., Ulubil S.A., Hodges A., Balkany T. Revision cochlear implantation for facial nerve stimulation in otosclerosis. Otolaryngol. Head Neck Surg.
2006;132:398–404. doi: 10.1001/archotol.132.4.398.
Поступила 17.04.20
Принята в печать 06.06.20
Received 17.04.20
Accepted 06.06.20
Вклад авторов: А.А. Каибов – концепция и дизайн исследования; Х.М. Диаб,
Н.А. Дайхес – анализ полученных данных, оценка результатов исследования; А.А. Каибов, А. Араби – обзор публикаций по теме статьи, сбор данных; написание текста рукописи; О.А. Пащинина – редактирование текста рукописи.
Contribution of the authors: A.A. Kaibov – concept and design of the study; H.M.
Diab, N.A. Dayhes – analysis of the data obtained, evaluation of the research
Информация об авторах:
Х.М.А. Диаб – д.м.н., заместитель директора по международной деятельности, главный научный сотрудник ФГБУ НМИЦО ФМБА России, Москва; e-mail: Hasandiab@mail.ru. https://orcid.org/0000-0002-2790-7900
Н.А. Дайхес – д.м.н., профессор, член-корр. РАН, директор ФГБУ НМИЦО
ФМБА России, Москва; e-mail: admin@otolar.ru. https://orcid.org/0000-0003-
2674-4553
А.А. Каибов – соискатель отдела заболеваний уха ФГБУ НМИЦО ФМБА
России, Москва; e-mail: kaibov2989@mail.ru. https://orcid.org/0000-00021235-002X
О.А. Пащинина – к.м.н., руководитель и заведующая отделением научноклинического отдела заболеваний уха ФГБУ НМИЦО ФМБА России, Москва; e-mail: Olga83@mail.ru. https://orcid.org/0000-0002-3608-2744
А. Араби – аспирант отдела заболеваний уха ФГБУ НМИЦО ФМБА России, Москва; e-mail: dr.aflatonarabi@mail.ru. https://orcid.org/0000-0002-3677-7095
Information about the authors:
K.M. Diab – Doctor of Medicine, Deputy Director for International Affairs, chief research officer of the Federal State Budgetary Institution «The National Medical Research Center for Otorhinolaryngology of the Federal Medico-Biological Agency of Russia», Moscow, Russia; e-mail: Hasandiab@mail.ru. https://orcid.org/0000-
0002-2790-7900
N.A. Daikhes – Doctor of Medicine, Professor, Associate Member of the Russian Academy of Sciences, Director, FSBI “The National Medical Research Center for Otorhinolaryngology of the FMBA of Russia”, Moscow; e-mail: admin@otolar.ru. https://orcid.org/0000-0003-2674-4553
A.A. Kaibov – postgraduate student, Department of diseases of the ear, FSBI
“The National Medical Research Center for Otorhinolaryngology of the FMBA of
Russia”, Moscow; e-mail: Kaibov2989@mail.ru. https://orcid.org/0000-0002-
1235-002X
O.A. Paschinina – PhD, Head of the Branch of the Clinical Research, Department of diseases of the ear, FSBI “The National Medical Research Center for Otorhinolaryngology of the FMBA of Russia”, Moscow; e-mail: Olga83@mail.ru. https://orcid.org/0000-0002-3608-2744
-
Arabi – postgraduate student, Department of diseases of the ear, FSBI “The National Medical Research Center for Otorhinolaryngology of the FMBA of
Russia”, Moscow; e-mail: dr.aflatonarabi@mail.ru. https://orcid.org/0000-00023677-7095
Статья посвящена актуальной теме, имеющей принципиально большое значение для врачей разных специальностей, включая оториноларингологов, неврологов, нейрохирургов. Авторы приводят аналитический обзор литературы по данной проблеме, но особый интерес представляет собственный материал, накопленный за последние годы, по применению различных хирургических способов устранения поражений лицевого нерва. Полученные результаты свидетельствуют об эффективных методах операций, проводимых авторами. Это представляется очень важным и своевременным, особенно в связи с тем, что данные воздействия в нашей стране до настоящего времени не нашли широкого применения и проводятся в единичных центрах. Накопленный опыт представляется уникальным и будет востребован и в научных, и в практических областях. Рекомендуется к печати.