Для цитирования: Морозов И.И., Грачев Н.С. Способ эндоскопической пластики стойкой перфорации перегородки носа. Голова и шея. Российский журнал Head and neck. Russian Journal. 2020;8(2):39–44
For citation: Morozov I.I., Grachev N.S. Method for endoscopic plastic surgery of persistent perforation of the nasal septum. Head and neck Russian Journal. 2020;8(2):39–44 (in Russian).
Основной причиной недостаточной эффективности хирургического лечения перфораций перегородки носа (ПН) является полное или частичное отторжение трансплантата и лоскутов слизистой оболочки, которое наблюдается в 7–37% случаев. При несостоятельности пластики значительно затрудняется выполнение повторных реконструктивных операций на ПН.
Цель исследования: повышение эффективности хирургического лечения перфораций ПН посредством разработки оптимального хирургического способа.
Материал и методы. В период с 2016 по 2018 г. по оригинальной методике были прооперированы 26 пациентов. Критерием оценки эффективности способа закрытия перфорации ПН являлось отсутствие реперфорации как на раннем этапе послеоперационного периода, так и в течение года после операции. Техническим результатом предлагаемого нами способа (патент RU 2705268) является повышение эффективности лечения стойких перфораций ПН за счет использования двух лоскутов слизистой оболочки на питающих ножках одной половины полости носа с интерпозицией между лоскутами фрагмента височной аутофасции. Указанный технический результат достигается путем выполнения вертикального разреза скальпелем по слизистой оболочке ПН, отступя кзади 0,5–1,0 см от места прикрепления средней носовой раковины, при этом разрез продолжают на дно полости носа по границе твердого и мягкого неба до основания нижней носовой раковины, далее скальпель поворачивают параллельно дну полости носа и продолжают разрез по латеральной стенке до переднего конца нижней носовой раковины, затем разрез разворачивают перпендикулярно к ПН и доводят до нижнего края перфорации, продолжают на задний край перфорации и поднимают вверх до спинки носа. Слизистую оболочку отсепаровывают под надхрящницей/под надкостницей, выделенный лоскут на решетчатых артериях смещают на область перфорации и вшивают в края перфорации. Предлагается первоначально получать поднадхрящничный лоскут из верхних отделов ПН, который ротируют в другую половину носа через верхний край перфорации ПН. Лоскут на решетчатых артериях имеет размер, достаточный для закрытия не только перфорации, но и донорской зоны первого лоскута, полученного из верхних отделов ПН, между лоскутами осуществляют интерпозицию фрагмента височной аутофасции, превышающего размеры дефекта вдвое. При наличии в верхних отделах ПН хряща ротацию первого лоскута можно осуществлять вместе с мобилизованным хрящом, что позволяет дополнительно укрепить остов ПН в зоне перфорации ПН.
Результаты. .Отмечено стойкое закрытие перфорации ПН, а также отсутствие рецидива в течение последующих 2 лет у всех Выводы. Полученные результаты позволяют утверждать, что метод является физиологичным и сочетает в себе восстановление анатомических взаимоотношений структур. Технико-экономическим улучшением следует считать сокращение сроков реабилитации после операции за счет меньшей травматизации тканей, безопасности методики, т.к. закрытие дефекта вышеуказанными структурами совместно позволяет снизить послеоперационные риски в виде флотации и травматизацииобласти закрытия септального дефекта. Предлагаемый способ позволил достигнуть результата, заключающегося в повышении эффективности пластики стойких перфораций ПН. Преимуществами метода являются простота выполнения, безопасность мобилизации мягких тканей, возможность результативно сформировать блок тканей, закрывающих дефект, и надежно зафиксировать его. Получаемый клинический результат существенно улучшает качество жизни пациентов данной категории . Способ может использоваться для пластики травматических, послеоперационных и идиопатических перфораций ПН.
Ключевые слова: перфорация перегородки носа, послеоперационная перфорация перегородки носа, хирургическое лечении перфораций перегородки носа, способ эндоскопической пластики перфорации перегородки носа.
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Работа выполнена без спонсорской поддержки
Для цитирования: Морозов И.И., Грачев Н.С. Способ эндоскопической пластики стойкой перфорации перегородки носа. Голова и шея. Российский журнал Head and neck. Russian Journal. 2020;8(2):39–44
Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
The main reason of low effectiveness of the nasal septum perforations (NSP) surgical treatment is complete or partial necrosis of the graft and the mucous membrane flaps, which is observed in 7–37% of cases. In these cases, it is significantly more difficult to perform repeated reconstructive operations on the nasal septum (NS).
Objective. To increase the effectiveness of surgical treatment of NSP through the development of an optimal surgical method.
Material and methods. In the period from 2016 to 2018, the original method of surgical treatment was performed in 26 patients, the criterion for effectiveness of the method was the absence of reperforation both at the early stage of the postoperative period and during the first year after surgery. The technical result of our proposed method is an increase of the NSP treatment effectiveness due to the use of two flaps of the mucous membrane on the pedicles from one half of the nasal cavity with interposition of temporal autofascia fragment between the flaps. This technical result is achieved by performing a vertical incision with a scalpel along the mucosa of the NS, with distance of 0.5–1.0 cm from the posterior border of the middle nasal concha attachment site projection, while the incision is continued to the bottom of the nasal cavity along the border of the hard and soft palate to the base of the lower concha, then the scalpel is turned parallel to the bottom of the nasal cavity and the incision is continued along the lateral wall to the front end of the lower nasal concha, then the incision is turned perpendicular to the nasal septum and brought to the lower perforation border, and continued to the posterior edge of the perforation and lift up to the nasal dorsum; the mucous membrane is separated under the perichondrium/ periosteum; the isolated flap on the ethmoid arteries is displaced to the perforation area and sutured to the perforation edges; it is proposed to initially obtain the subperichondrium flap from the upper sections of the NS, which will be rotated into the other half of the nose through the upper edge of the NSP. The flap on ethmoid arteries has the size sufficient to close not only the perforation, but also the donor zone of the first flap obtained from the upper sections of the NS; a twice size of the defect temporal autofascia fragment is interposed between the flaps. If there is cartilage in the upper sections of the NS, the rotation of the first flap can be carried out together with mobilized cartilage, which allows to further strengthen the basis of the NS in the perforation zone.
Results. We noted a durable closure of perforation of the nasal septum, as well as the absence of relapse over the next two years in all 26 patients.
Conclusions. The results obtained suggest that the method is physiological and combines the restoration of the anatomical relationships of structures. A technical and economic improvement should be considered in a reduction in the rehabilitation time after surgery, due to less tissue trauma, the safety of the technique, because defect closure by the abovementioned structures together can reduce such postoperative risks as the flotation and trauma to the septal defect closure area. The proposed method made it possible to achieve a result consisting in increasing the effectiveness of the plastic surgery of persistent perforation of the nasal septum. The advantages of the method are simplicity of execution, safety of mobilization of soft tissues, the ability to efficiently form a block of tissues covering the defect and to securely fix it. The resulting clinical effect significantly improves the quality of life of this category of patients. The method can be used to repair traumatic, postoperative and idiopathic perforations of the nasal septum.
Key words: nasal septum perforation, postoperative nasal septum perforation, surgical treatment of nasal septum perforations, endoscopic nasal septum perforation repair.
Conflicts of interest. The authors have no conflicts of interest to declare.
Funding. There was no funding for this study
For citation: Morozov I.I., Grachev N.S. Method for endoscopic plastic surgery of persistent perforation of the nasal septum. Head and neck Russian Journal. 2020;8(2):39–44 (in Russian).
The authors are responsible for the originality of the data presented and the possibility of publishing illustrative material – tables, figures, photographs of patients.
Введение
Несмотря на успехи ринохирургии, результаты операций по закрытию перфораций перегородки носа (ПН) свидетельствуют о необходимости дальнейшего изучения и разрешения ряда вопросов, связанных с повышением положительных функциональных исходов этих операций.
Основной причиной недостаточной эффективности хирургического лечения перфораций ПН является полное или частичное отторжение трансплантата или лоскутов слизистой оболочки, которое наблюдается, по данным литературы, в 7–37% случаев [1–6]. При несостоятельности пластики значительно затрудняется выполнение повторных операций на ПН [6, 7].
На сегодняшний день предложено много методов устранения перфорации ПН. Известен способ закрытия перфорации ПН по P. Castelnuovo, выбранный нами за прототип [7]. Способ включает в себя выполнение вертикального разреза скальпелем по ПН, отступя кзади 0,5–1,0 см от места прикрепления средней носовой раковины, при этом разрез продолжают на дно носовой полости и осуществляют до латеральных отделов нижнего носового хода, далее скальпель поворачивают параллельно ПН и продолжают разрез по латеральной стенке нижнего носового хода до переднего отдела, затем разрез разворачивают перпендикулярно к ПН и доводят до нижнего края перфорации, по заднему краю перфорацию и выше по ПН. Слизистую оболочку отсепаровывают, выделенный лоскут на передней решетчатой артерии смещают на область перфорации и вшивают в края перфорации. Края перфорации на контралатеральной стороне не ушивают. К ПН фиксируют силиконовые шины. Задние отделы ПН и дно полости носа остаются без слизистой оболочки, в полость носа на 2 дня помещают губку Мирацель. Недостатком способа является то, что авторы не закрывали перфорацию ПН на противоположной стороне, тонкий односторонний лоскут при дыхании подвержен флотации и травматизации. Деэпителизированные участки лоскута заживают вторичным натяжением, имеют длительный период заживления. Такая тактика влияет на результат операции и течение послеоперационного периода. Также формирование такого лоскута затруднительно в ранее оперированной ПН в условиях дефицита местных тканей.
Цель исследования: повышение эффективности хирургического лечения перфораций ПН посредством разработки оптимального хирургического способа.
Материал и методы
Техническим результатом предлагаемого нами способа (патент RU 2705268) является повышение эффективности лечения стойких перфораций ПН за счет использования двух лоскутов слизистой оболочки на питающих ножках одной половины полости носа с интерпозицией между лоскутами фрагмента височной аутофасции.
В период с 2016 по 2018 г. по данной методике оперированы 26 пациентов. Критерием оценки эффективности являлось отсутствие перфорации как на раннем этапе послеоперационного периода, так и в течение года после операции.
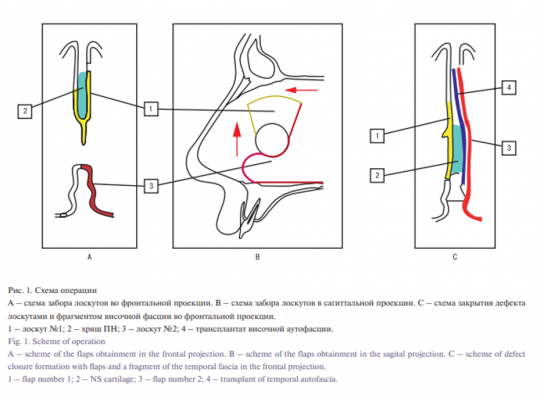
Способ осуществляют следующим образом (рис. 1). Хирургическое лечение проводят под видеоэндоскопическим контролем. В типичном месте, в преддверии носа слева, выполняют стандартный разрез для доступа к хрящу ПН как при септопластике. Поднадхрящнично производят отсепаровку мукоперихондрия до переднего края, далее под нижним краем перфорации на протяжении всего хрящевого отдела ПН. Параллельно спинке носа намечают линию разреза в 1,5 раза длиннее максимального горизонтального размера перфорации ПН. Далее от переднего и заднего концов линия продолжается радиально к центру септального дефекта, таким образом формируют первый лоскут (1) в форме перевернутой трапеции с ножкой в области верхнего края перфорации ПН. При наличии в верхнем крае перфорации септального хряща (2), выполняют полупроникающий разрез хряща и осуществляют отсепаровку поднадхрящнично с противоположной стороны сверху вниз. При отсутствии хряща, например вследствие ранее проведенной операции, следует проводить отсепаровку тканей аналогичным образом между листками мукоперихондрия, не повреждая верхний край перфорации ПН. Поднадкостнично из разреза на уровне переднего края перфорации ПН производят отсепаровку мукопериоста со дна полости носа от преддверия полости носа до заднего края небной пластинки верхней челюсти спереди-назад, латерально – до места прикрепления нижней носовой раковины, медиально ткани отсепаровывают до нижнего края перфорации и кзади от перфорации ПН на протяжении всего костного отдела ПН до уровня верхнего края перфорации ПН горизонтально и медиального края хоаны кзади. При помощи скальпеля по указанным границам производят мобилизацию лоскута (3), оставляя питающую ножку на решетчатых артериях кзади и сверху от перфорации ПН. В заушной области, отступя 4 см от места прикрепления ушной раковины, скальпелем делают разрез 4–5 см, выделяют фрагмент височной аутофасции (4), в 2 раза превышающий площадь дефекта ПН, разрез ушивают послойно. Фрагмент височной аутофасции (4) очищают от жира и мышечных волокон, не сушат. Первый лоскут (1) ротируют из одной половины носа в другую через верхний край перфорации ПН. Второй лоскут (3) перемещают в этой же половине носа кпереди и кверху для закрытия перфорации ПН и донорской зоны первого лоскута. Между лоскутами устанавливают аутотрансплантат – фрагмент височной фасции (4). Фиксацию осуществляют рассасывающимся шовным материалом транссептальными швами через оба лоскута (1, 3) и фрагмент височной аутофасции в области нижнего, переднего и заднего краев перфорации. Второй лоскут (3) дополнительно фиксируют швами в области разреза под спинкой носа, передний край лоскута (3) ушивают узловыми швами под кожей в области разреза в преддверии носа. ПН с двух сторон укрывают силиконовыми пластинами, которые фиксируют транссептальными швами на 1 см кпереди, кзади и кверху от проекции септального дефекта.
Таким образом, в результате операции перфорация ПН оказывается закрытой с обеих сторон эпителизированными лоскутами на питающей ножке и дополнительно укреплена фрагментом височной аутофасции. В случае расхождения или прорезывания швов в раннем послеоперационном периоде фасциальный трансплантат препятствует рецидиву перфорации – эпителизация продолжится по оппозиционному типу по фасции с краев лоскута. При ротации первого лоскута вместе с хрящом сохраняется связь хряща с питающим его мукоперихондрием в отличие от свободного хрящевого трансплантата. Лоскуты для пластики выкраивают только из одной половины носа, слизистая оболочка другой половины полости носа остается интактной, отсутствует фактор дополнительной хирургической травмы, сокращаются сроки реабилитации, повышается качество жизни пациентов в послеоперационном периоде.
Данный способ может использоваться для пластики травматических, послеоперационных и идиопатических перфораций ПН. Метод особенно актуален при закрытии послеоперационных перфораций в условиях дефицита тканей ПН. Способ позволяет повысить эффективность закрытия септальных перфораций и снизить число их рецидивов. Мы отмечали стойкое закрытие перфорации ПН, а также отсутствие рецидива в течение последующих 2 лет у всех 26 пациентов.
Клинический случай
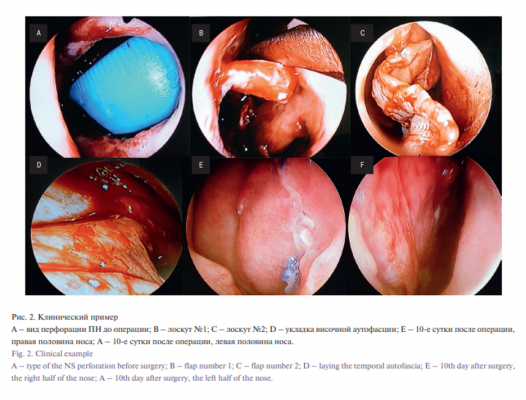
Пациент Ю., 40 лет. Клинический диагноз: «перфорация ПН (МКБ 10–J34.8)». Поступил в клинику с жалобами на заложенность носа, обильное число корочек в полости носа, периодически головную боль, носовые кровотечения. Из анамнеза известно, что эти жалобы беспокоят на протяжении последних 6 лет. В 2010 г. пациенту была проведена подслизистая резекция ПН. Наблюдался и лечился по месту жительства, консервативная терапия без положительного эффекта.
При осмотре: форма наружного носа не изменена, при риноскопии ПН по средней линии в хрящевом отделе имеется септальная перфорация 19х12 мм, умеренно выраженные рубцовые изменения слизистой оболочки. Носовые раковины не увеличены, реакция на лекарственную анемизацию слизистой оболочки выражена незначительно.
Под эндотрахеальным наркозом произвели хирургическое лечение по предлагаемому способу. У пациента отсутствовал септальный хрящ в верхнем крае перфорации. Осторожно осуществили отсепаровку тканей между листками мукоперихондрия, не повреждая верхний край перфорации. Сформировали первый лоскут. После формирования второго лоскута выполнили закрытие септального дефекта двумя лоскутами и фрагментом височной аутофасции, ПН с двух сторон укрыли силиконовыми пластинами с фиксацией транссептальными швами на 1 см кпереди, кзади и кверху от проекции септального дефекта. Произвели переднюю тампонаду носа. Операция прошла без осложнений.
После операции пациент Ю. получал антибактериальную терапию, тампоны удалены на 1-е сутки. Выписан на 4-е сутки. На 10-е сутки удалены силиконовые пластины. При осмотре ПН находилась по средней линии, трансплантат был состоятелен. В течение года рецидива перфорации ПН не отмечалось.
Обсуждение
Полученные результаты позволяют утверждать, что метод является физиологичным и сочетает в себе восстановление анатомических взаимоотношений структур. Технико-экономическим улучшением следует считать сокращение сроков реабилитации после операции за счет меньшей травматизации тканей, безопасности методики, т.к. закрытие дефекта вышеуказанными структурами позволяет снизить послеоперационные риски в виде флотации и травматизации области закрытия септального дефекта.
Предлагаемый способ позволил достигнуть результата, заключающегося в повышении эффективности пластики стойких перфораций ПН. Проведенные исследования свидетельствуют о том, что использование способа позволяет безопасно и с минимальными операционными рисками получать стойкий клинический результат.
Преимуществами метода являются простота выполнения, безопасность мобилизации мягких тканей, возможность результативно сформировать блок тканей, закрывающих дефект, и надежно зафиксировать его. Получаемый клинический результат существенно улучшает качество жизни пациентов данной категории.
Заключение
Способ может использоваться для пластики травматических, послеоперационных и идиопатических перфораций ПН. Способ позволяет повысить эффективность закрытия септальных перфораций и снизить число их рецидивов.
ЛИТЕРАТУРА
- Мейер Р. Перфорации перегородки носа должны и могут быть закрыты. Рос. ринология. 1995;3:12–27.
- Пискунов Г.З. Варианты и выполнение хирургического подхода при закрытии перфорации перегородки носа. Рос. ринология. 2012;4:30–4.
- КрюковА.И., КунельскаяН.Л., ЦарапкинГ.Ю., ТовмасянА.С., ПанасовС.А. Перфорация перегородки носа: современное состояние проблемы. Рос. ринология. 2016;1:4–9.
- Чекалдина Е.В., Лопатин А.С. Перфорации перегородки носа: наш опыт. Folia Otorhinolaryngol. Pathol. Respir. 2015;3:24–7.
- Pedroza F., Patrocinio L.G., Arevalo O. A review of 25-year experience of nasal septal perforation repair. Arch. Facial. Plast. Surg 2007;9(1):12–8. doi: 10.1001/archfaci.9.1.12.
- Lindemann J., Scheithauer M., Hoffmann T.K., Rettinger G., Kobes C., Sommer F. Long-term results after surgical closures of septal perforations. Laryngorhinootol. 2014;93(11):751–5. doi: 10.1055/s-0034-1385891.
- Castelnuovo P., et al. Anteriorethmoidal arteryseptal flap for the management of septal perforation. Archfacialplastsurg. 2011;13(6):411–4.
Поступила 02.02.20 Принята в печать 25.03.20
REFERENCES
- Meyer R. Nasal septum perforations must and can be closed. Ros. Rinol. 1995;3:12–27. (In Russ.).
- Piskunov G.Z. Varianty i vypolneniye khirurgicheskogo podkhoda pri zakrytii perforatsii peregorodki nosa. Ros. Rinol. 2012;4:30–4. (In Russ.).
- Kryukov A.I., Kunelskaya N.L., Tsarapkin G.Yu., Tovmasyan A.S., Panasov S.A. Nasal septal perforation: State-of-the-art. Ros. Rinol. 2016;1:4–9. (In Russ.).
- Chekaldina E., Lopatin A. Nasal septal perforations: our experience. Folia Otorhinolaryngol. Pathol. Respir 2015;3:24–7. (In Russ.).
- Pedroza F., Patrocinio L.G., Arevalo O. A review of 25-year experience of nasal septal perforation repair. Arch. Facial. Plast. Surg 2007;9(1):12–8. doi: 10.1001/ archfaci.9.1.12.
- Lindemann J., Scheithauer M., Hoffmann T.K., Rettinger G., Kobes C., Sommer F. Long-term results after surgical closures of septal perforations. Laryngorhinootol. 2014;93(11):751–5. doi: 10.1055/s-0034-1385891.
- Castelnuovo P., et al. Anteriorethmoidal arteryseptal flap for the management of septal perforation. Archfacialplastsurg. 2011;13(6):411–4.
Received 02.02.20 Accepted 25.03.20
Вклад авторов: И.В. Морозов, Н.С. Грачев – концепция и дизайн исследования. Морозов И.И. – сбор и обработка материала, статистическая обработка данных, написание текста. Грачев Н.С. – редактированиетекста. Authors’ contributions. I.V. Morozov, N.S. Grachev – research concept and design. Morozov I.I. – collection and processing of material, statistical data processing, writing text. Grachev N.S. – text editing.
Информация об авторах:
И.И. Морозов – начальник оториноларингологического отделения ФКУЗ ГКГ МВД России, ассистент кафедры оториноларингологии МИНО ФГБУ ВО МГУПП, Москва; e-mail: ivmoro@mail.ru; http://orcid.org/0000-0002- 7178-2594 Н.С. Грачев – д.м.н., доцент, руководитель группы ОГШ и РПХ, заведующий хирургическим отделением НМИЦ ДГОИ им. Дмитрия Рогачева, заведующий кафедрой Оториноларингологии МИНО ФГБУ «МГУПП», Москва, Россия; e-mail: nick-grachev@yandex.ru
Information about the authors:
I.I. Morozov – head of the ENT department of the FCHI Main Clinical Hospital of the Ministry of IA of Russia; Assistant of the Department of Otorhinolaryngology of the Medical Institute of continuous education of FSBI HE MSUFP Moscow, Russia; e-mail: ivmoro@mail.ru; http://orcid.org/0000-0002-7178-2594
N.S. Grachev – Doctor of Medicine, Head of Division of Head and Neck Surgery with Reconstructive and Plastic Surgery (HNS-RPS), head of Surgical Department of Dmitriy Rogachev National Medical Research Center of Pediatric Hematology, Oncology and Immunology; Head of ENT Department, Medical Institute of continuous education of FSBI HE MSUFP, Moscow, Russia; e-mail: nick-grachev@yandex.ru