Для цитирования: Синельников М.Е., Бабаева Ю.В., Старцева О.И., Бурдин С.А. Острые сосудистые осложнения после контурной пластики лица. Механизмы развития патологии, методы профилактики и лечения. Голова и шея. Российский журнал Head and neck Russian Journal. 2020;8(1):63–68
For citation: Sinelnikov M.E., Babaeva J.V., Startseva O.I., Burdin S.A. Acute vascular complications after facial contouring. Mechanisms of development, methods of prevention and treatment. Golova i sheya. Rossijskij zhurnal Head and neck Russian Journal. 2020;8(1):63–68 (in Russian).
Doi: 10.25792/HN.2020.8.1.63–68
Сосудистые осложнение после контурной пластики лица требуют неотложной медицинской помощи, чреваты серьезными эстетическими и функциональными нарушениями, в редких случаях – летальным исходом. В данной работе рассмотрены механизмы формирования эмболизации сосуда при непреднамеренном введении филлера в его просвет. Для минимизации риска серьезных осложнений необходимо соблюдать правило АБВ – Аспирационная проба; Болевой контроль, Высокократное и медленное введение филлера. Разработана тактика коррекции сосудистых осложнений после контурной пластики лица. Выполнение разработанного алгоритма СТАП-ТРОМБ направлено на улучшение кровоснабжения ишемизированных тканей в присутствии артериального эмбола. Несмотря на преимущество минимально инвазивных методик с применением филлеров на основе гиалуроновой кислоты, CaHA, PLLA, PMMA, аутологичного жира, отсутствие объективных методов оценки сосудистой анатомии во время выполнения процедуры делает данную манипуляцию опасной и требующей высокой квалификации специалиста. Понимание механизма артериальной эмболизации, путей распространения эмбола, знание методов коррекции осложнений является приоритетом врача, выполняющего данную процедуру.
Ключевые слова: острые сосудистые осложнения, артериальная эмболия, эмболизация, ятрогенные осложнения, контурная пластика, косметология, пластическая хирургия, осложнения эстетической медицины
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Работа выполнена без спонсорской поддержки
Для цитирования: Синельников М.Е., Бабаева Ю.В., Старцева О.И., Бурдин С.А. Острые сосудистые осложнения после контурной пластики лица. Механизмы развития патологии, методы профилактики и лечения. Голова и шея. Российский журнал Head and neck Russian Journal. 2020;8(1):63–68
Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
Vascular complications after facial contouring require emergency medical care; they may lead to serious aesthetic and functional disorders, and in rare cases, to death. In this paper, we describe the mechanisms of formation of a blood vessel embolization after the unintentional adninistration of a filler into its lumen. To minimize the risk of serious complications, it is necessary to comply with the APH rule – Aspiration test; Pain control; High-fold and slow administration of filler. The tactics of correction of vascular complications after facial contouring has been developed. Implementation of the developed STAP-TROMB algorithm is aimed at improving blood supply to ischemic tissues in the presence of an arterial embolus. Despite the advantage of minimally invasive techniques using fillers based on hyaluronic acid, CaHA, PLLA, PMMA, autologous fat, the lack of objective methods for assessing vascular anatomy during the procedure makes this manipulation dangerous and requires highly qualified specialist. Understanding the mechanism of arterial embolization, the pathways of embolus distribution, knowledge of methods for correcting complications is the priority of the doctor performing this procedure.
Key words: acute vascular complications, arterial embolism, embolization, iatrogenic complications, contouring, cosmetology, plastic surgery, aesthetic medicine complications
Conflicts of interest. The authors have no conflicts of interest to declare. Funding. There was no funding for this study.
For citation: Sinelnikov M.E., Babaeva J.V., Startseva O.I., Burdin S.A. Acute vascular complications after facial contouring. Mechanisms of development, methods of prevention and treatment. Golova i sheya. Rossijskij zhurnal Head and neck Russian Journal. 2020;8(1):63–68 (in Russian).
The authors are responsible for the originality of the data presented and the possibility of publishing illustrative material – tables, figures, photographs of patients.
Введение
Применение экзогенных и аутологичных филлеров в клинической практике врача дерматолога-косметолога и пластического хирурга становится одной из наиболее распространенных эстетических процедур. По данным Международного общества эстетической пластической хирургии (ISAPS), за 2017 г. во всем мире 3 298 266 пациентам была выполнена инъекция филлера на основе гиалуроновой кислоты (HA), 602 760 пациентам выполнена контурная пластика аутологичным жиром (AFG), 167 385 пациентам выполнена установка филлера на основе гидроксиапатита кальция (CaHA), 72 852 пациентам выполнена инъекция филлеров на основе поли-L-молочной кислоты (PLLA) [1]. Таким образом, за 2017 г. выполнено более 4 000 000 официально зарегистрированных процедур. Следует отметить, что настоящее число выполняемых процедур значительно больше, т.к. многие страны не принимают участия в опросах ISAPS и часто данные процедуры выполняются незаконно. Оценивая статистику выполнения контурной пластики лица инъекционными наполнителями в США, можно предположить частоту выполнения данной процедуры. При населении в 325 700 000 на 2017 г. в США выполнено более 2 000 000 инъекций филлеров на лице, что означает, что около 0,6% населения подвержены риску осложнений от данной процедуры. К сравнению, аугментацию молочных желез выполняют лишь 0,00009% населения США [1].
Постоянно увеличивающийся спрос на контурную пластику лица сопровождается увеличением количества и разнообразия осложнений от легких (эритема, транзиторный отек) до тяжелых (острое нарушение зрения, локальные некрозы) и летальных (инсульт). Квалифицированный специалист, который выполняет данную процедуру, должен на профессиональном уровне понимать все аспекты выполняемой минимально-инвазивной манипуляции. В данной статье будут рассмотрены анатомические, физические и клинические аспекты развития острых сосудистых осложнений при использовании филлеров для инъекционной контурной пластики лица.
С появления инъекционных тканевых филлеров известны всевозможные осложнения при их применении в клинической практике. Побочные эффекты, развивающиеся после установки филлера, относят к вторичным, они включают покраснение, отек, инфекционные осложнения (абсцедирование, грануляции, воспаление) и другие обратимые осложнения [2]. Наиболее опасными являются острые сосудистые осложнения, возникающие сразу или в ближайшее время после введения филлера. С целью систематизации существующих данных о предупреждении, механизмах развития и лечении острых сосудистых осложнений, связанных с проведением контурной пластики, проведен анализ литературных данных, разработаны рекомендации по лечению.
Было проведено исследование литературы по базам данных, таких как PubMed, Medline и других (eMedicine, NLM, ReleMed). Был проведен автоматический поиск и ручная отборка статей. Всего при введении ключевых слов «vascular complications», «filler», «Injection», «Complication», «Treatment» было получено 86 статьей, отвечающих на вопросы, актуальные для нашего анализа. Из них выбраны наиболее актуальные вопросы по параметрам рассмотрения сосудистых осложнений при контурной пластике лица.
Результаты проведенного анализа
Артериальная эмболизация. Наиболее опасным осложнением при выполнении контурной пластики филлерами является непреднамеренное введение филлера в сосуд и/или эмболизация филлера в артериальную систему [3, 4]. Данное осложнение проявляется некрозом мягких тканей, нарушением зрения вплоть до слепоты и даже инсультом [5–8]. Наиболее опасными зонами с высоким риском артериальной эмболизации являются глабелла, фронтальная, носогубные, скулоорбитальные, назальная области, а также нижняя губа и носослезные борозды [9–11].
Острые сосудистые осложнения могут возникнуть независимо от опыта врача, выполняющего процедуру, и только четкое понимание механизма артериальной окклюзии, симптоматики и агрессивная тактика лечения могут спасти жизнь пациента и предотвратить необратимые изменения тканей.
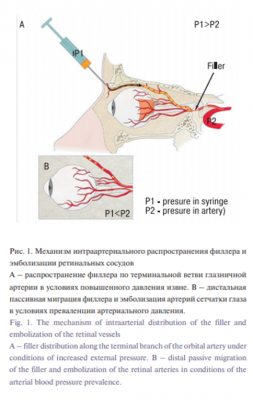
Механизм артериальной эмболизации сложен и характеризуется высоким давлением, создаваемым вводимым препаратом в ограниченные компартменты лица [12]. Наиболее часто филлер непреднамеренно вводится в поверхностные артериальные сосуды средней и верхней третей лица. Сосуды данных областей являются конечными (терминальными) ветвями глазной артерии (скуло-темпоральная, скулолицевая, надглазничная, надблоковая артерии, артерия спинки носа, угловая артерия носа). Артерия сетчатки глаза и задние цилиарные артерии являются проксимальными ветвями глазничной артерии [13]. Введение филлера в терминальные ветви глазничной артерии в условиях высокого давления, а иногда и за счет ретроградной внутрисосудистой миграции филлера способствует попаданию филлера в более проксимальные отделы глазничной артерии, что может привести к острой потере зрения и инсульту [14]. Потеря зрения наблюдается в случае, если проксимальная миграция филлера не доходит до места отхождения глазничной артерии от внутренней сонной артерии. В случае проксимальной миграции до места отхождения сосуда от сонной артерии высока вероятность развития инсульта [15]. Таким образом, филлер, введенный в терминальную ветвь глазничной артерии, мигрирует по пути минимального сопротивления (от шприца с высоким давлением, создаваемым рукой оператора) в более проксимальные отделы и при прекращении введения (извлечение иглы приводит к восстановлению преваленции систолического артериального давления и моментальной эмболизации филлера) филлер распространяется по всем ветвям дистальнее максимально достигнутой точки введения. Именно этот механизм стоит в основе эмболизации более глубоких сосудистых структур лица (рис. 1).
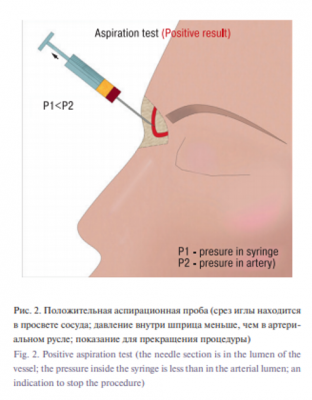
Меры профилактики. При понимании основного механизма эмболизации становятся очевидными меры профилактики тяжелого осложнения. Для минимизации риска серьезных осложнений авторы предлагают соблюдать правило АБВ – Аспирационная проба; Болевой контроль; Высокократное и медленное введение филлера. Аспирационная проба проводится после введения иглы в зону коррекции и перед началом подачи препарата. Осуществляется легкое обратное движение поршня шприца с целью создать отрицательное давление в шприце, тем самым обеспечить благоприятные условия для поступления крови в шприц [16]. Отсутствие следов крови при выполнении аспирационной пробы наиболее часто свидетельствует о локализации иглы вне сосуда, что является показанием для продолжения процедуры. Присутствие следов крови в шприце свидетельствует о нарушении целостности сосудистой стенки иглой (рис. 2) и является показанием для незамедлительного прекращения процедуры [17, 18]. Высокократное и медленное введение филлера определяет ограничения по технике введения препарата в реципиентную зону: филлер должен вводиться небольшими порциями (до 0,1 мл) по проекции желаемой зоны заполнения, медленно, без усиленного давления на поршень. Это позволяет предупредить развитие глубоких тромботических процессов даже при попадании препарата в сосудистое русло [19]. Стоит отметить, что данная методика не уменьшает риска развития локальных некрозов [20]. Болевой контроль дополняет вышеуказанные методики и заключается в постоянном контроле состоянии пациента. Резкие болевые ощущения при введении препарата характерны для тромботических процессов. Острая боль при введении иглы часто связана с перфорацией сосудистой стенки [21]. При отрицательной аспирационной пробе, сопровождающейся резкими болевыми ощущениями в зоне инъекции, высока вероятность нахождения иглы в просвете сосуда [22, 23].
Диагностика. Диагноз острой артериальной окклюзии с вторичной тканевой ишемией после введения филлера экзогенного или эндогенного происхождения устанавливается по клиническим проявлениям, как ранним (острая боль, побледнение кожи, нарушение зрения), так и отсроченным (прогрессирующий некроз, вторичное инфицирование кожи, слепота) [24]. Локализация поражения уточняется на основании местных проявлений артериальной эмболизации: локальных некротических процессов, клинической картины и зоны побледнения.
Уточнение локализации эмбола является важным диагностическим признаком, который определяет дальнейшее лечение, а также позволяет дифференцировать местный тканевой некроз от более глубоких артериальных окклюзий (инсульт, слепота, парезы) [25].
Лечение. В зависимости от введенного препарата формируется тактика лечения. Пациенты с диагностированным интраартериальным введением филлера требуют экстренной медицинской помощи. По результатам анализа литературных данных можно сделать вывод, что тактика лечения должна включать следующий алгоритм [26–32]:
- Срочно прекратить выполнение запланированной процедуры и любых других манипуляций.
- Провести тепловую компрессию пораженной зоны с целью вазодилатации.
- Произвести подкожное введение эноксипарина или перорально применить ацетилсалициловую кислоту (при отсутствии противопоказаний, в комбинации с антацидами).
- Начать профилактическую противовирусную и противобактериальную терапию (чаще всего используется комбинация цефтриаксон+ацикловир).
- Выполнить 3-часовой курс аппликаций 2% нитроглицериновой мази на пораженную зону с перерывами в 5–15 минут.
- В случае использования филлеров на основе гиалуроновой кислоты выполнить инъекцию раствора гиалуронидазы вокруг и в месте введения филлера.
- Начать курс гипербарической оксигенации по показаниям.
- Начать курс лечения метилпреднизолоном.
- Назначить ингибитор фосфодиэстеразы 5-го типа (тадалафил, варденафил силденафил – Виагра) с целью ингибирования деградации циклического гуанозин-монофосфата, что способствует расслаблению мышечной стенки сосуда и улучшенной вазодилатации.
Для лучшего запоминания, авторы работы предлагают представить данный алгоритм в виде акронима СТАП ТРОМБ:
Срочно прекратить интервенцию
Тепловая компрессия (локально)
Ацетилсалициловая кислота (per os)
Профилактическая противовирусная и противобактериальная терапия
Трехчасовая аппликация 2% нитроглицериновой мази (местно)
Раствор гиалуронидазы (инъекции в зону поражения)
Оксигенация гипербарическая (при необходимости)
Метилпреднизолон (курс)
Блокатор фосфодиэстеразы 5-го типа (вазодилатация).
Выполнение данного алгоритма направлено на улучшение кровоснабжения ишемизированных тканей при наличии артериального эмбола. Этиопатогенетическое лечение доступно лишь в случаях применения препаратов гиалуроновой кислоты, т.к. введение гиалуронидазы позволяет растворить эмбол с восстановлением кровотока в пораженных тканях [33].
Применение гиалуронидазы оправдано в случаях артериальной эмболизации филлерами на основе гиалуроновой кислоты. Препарат оказывает ферментативное расщепление полимеров гиалуроновой кислоты [34, 35].
Локальные аппликации 2% нитроглицериновой мази способствуют расширению сосудов и перераспределению кровотока, что может способствовать направлению кровотока в зону ишемии. Нитроглицерин стоит наносить каждые 5 минут в течение 2–3 часов, с учетом самочувствия пациента [36].
С целью уменьшения проявлений воспалительной реакции на ишемию ткани применяются глюкокортикостероиды. Применение высоких доз пероральных кортикостероидных препаратов в течение 4–5 дней (60 мг) облегчает симптоматику в результате снижения уровня отека и вторичной компрессии. С осторожностью использовать у пациентов с сахарным диабетом (контроль глюкозы крови) [37, 38].
Ацетилсалициловая кислота необходима для ускорения внутрисосудистого фибринолиза и нормализации воспалительной гиперреактивности. Рекомендованная доза 325 мг перорально в сутки в течение 7–14 дней [39].
Блокаторы (ингибиторы) фосфодиэстеразы 5-го типа ингибируют расщепление молекулы cGMF, что способствует расслаблению артериальной стенки и улучшению вазодилатации. Назначают силденафил 100 мг/сут в течение 7–14 дней до восстановления кровотока [40].
Противовирусная и антибактериальная терапия: цефалоспорин 500 мг 4 раза в сутки или клиндамицин 150 мг 4 раза в сутки, или цефтриаксон 1000 мг 2 раза в сутки, ацикловир 800 мг 5 раз в сутки. Продолжать курс превентивной терапии до эпителизации ишемизированных тканей [41, 42].
Гипербарическая оксигенация показана при некротических процессах. Лечение проводить в режиме 3 атмосферы, 45 минут в сутки, до восстановления нормальной эпителизации [43, 44].
Обсуждение
Острые сосудистые осложнения контурной пластики даже при агрессивной и вовремя начатой терапии часто приводят к необратимым патологическим изменениям. Несмотря на преимущество минимально инвазивных методик с применением филлеров на основе гиалуроновой кислоты, CaHA, PLLA, PMMA, аутологичного жира. Отсутствие объективных методов оценки сосудистой анатомии во время выполнения процедуры делает данную манипуляцию опасной, что требует высокой квалификации специалиста.
Пациенты с клинической манифестацией острого сосудистого осложнения после контурной пластики должны получить экстренную медицинскую помощь в стационарном отделении. Клиники с лицензией на выполнение косметологических процедур должны быть оснащены необходимыми лекарственными средствами для немедленной коррекции острых осложнений для исключения тяжелых, а порой летальных последствий.
Понимание механизма развития острых сосудистых осложнений позволит более эффективно проводить профилактику и лечебные мероприятия для коррекции последствий введения филлера в артериальное русло. Наиболее эффективным методом предотвращения острых сосудистых осложнений является профилактика, которая должна быть направлена на снижение объема однократного введения филлера, медленную скорость введения филлера с целью сохранения низкого давления внутри шприца, выполнение аспирационной пробы. Если, несмотря на проведенные профилактические меры возникает развитие острого сосудистого осложнения, то необходимо знание алгоритма оказания экстренной медицинской помощи. Неотложные мероприятия по восстановлению кровотока и устранению патологических последствий внутриартериального введения филлера позволяют предотвратить тяжелые осложнения и инвалидизацию пациента.
ЛИТЕРАТУРА/REFERENCES
- International Society of Aesthetic Plastic Surgery. 2017. ISAPS International Survey on aesthetic/cosmetic procedures performed in 2017. Available at: https:// www.isaps.org/wp-content/uploads/2018/10/ISAPS_2017_International_ Study_Cosmetic_Procedures.pdf.
- Coleman S.R. Injectable silicone returns to the United States. Aesth. Surg. J. 2001;21(6):576–8.
- Kim Y.J., Kim S.S., Song W.K., Lee S.Y., et al. Ocular Ischemia With Hypotony After Injection of Hyaluronic Acid Gel. Ophthalm. Plast. Reconstruct. Surg. 2011;27(6):e152–5. doi: 10.1097/iop.0b013e3182082f37.
- Carruthers J.D., Fagien S., Rohrich R.J., Weinkle S., Carruthers A. Blindness caused by cosmetic filler injection: a review of cause and therapy. Plast. Reconstr. Surg. 2014;134(6):1197–201.
- Sung M.S., Kim H.G., Woo K., Kim Y.D. Ocular ischemia and ischemic oculomotor nerve palsy after vascular embolization of injectable calcium hydroxylapatite filler. Ophthalm. Plast. Reconstruct. Surg. 2010;26(4):289–91.
- Kang M.S., Park E.S., Shin H.S., Jung S.G., Kim Y.B., Kim D.W. Skin necrosis of the nasal ala after injection of dermal fillers. Dermatol. Surg. 2011;37(3):375– 80.
- Woodward J., Khan T., Martin J. Facial filler complications. Facial Plast. Surg. Clin. 2015;23(4):447–58.
- Rayess H.M., Svider P.F., Hanba C., Patel V.S., DeJoseph L.M., Carron M., Zuliani G.F. A cross-sectional analysis of adverse events and litigation for injectable fillers. JAMA. Facial Plast. Surg. 2018;20(3):207–14.
- Khan T.T., Colon-Acevedo B., Mettu P., DeLorenzi C., Woodward J.A. An anatomical analysis of the supratrochlear artery: considerations in facial filler injections and preventing vision loss. Aesth. Surg. J. 2007;37(2):203–8.
- Ferneini E., Gady J., Nuveen E. Complications associated with facial soft-tissue fillers. Am. J. Cosmet. Surg. 2014;31(4):238–42.
- Ozturk C.N., Li Y., Tung R., Parker L., Piliang M.P., Zins J.E. Complications following injection of soft-tissue fillers. Aesth. Surg. J. 2013;33(6):862–77.
- Tansatit T., Moon H.J., Apinuntrum P., Phetudom T. Verification of embolic channel causing blindness following filler injection. Aesth. Plast. Surg. 2015;39(1):154–61.
- Hayreh S.S. Orbital vascular anatomy. Eye. 2006;20(10):1130–44.
- Carle M.V., Roe R., Novack R., Boyer D.S. Cosmetic facial fillers and severe vision loss. JAMA. Ophthalmol. 2014;132(5):637–9.
- Lee W.S., Yoon W.T., Choi Y.J., Park S.P. Multiple cerebral infarctions with neurological symptoms and ophthalmic artery occlusion after filler injection. J. Korean Ophthalmol. Soc. 2015;56(2):285–90.
- Casabona G. Blood aspiration test for cosmetic fillers to prevent accidental intravascular injection in the face. Dermatol. Surg. 2015;41(7):841–7.
- Van Loghem J.A., Fouché J.J., Thuis J. Sensitivity of aspiration as a safety test before injection of soft tissue fillers. J. Cosmet. Dermatol. 2018;17(1):39–46.
- Carey W., Weinkle S. Retraction of the plunger on a syringe of hyaluronic acid before injection: are we safe? Dermatol. Surg. 2015;41:S340–6.
- Li X., Le Du J.L. A novel hypothesis of visual loss secondary to cosmetic facial filler injection. Ann. Plast. Surg. 2015;75(3):258.
- Glogau R.G., Kane M.A. Effect of injection techniques on the rate of local adverse events in patients implanted with nonanimal hyaluronic acid gel dermal fillers. Dermatologic surgery. 2008;34:S105-S109.
- Van Dyke S, Hays GP, Caglia AE, Caglia M. Severe acute local reactions to a hyaluronic acid-derived dermal filler. J. Clin. Aesth. Dermatol. 2010;3(5):32.
- Ferneini E.M., Ferneini A.M. An overview of vascular adverse events associated with facial soft tissue fillers: recognition, prevention, and treatment. J. Oral Maxillofacial. Surg. 2016;74(8):1630–6.
- Engelman D.E., Bloom B., Goldberg D.J. Dermal fillers: complications and informed consent. J. Cosmet. Laser Ther. 20015;7(1):29–32.
- Bolton J.G., Fabi S.G. Complications of temporary fillers. Soft Tissue Augmentation E-Book: Procedures in Cosmetic Dermatology Series. 2017. 191 р.
- Fitzgerald R., Bertucci V., Sykes J.M., Duplechain J.K. Adverse reactions to injectable fillers. Facial Plast. Surg. 2016;32(05):532–55.
- Lee D.H., Yang H.N., Kim J.C., Shyn K.H. Sudden unilateral visual loss and brain infarction after autologous fat injection into nasolabial groove. Br. J. Ophthalmol. 1996;80(11):1026–7.
- Thaunat O., Thaler F., Loirat P., Decroix J.P., et al. Cerebral fat embolism induced by facial fat injection. Plast. Reconstr. Surg. 2004;113(7):2235–6.
- Yoon S.S., Chang D.I., Chung K.C. Acute fatal stroke immediately following autologous fat injection into the face. Neurol. 2003;61(8):1151–2.
- US Food and Drug Administration. Current and Useful Information on Collagen and Liquid Silicone Injections. FDA Backgrounder, August 1991. BG91-2.0.
- Kwon S.G., Hong J.W., Roh T.S., Kim Y.S., et al. Ischemic oculomotor nerve palsy and skin necrosis caused by vascular embolization after hyaluronic Acid filler injection: a case report. Ann. Plast .Surg. 2013;71(4):333–4. doi: 10.1097/ SAP.0b013e31824f21da.
- Peter S., Mennel S. Retinal branch artery occlusion following injection of hyaluronic acid (Restylane). Clin. Exp. Ophthalmol. 2006;34(4):363–4. doi: 10.1111/j.1442-9071.2006.01224.x.
- Grunebaum L.D., Bogdan Allemann I., Dayan S., Mandy S., et al. The risk of alar necrosis associated with dermal filler injection. Dermatol. Surg. 2009;35(Suppl. 2):1635–40. doi: 10.1111/j.1524-4725.2009.01342.x.
- DeLorenzi C. New high dose pulsed hyaluronidase protocol for hyaluronic acid filler vascular adverse events. Aesth. Surg. J. 2017;37(7):814–25.
- Chesnut C. Restoration of visual loss with retrobulbar hyaluronidase injection after hyaluronic acid filler. Dermatol. Surg. 2018;44(3):435–7.
- Loh K.T.D., Phoon Y.S., Phua V., Kapoor K.M. Successfully managing impending skin necrosis following hyaluronic acid filler injection, using high-dose pulsed hyaluronidase. Plast. Reconstruct. Surg. Global Open. 2018:6(2):1–3.
- Carley S.K., Kraus C.N., Cohen J.L. Nitroglycerin, or Not, When Treating Impending Filler Necrosis. Dermatol. Surg. 2020;46(1):31–40.
- Salval A., Ciancio F., Margara A., Bonomi S. Impending facial skin necrosis and ocular involvement after dermal filler injection: a case report. Aesth. Plast. Surg. 2017;41(5):1198–201.
- Dominguez S., Moshrefi S., Dobke M. Treatment Protocol for Acute Arterial Occlusion Secondary to Facial Revolumization Procedures Artificial injectable dermal fillers offer minimally invasive and cost-effective alternatives to traditional cosmetic surgical procedures, but are associated with complications and adverse events. Emergency Med. 2017;49(5):221–9.
- Rullan P.P., Lee K.C. Successful management of extreme pain from delayed embolization after hyaluronic acid filler injection. JAAD. Case Rep. 2019;5(7):569–71.
- Urdiales-Gálvez F., Delgado N.E., Figueiredo V., Lajo-Plaza J.V., Mira M., Moreno A., Segurado M.A. Treatment of soft tissue filler complications: expert consensus recommendations. Aesth. Plast. Surg. 2018;42(2):498–510.
- Signorini M., Liew S., Sundaram H., De Boulle K.L., Goodman G.J., Monheit G., Group GAC. Global aesthetics consensus: avoidance and management of complications from hyaluronic acid fillers – evidence and opinion-based review and consensus recommendations. Plast. Reconstruct. Surg. 2016;137(6):961.
- Abduljabbar M.H., Basendwh M.A. Complications of hyaluronic acid fillers and their managements. J. Dermatol. Derm. Surg. 2016;20(2):100–6.
- Olszański R., Dąbrowiecki Z., Marusza W., Netsvyetayeva I., Niewiedział D., Siermontowski P., Zieliński E. Vascular Complication in Aesthetic Medicine Treated with Hyperbaric Oxygenation. Polish Hyperbaric. Res. 2018; 63(2):18–21.
- Hwang K. Hyperbaric oxygen therapy to avoid blindness from filler injection. J. Craniofac. Surg. 2016;27(8):2154–5.
Поступила 11.11.19 Принята в печать 11.12.19
Received 11.11.19 Accepted 11.12.19
Вклад авторов: Синельников М.Е., Бабаева Ю.В., Старцева О.И., Бурдин С.А.: концепция и дизайн исследования, обзор публикаций по теме статьи, сбор данных, анализ полученных данных, написание текста рукописи, редактирование.
Authors’ contributions. Sinelnikov M.E., Babaeva J.V., Startseva O.I., Burdin S.A.: conception and design of the study, data collection and analysis, manuscript preparation, and editing
Информация об авторах:
М.Е. Синельников – врач, младший научный сотрудник, Институт Регенеративной Медицины ФГОАУ ВО Первый МГМУ им. И.М. Сеченова Минздрава РФ (Сеченовский университет), Москва; e-mail: Mikhail.y.sinelnikov@gmail.com. https://orcid.org/0000-0002-0862-6011
Ю.В. Бабаева – к.м.н., заведующая учебной частью кафедры онкологии, радиотерапии и пластической хирургии ФГОАУ ВО Первый МГМУ им. И.М. Сеченова Минздрава РФ (Сеченовский университет), Москва; e-mail: juliybelova@yandex.ru. https://orcid.org/0000-0003-2170-7286
О.И. Старцева – д.м.н., профессор кафедры онкологии, радиотерапии и пластической хирургии ФГОАУ ВО Первый МГМУ им. И.М. Сеченова Минздрава РФ (Сеченовский университет), Москва; e-mail: ostarceva@mail. ru, https://orcid.org/0000-0001-9778-2624
С.А. Бурдин – студент школы мастерства по пластической хирургии лечебного факультета ФГОАУ ВО Первый МГМУ им. И.М. Сеченова Минздрава РФ (Сеченовский университет), Москва; e-mail: burdybreed@ gmail.com, https://orcid.org/0000-0002-2453-0722
Information about the authors:
M.E. Sinelnikov – MD, junior researcher, Institute of Regenerative Medicine FSEAI HE First MSMU n.a. I.M. Sechenov of the Ministry of Health of the Russian Federation (Sechenov University), Moscow; e-mail: Mikhail.y.sinelnikov@gmail. com. https://orcid.org/0000-0002-0862-6011
J.V. Babaeva – PhD, head of the educational department of the Department of Oncology, Radiotherapy and Plastic Surgery FSEAI HE First MSMU n.a. I.M. Sechenov of the Ministry of Health of the Russian Federation (Sechenov University), Moscow; e-mail: juliybelova@yandex.ru. https://orcid.org/0000-0003-2170-7286
O.I. Startseva – Doctor of Medicine, professor of the Department of Oncology, Radiotherapy and Plastic Surgery FSEAI HE First MSMU n.a. I.M. Sechenov of the Ministry of Health of the Russian Federation (Sechenov University), Moscow; e-mail: ostarceva@mail.ru, https://orcid.org/0000-0001-9778-2624
S.A. Burdin — a student of the School of Excellence in Plastic Surgery, Faculty of Medicine, FSEAI HE First MSMU n.a. I.M. Sechenov of the Ministry of Health of the Russian Federation (Sechenov University), Moscow; e-mail: burdybreed@ gmail.com, https://orcid.org/0000-0002-2453-0722