Для цитирования: Решетов И.В., Гапонов М.Е., Святославов Д.С., Богословский С.Г. Реконструкция дефектов средней зоны лица композитными материалами Голова и шея. Российский журнал = Head and neck. Russian Journal. 2020;8(1):22–31
For citation: Reshetov I.V., Gaponov M.E., Svyatoslavov D.S., Bogoslovsky S.G. Reconstruction of the face middle zone defects with composite materials. Head and neck. Russian Journal. 2020;8(1):22–31 (in Russian).
Doi: 10.25792/HN.2020.8.1.22–31
Цель работы: оценить клинические случаи с использованием индивидуальных эндопротезов, изготовленных из биосовместимых композитных материалов на основе гидроксиапатита и метилметакрилата с использованием компьютерного моделирования, и последующего изготовления для реконструкции лицевого скелета.
Материал и методы. В создании 3-мерной модели костного дефекта используется компьютерная томография (КТ). Полученные данные DICOM преобразуются в файлы стереолитографии посредством алгоритма создания индивидуальных имплантатов, после чего модель печатается на стереолитографическом принтере. Для изготовления имплантата использовали Гидроксилапатит – ГАП-99г, полученная модель высвобождается из пресс-форм и подвергается стерилизации.
Результаты и обсуждение. В ходе проведения работы устранены посттравматический дефект верхней челюсти, нижнего орбитального края слева и дефект верхней челюсти слева.
Заключение. Использование композитных материалов на основе ГАП для замещения костных дефектов черепа позволяет значительно повысить эффективность лечения и качество реабилитации этой сложной категории пациентов.
Ключевые слова: костные дефекты, Гидроксилапатит – ГАП-99
Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов.
Финансирование. Работа выполнена при финансовой поддержке Министерства образования и науки Российской Федерации, субсидия на реализацию комплексных проектов по созданию высокотехнологичного производства в рамках реализации постановления Правительства Российской Федерации от 9 апреля 2010 г. № 218, очередь 8 по теме «Создание высокотехнологичного цифрового производства прецизионных металлических комплексов для имплантации на базе аддитивных технологий», номер соглашения 03.G25.31.0234 от 03.03.2017.
Для цитирования: Решетов И.В., Гапонов М.Е., Святославов Д.С., Богословский С.Г. Реконструкция дефектов средней зоны лица композитными материалами Голова и шея. Российский журнал = Head and neck. Russian Journal. 2020;8(1):22–31
Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
Objective: to evaluate clinical cases with the usage of individual endoprostheses made of biocompatible composite materials based on hydroxyapatite and methyl methacrylate using computer modeling and subsequent manufacturing for reconstruction of the facial skeleton.
Material and methods. To create a 3-dimensional model of a bone defect, computed tomography (CT) is used. The obtained DICOM data is converted into stereolithography files using an algorithm for creating individual implants. After that the model is printed on a stereolithographic printer. Hydroxylapatite – HAP-99g was used to make the implant; the resulting model is released from the molds and sterilized.
Results and discussion.
In the cases enrolled in this research work, the post-traumatic defects of the upper jaw, lower orbital margin on the left and upper jaw on the left were corrected. Conclusion. The use of HAP-based composite materials to replace bone defects in the skull allows to significantly improve the effectiveness of treatment and the quality of rehabilitation of this complex category of patients. Key words: bone defects, Hydroxylapatite — HAP-99
Conflicts of interest. The authors have no conflicts of interest to declare.
Funding. This work was financially supported by the Ministry of Education and Science of the Russian Federation, a subsidy for the implementation of complex projects for the creation of high-tech manufacturing as part of the implementation of the Statement of the Government of the Russian Federation dated April 9, 2010 No. 218, stage 8 on the topic “Creation of high-tech digital manufacturing of precision metal complexes for implantation based on additive technologies”, agreement number 03.G25.31.0234 dated 03.03.2017
For citation: Reshetov I.V., Gaponov M.E., Svyatoslavov D.S., Bogoslovsky S.G. Reconstruction of the face middle zone defects with composite materials. Head and neck. Russian Journal. 2020;8(1):22–31 (in Russian).
The authors are responsible for the originality of the data presented and the possibility of publishing illustrative material – tables, figures, photographs of patients.
Введение
Злокачественные опухоли, травмы, ранения челюстно-лицевой области как в нашей стране, так и за рубежом приводят к увеличению потребности в специализированной помощи при устранении протяженных дефектов костей лицевого черепа [1–4]. Несмотря на то что выбор метода реконструкции зависит от самого дефекта, нет универсального стандартного метода реконструкции лицевого отдела черепа. Анатомия средней зоны лица достаточно сложна и относительно постоянна, даже незначительные изменения в анатомических ориентирах могут приводить к формированию дефекта, меняющего конфигурацию лица и приносящего тяжелые страдания человеку. Сами дефекты могут варьироваться от «небольших» – ороантральное или ороназальное сообщение, – которые приводят к затруднению жевания, гнусавости, попаданию пищи в полость носа, до «обширных», которые встречаются у 60% пациентов, оперированных по поводу злокачественных новообразований, поражающих среднюю зону лица. [5] Сочетание сложной анатомии и нарушение жизненно важных функций, таких как дыхание, жевание, зрение, снижение качества жизни пациента, делают реконструкцию средней зоны лица сложной задачей с практической точки зрения и до сих пор остаются вызовом для хирургов [6–9].
Синтетические материалы по сравнению с костными трансплантатами обладают рядом преимуществ: возможность получения неограниченных по размеру (объему) количества материала без оперативного вмешательства: забор костного материала и, как следствие, развитие послеоперационных осложнений: повреждение сосудов и нервов, образование гематом, развитие инфекционно-воспалительного процесса; отсутствие риска передачи от донора к реципиенту различных заболеваний бактериальной или вирусной этиологии, возможность развития реакции гистонесовместимости и хронического гранулематозного воспаления. Это заставляет искать альтернативные способы реконструкции лицевого скелета для достижения функционального и хорошего внешнего результата, приемлемого для пациента [10]. Благодаря развитию компьютерных и лазерных технологий, начиная с 2000-х гг. стало возможным получение твердых копий трехмерных образов, созданных с помощью 3D-печати [11]. Эти технологии были объединены под названием метода быстрого прототипирования. К настоящему времени основным методом создания полимерных копий компьютерных образов служит лазерная стереолитография –технология послойного изготовления трехмерных объектов. Технологии 3D-моделирования на основе данных компьютерной томографии (КТ) и быстрого прототипирования позволяют изготовить индивидуальный эндопротез, повторяющий естественную анатомию, утраченную в следствие заболевания, и восполнить дефект, обеспечивая как биомеханический, так и визуальный результат [12–13].
Материал и методы
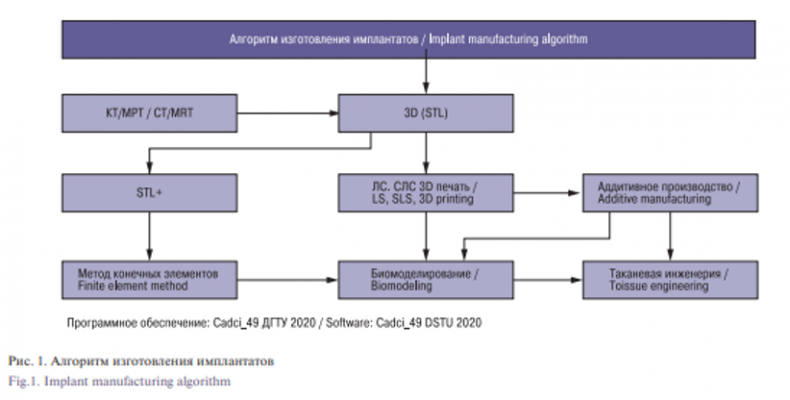
Важнейшую роль в создании 3-мерной модели костного дефекта играет КТ, в результате которой полученные данные DICOM преобразуются в файлы стереолитографии. Нами был разработан алгоритм создания индивидуальных имплантатов. На этапе преобразования информации осуществляются: 1) определение порогов плотностей – фильтрация шумовой составляющей делается автоматически, возможно добавление бара/ бегунка для ручной корректировки; 2) примерное выделение объекта, с которым необходимо работать – выделяется вручную оператором; 3) удаление артефактов, вызванных неточным восстановлением (автоматизировано, выполняется по 3D); 4) реконструкция дефектных областей; 5) сглаживание полученной модели (устранение углов и мелких дефектов, автоматически); 6) определение области повреждения (автоматизировано, предположительно с использованием универсальной модели/шаблона или в ручную задается оператором); 7) подбор имплантата из имеющихся шаблонов с одновременным выполнением условия максимального приближения к шаблону (в случае наличия симметричного объекта, то совпадения с ним) и совпадению масштабов с областью, помеченной как неповрежденная (выполняется автоматически, и вручную); 8) проверка условия наложения, полученного имплантата с общей моделью и информирование в случае пересечения с объектами такой же плотностью; 9) преобразование полученной модели в файл формата CAD с последующим преобразованием файла в объект печати (драйвера принтера) и 10) Печать объекта (рис. 1).
После создания в «цифре» модели имплантата – его техническое задание передается на стереолитографический принтер ЛС-150 (рис. 2)
На стереолитографе ЛС-150 производится печать из полимера модели части черепа с наличием дефекта и также модели вновь созданного имплантата. Планирование и моделирование хирургического вмешательства по замещению костного дефекта черепа осуществляется с помощью ранее распечатанных на ЛС-150 моделей части черепа и имплантата. При этом следует подчеркнуть, что «подгонка» модели имплантата осуществляется на ранее распечатанной модели черепа с дефектом, таким образом, для достижения прецизионности могут быть внесены изменения в форму имплантата, при этом модель может быть распечатана несколько раз, пока не будет достигнут искомый вариант формы и объема, по достижении которого для имплантата изготавливаются «пресс-формы», которые также распечатываются на стереолитографе ЛС-150. Для изготовления имплантата мы использовали Гидроксилапатит – ГАП-99 г в виде гранул размером 0,25–2 мм. Гидроксиапатит (ГАП) 1 мм 1 г партия 28021716 и ГАП 2 мм 1 г партия 28021717, производитель ООО «Полистом»; ГАП 99 г смешивают с метилметакрилатом – костный цемент CMW 3/40 с гентамицином. Полученную смесь хирургическим инструментом вносили в ранее напечатанные пресс-формы имплантата. Затвердение костного цемента средней вязкости при температуре в помещении 23 °С должно происходить за 80 секунд при условии, что на смешивание тратится 40 секунд, время ожидания составляет 95 секунд, а рабочее время не превышает 325 секунд. Общее время от начала перемешивания порошкового и жидкого костного цемента до полного затвердения не должно превышать 540 секунд при указанной выше температуре. Полученная модель высвобождается из пресс-форм и подвергается стерилизации в сухожаровом шкафу при температуре 180 °C не менее 20 минут.
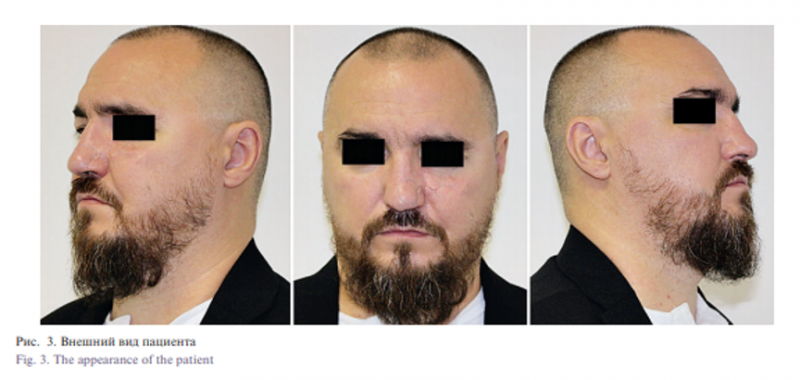
Пациент Б. 48 лет, поступил в клинику с диагнозом: посттравматический дефект верхней челюсти и нижнего орбитального края слева. Состояние после хирургического лечения (рис. 3).
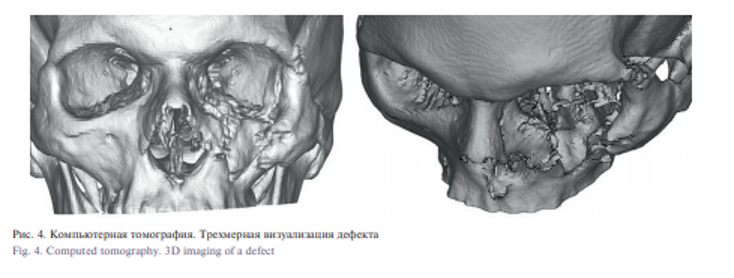
Из анамнеза: в 2017 г. была получена производственная травма, проведено хирургическое лечение по месту жительства, дальнейшее лечение не проводилось. При осмотре отмечено нарушение конфигурации лица, западение мягких тканей средней зоны лица слева из-за отсутствия костной основы верхней челюсти слева и орбитального края. Деформированы и рубцово изменены подглазничная и щечная области. Отмечается энофтальм и птоз главного яблока. По данным КТ определяется дефект передней стенки верхней челюсти, нижнеглазничного края и дна орбиты.
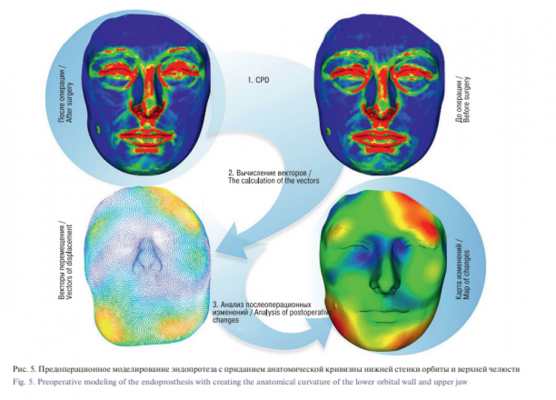
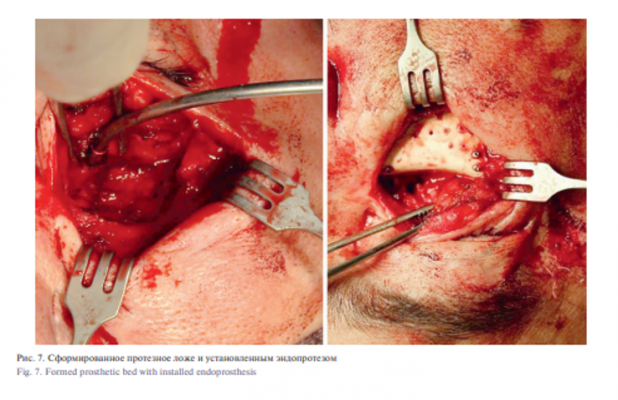
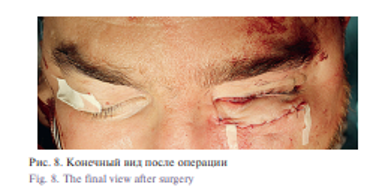
Под эндотрахеальным наркозом проведена операция: устранение дефекта передней стенки верхней челюсти и нижнего края орбиты индивидуальным эндопротезом. В ходе операции было сформировано протезное ложе с последующей постановкой и фиксацией индивидуального протеза микровинтами в области верхней челюсти и скуловой кости. Восстановлена передняя стенка верхней челюсти, нижнеглазничный край и устранен энофтальм. Послеоперационный период протекал без особенностей, рана зажила первичным натяжением.
Пациенту рекомендована повторная явка в клинику через 1, 3, 6 месяцев после операции и динамическое наблюдение.
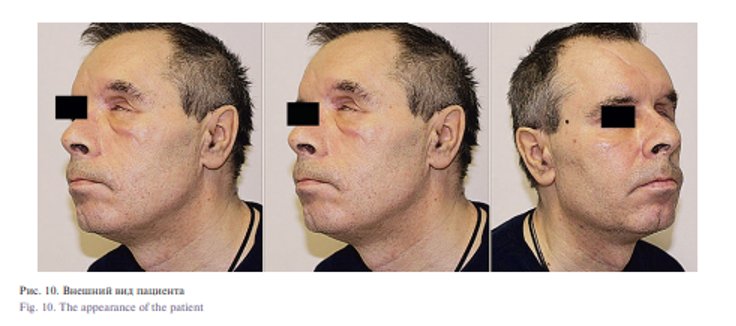
Пациент Г. 51 год, поступил в клинику с диагнозом: дефект верхней челюсти слева. Злокачественное новообразование левой глазницы (рис. 10).
Из анамнеза: в 2010 г. появилось слезотечения из левого глаза, по поводу чего за медицинской помощью не обращался. В 2012 г. отметил ухудшение клинической симптоматики слезотечения, обратился к окулисту по месту жительства, рекомендовано динамическое наблюдение, консервативная терапия, оперативное вмешательство по поводу восстановления проходимости левого носослезного канала.
В 2013 г. выполнена эндоскопическая операция по поводу восстановления проходимости левого носослезного канала. В течение последующего года наблюдалось улучшение, однако в 2014 г. на фоне перенесенного воспалительного заболевания носа и околоносовых пазух отметил отечность век, интенсивное слезотечение, появление гнойного отделяемого из носа. В апреле 2015 г. отметил выбухание конъюнктивы в области медиального угла левого глаза, со временем участок конъюнктивы увеличивался в размерах появилось округлое образование, оттесняющее глазное яблоко, появилась диплопия, в связи с чем обратился к онкологу по месту жительства. В сентябре 2015 г. выполнено КТ и МРТ-исследование черепа, выявлена опухоль носослезного канала. В НИИ нейрохирургии им. Н.Н. Бурденко было выполнено эндоскопическое эндоназальное удаление опухоли решетчатого лабиринта, ревизия левой гайморовой пазухи. По результатам послеоперационного гистологического исследования: краниофациальный плоскоклеточный рак в области лабиринта решетчатой кости слева с распространением в левую орбиту ТзNхМо. Пересмотр блоков и стекол в ФБГУ «РОНЦ им Н.Н. Блохина»: в готовых препаратах кусочков опухоли – переходноклеточный рак. В октябре 2016 г. выполнено удаление новообразования левой глазницы, пластика дефекта местными тканями. Течение послеоперационного периода протекало без осложнений.
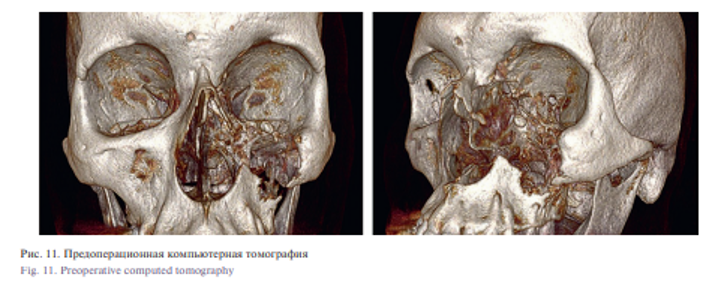
При осмотре отмечено нарушение конфигурации лица, уплощение мягких тканей средней зоны лица в левой скуловой, подглазничных щечной областях. Отмечалось опущение глазного яблока, послеоперационный рубец в подглазничной области слева. По данным КТ отмечался обширный дефект тела верхней челюсти, носовой и скуловой костей, отсутствие нижней стенки орбиты.
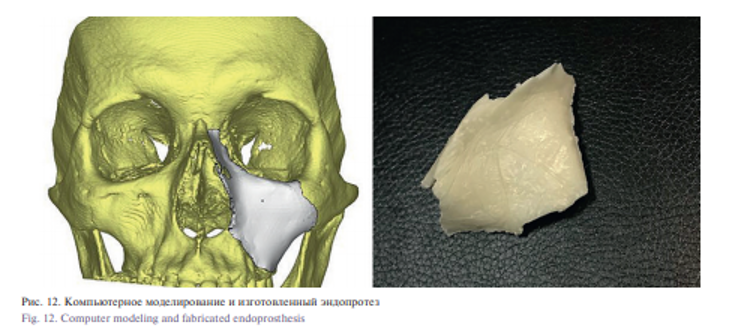
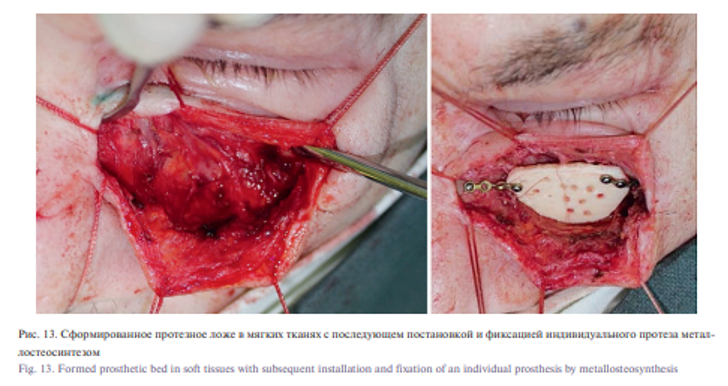
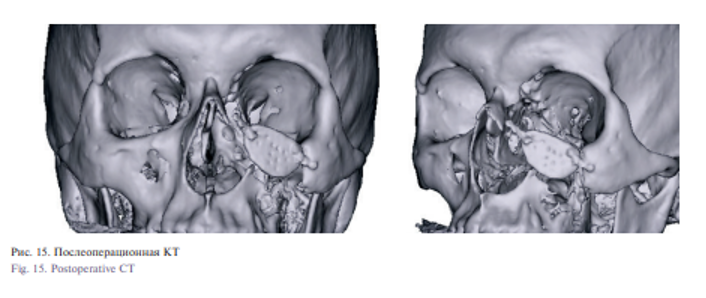
Под эндотрахеальным наркозом проведена операция: устранение дефекта передней стенки верхней челюсти и нижнего края орбиты индивидуальным эндопротезом. В ходе операции было сформировано протезное ложе в мягких тканях, вследствие обширного дефекта тела верхней челюсти и недостаточного объема мягких тканей для укрытия эндоротеза, было принято решение перемоделировать эндопротез с последующей постановкой и фиксацией в области верхней челюсти и скуловой кости металлоостеосинтезем. Была восстановлена передняя стенка верхней челюсти и анатомическая кривизна подглазничной области. Послеоперационный период протекал без особенностей, рана зажила первичным натяжением. Пациенту рекомендована повторная явка в клинику через 1, 3, 6 месяцев после операции. Пациент находится на динамическом наблюдении.
Обсуждение
Сегодня на помощь хирургу приходят новые технологии на основе быстрого прототипирования. Использование и разработка новых методик прототипирования является актуальным для устранения дефектов и является важным аспектом в системе оказания специализированной помощи. Есть несколько преимуществ данной методики: предоперационная модель позволяет хирургу планировать резекцию и реконструкцию до операции. Одноэтапная реконструкция сокращает время на работу и уменьшает болезненность. Индивидуальный эндопротез позволяет точно восстанавливать сложные трехмерные структуры резецированной кости с минимальными корректировками и позиционирования.
Заключение
Использование индивидуально изготовленного эндопротеза приводит к адекватной реконструкции анатомически сложной области, восстановлению функции опорных структур и хорошим внешним результатам. Использование данного метода может быть предпочтительным, особенно когда резецированная область маленькая и не включает в себя бо`льшую часть орбитальных стенок. Кроме того, эндопротезы из композита на основе гидроксиапатита и метилметакрилата хорошо переносятся, биосовместимы, не обладают алогическими свойствами, и данная техника является перспективным вариантом для реконструкции средней зоны лица вследствие резекции или травмы.
ЛИТЕРАТУРА
- Асиятилов А.Х., Ордашев Х.А., Шахбанова А.К., Минкаилова С.Р. Особенности травматизма челюстно-лицевой области в Республике Дагестан. В кн.: Актуальные вопросы челюстно-лицевой хирургии и стоматологии: Сборник научных трудов. СПб., 2004. С. 15–6.
- Грачев И.Ф. Оптимизация планирования ортопедической стоматологической помощи больным с челюстно-лицевыми дефектами в современных условиях (на примере Орловской области). Дисс. канд. мед. наук. М., 2008.
- Макаревич А.А. Качество жизни челюстно-лицевых онкологических больных после ортопедической стоматологической реабилитации: ). Дисс. канд. мед. наук. М., 2009.
- Кравцов Д.В. Клинико-микробиологическое обоснование и оценка эффективности применения зубочелюстных протезов-обтураторов из различных конструкционных материалов: ). Дисс. канд. мед. наук. М., 2012.
- Поляков А.П. Микрохирургическая реконструкция лицевого скелета костными аутотрансплантатами у онкологических больных. Дисс. докт. мед. наук, М., 2017.
- Scolozzi P., Martinez A., Jaques B. Complex orbito-fronto-temporal reconstruction using computer-designed PEEK implant. J. Craniofac. Surg. 2007;18:224–8.
- Eppley B.L., Kilgo M., Colleman J.J. III: Cranial reconstruction with computergenerated hard tissue replacement patient-matched implants: Indications, surgical technique and long term follow up. Plast. Reconstr. Surg. 2002;109–864.
- Spetzger U., Vougioukas V., Schipper J. Materials and techniques for osseous skull reconstruction. Minim Invasive Ther. Allied. Technol. 2010;19:110.
- Futran N.D., Mendez E. Developments in reconstruction of midface and maxilla. Lancet. Oncol. 2006;7:249–58.
- Gerbino G., Bianchi F.A., Zavattero E., Tartara F., Garbossa D., Ducati A. Single-step resection and reconstruction using patient-specific implants in the treatment of benign cranio-orbital tumors. J. Oral Maxillofac. Surg. 2013;71(11).
- Ventola C.L. Medical Applications for 3D Printing: Current and Projected Uses. 2014;39(10):704–11.
- Рогинский В.В. и др. Разработка отечественной программы объемного компьютерного моделирования в краниофациальной хирургии. Материалы XI Международной конференции челюстно-лицевых хирургов и стоматологов. СПб., 2006. 162 с.
- Кулагин В.В. Стереолитография в медицинской промышленности. Новое в стоматологии. 2002;3:37–8.
Поступила 11.01.20 Принята в печать 25.01.20
REFERENCES
- Asiyatilov A.H., Ordashev H.A., Shakhbanova A.K., Minkailova S.R. Features of injuries of the maxillofacial region in the Republic of Dagestan. In the book: Actualnyie voprosy chelyustno-licevoi hirurgii i stomatologii: Collection of scientific papers. SPb., 2004. P. 15-16 (In Russ.).
- Grachev I.F. Optimization of planning the orthopedic dental care for patients with maxillofacial defects in modern conditions (in the example of the Oryol region). PhD thesis. M., 2008. (In Russ.).
- Makarevich A.A. Quality of life of maxillofacial oncological patients after orthopedic dental rehabilitation. PhD thesis. M., 2009 (In Russ.).
- Kravtsov D.V. Clinical and microbiological substantiation and assessment of the effectiveness of the use of dento-maxillary obturator prostheses from various structural materials. PhD thesis. M., 2012 (In Russ.).
- Polyakov A.P. Microsurgical reconstruction of the facial skeleton with bone autografts in cancer patients. Doctor of Medicine degree thesis, M., 2017 (In Russ.).
- Scolozzi P., Martinez A., Jaques B. Complex orbito-fronto-temporal reconstruction using computer-designed PEEK implant. J. Craniofac. Surg. 2007;18:224–8.
- Eppley B.L., Kilgo M., Colleman J.J. III: Cranial reconstruction with computergenerated hard tissue replacement patient-matched implants: Indications, surgical technique and long term follow up. Plast. Reconstr. Surg.2002;109–864.
- Spetzger U., Vougioukas V., Schipper J. Materials and techniques for osseous skull reconstruction. Minim Invasive Ther. Allied Technol. 2010;19:110.
- Futran N.D., Mendez E. Developments in reconstruction of midface and maxilla. Lancet. Oncol. 2006;7:249–58.
- Gerbino G., Bianchi F.A., Zavattero E., Tartara F., Garbossa D., Ducati A. Single-step resection and reconstruction using patient-specific implants in the treatment of benign cranio-orbital tumors. J. Oral Maxillofac. Surg. 2013;71(11).
- Ventola C.L. Medical Applications for 3D Printing: Current and Projected Uses. 2014;39(10):704–11.
- Roginsky V.V. et al. Development of a domestic volumetric computer modeling program in craniofacial surgery. Materials of the XI International Conference of Oral and Maxillofacial Surgeons and Dentists. St. Petersburg, 2006. 162 p. (In Russ.).
- Kulagin V.V. Stereolithography in the medical industry. Novoe v stomatologii. 2002; 3: 37–38 (In Russ.).
Received 11.01.20 Accepted 25.01.20
Вклад авторов: Решетов И.В – координатор проекта, редактор, концепция и дизайн исследования;
Гапонов М.Е. – выполнение оперативных вмешательств по имплантации внедрению опытных образцов в лабораторных животных;
Святославов Д.С. – анализ полученных данных, оценка результатов исследования, написание текста рукописи, редактирование;
Богословский С.Г – выполнение оперативных вмешательств по имплантации внедрению опытных образцов в лабораторных животных
Authors’ contributions. Reshetov I.V – project coordinator, editor, research concept and design;
Gaponov M.E. – performing of the surgical interventions for the introduction of prototypes in laboratory animals;
Svyatoslavov D.S. – analysis of the data obtained, assessment of the results of the study, writing the text of the manuscript, editing;
Bogoslovsky S.G. – performing of the surgical interventions on the introduction of prototypes in laboratory animals
Информация об авторах:
И.В. Решетов – д.м.н., профессор, академик РАН, директор НОКЦ пластической хирургии, заведующий кафедрой онкологии, радиотерапии и пластической хирургии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава РФ (Сеченовский университет), Академия постдипломного образования ФГБУ ФНКЦ ФМБА России, Москва; e-mail: reshetoviv@mail. ru. https://orcid.org/0000-0002-0909-6278
М.Е. Гапонов – врач челюстно-лицевой хирург отделения реконструктивнопластической хирургии УКБ № 1 ФГОАУ ВО Первый МГМУ им. И.М. Сеченова (Сеченовский университет), Москва, Россия; e-mail: mihailmsi@ gmail.com
Д.С. Святославов – к.м.н., врач-онколог онкологического хирургического отделения комбинированных методов лечения УКБ № 1, доцент кафедры онкологии, радиотерапии и пластической хирургии ФГОАУ ВО Первый МГМУ им. И.М. Сеченова (Сеченовский университет), научный сотрудник лаборатории биоинжиниринга и прототипирования органов и тканей института регенеративной медицины Сеченовского университета, Москва, Россия; e-mail: dssvyatoslavov78@mail.ru. orcid.org/0000-0003- 0898-8693
С.Г. Богословский – аспирант кафедры онкологии, радиотерапии и пластической хирургии ФГАОУ ВО Первый МГМУ им. И.М. Сеченова Минздрава РФ (Сеченовский университет), Москва, Россия
Information about the authors:
I.V. Reshetov – Doctor of Medicine, Professor, Academician of the Russian Academy of Sciences, Director of the Scientific and Educational Clinical Center for Plastic Surgery, Head of the Department of Oncology, Radiotherapy and Plastic Surgery, FSAEI HE First Moscow State Medical University n.a. I.M. Sechenov of the Ministry of Health of the Russian Federation (Sechenov University), Academy of Postgraduate Education FSBI FSCC FMBA of Russia, Moscow; e-mail: reshetoviv@mail.ru. https://orcid.org/0000-0002-0909-6278
M.E. Gaponov – maxillofacial surgeon, Department of Reconstructive Plastic Surgery, UCH No. 1 FSAEI HE First Moscow State Medical University n.a. I.M. Sechenov of the Ministry of Health of the Russian Federation (Sechenov University), Moscow, Russia; e-mail: mihailmsi@gmail.com
D.S. Svyatoslavov – PhD, oncologist of the Oncological Surgical Department of Combined Methods of Treatment at the University Clinical Hospital No. 1, associate professor of the Department of Oncology, Radiotherapy and Plastic Surgery, FSAEI HE First Moscow State Medical University n.a. I.M. Sechenov of the Ministry of Health of the Russian Federation (Sechenov University), Researcher, Laboratory for Bioengineering and Prototyping of Organ and Tissue, Institute of Regenerative Medicine, Sechenov University, Moscow, Russia; e-mail: dssvyatoslavov78@mail.ru. orcid.org/0000-0003-0898-8693
S.G. Bogoslovsky – PhD student of the Department of Oncology, Radiotherapy and Plastic Surgery of the FSAEI HE First Moscow State Medical University n.a. I.M. Sechenov of the Ministry of Health of the Russian Federation (Sechenov University), Moscow, Russia
Рецензия на статью
Статья посвящена оценке клинических случаев восстановления анатомии, функции и эстетики средней зоны лица с применением индивидуальных эндопротезов изготовленных из биосовместимых композитных материалов с использованием компьютерного моделирования. Актуальность статьи не вызывает сомнения, поскольку проблема реконструкции средней зоны лица относится к разряду социально значимых и требует совместного внимания челюстно-лицевых хирургов, ЛОР-врачей, офтальмологов. Применение индивидуальных эндопротезов может существенно сократить время операции и повысить эффективность проводимого лечения. Авторами проведена серьезная работа по предоперационной подготовке пациентов с дефектами и деформациями средней зоны лица, включавшая мультидисциплинарное клиническое обследование и компьютерную томографию с последующим виртуальным планированием индивидуальных эндопротезов для восстановления нормальной анатомии и функциональности средней зоны лица.
Review on the article
The article is devoted to the evaluation of clinical cases of restoration of the anatomy, function and aesthetics of the middle zone of the face using individual endoprostheses made of biocompatible composite materials using computer simulation. The relevance of the article is not in doubt, since the problem of reconstruction of the middle zone of the face belongs to the category of socially significant ones and requires the joint attention of maxillofacial surgeons, ENT doctors, ophthalmologists. The use of individual endoprostheses can significantly reduce the time of surgery and increase the effectiveness of the treatment. The authors carried out serious work on the preoperative preparation of patients with defects and deformations of the middle zone of the face, including multidisciplinary clinical examination and computed tomography followed by virtual planning of individual endoprostheses to restore normal anatomy and functionality of the middle zone of the face.