Для цитирования: Комелягин Д.Ю., Петухов А.В., Иванов А.В., Фокин Е.И., Фокина Т.В., Дубин С.А., Владимиров Ф.И., Яматина С.В., Хаспеков Д.В., Пасечников А.В., Вафина Х.Я. Лечение ребенка с обширной лимфовенозной мальформацией в области головы и шеи. Голова и шея Head and neck Russian Journal. 2019;7(1):29–41
For citation: Komelyagin D.Yu., Petukhov A.V., Ivanov A.V., Fokin E.I., Fokina T.V., Dubin S.A., Vladimirov F.I., Yamatina S.V., Khaspekov D.V., Pasechnikov A.V., Vafina H.Y. Treatment of a child with extensive lymphovenous malformation in the head and neck area. Head and neck Russian Journal. 2019;7(1):29–41 (in Russian).
Doi: 10.25792/HN.2019.7.1.29–41
Обширные лимфатические и лимфовенозные мальформации головы и шеи у детей являются тяжелыми пороками развития лимфатических и венозных сосудов. Существует ряд важных нерешенных вопросов по лечению больных данной патологией, на которые современная медицинская литература не дает ответов в полном объеме: когда, как и в каком объеме удалять патологические ткани. В статье приведен клинический пример лечения ребенка с обширной диффузной формой лимфовенозной мальформации правой половины головы и шеи.
Ключевые слова: лимфатическая мальформация, лимфовенозная мальформация, склерозирующая терапия, лимфангиома, гемлимфангиома, хирургическое лечение мальформаций
Авторы заявляют об отсутствии конфликта интересов.
Источник финансирования. Не указан.
Для цитирования: Комелягин Д.Ю., Петухов А.В., Иванов А.В., Фокин Е.И., Фокина Т.В., Дубин С.А., Владимиров Ф.И., Яматина С.В., Хаспеков Д.В., Пасечников А.В., Вафина Х.Я. Лечение ребенка с обширной лимфовенозной мальформацией в области головы и шеи. Голова и шея Head and neck Russian Journal. 2019;7(1):29–41
Авторы несут ответственность за оригинальность представленных данных и возможность публикации иллюстративного материала – таблиц, рисунков, фотографий пациентов.
Extensive lymphatic and lymphovenous malformations of the head and neck in children are usually the severe hereditary abnormalities of lymphatic and venous vessels. There is a number of important questions concerning such patients’ treatment, which, however, have no full answers in the modern medical literature: when and how widely the abnormal tissues should be remove. The authors present a clinical example of treating a child with an extensive diffuse lymphovenous malformation of the right head and neck part.
Key word: lymphatic malformation, lymphovenous malformation, sclerosing therapy (sclerotherapy), lymphangioma, gemlymphangioma, surgical treatment of malformations, children.
The authors declare no conflict of interest.
Source of financing: not specified.
For citation: Komelyagin D.Yu., Petukhov A.V., Ivanov A.V., Fokin E.I., Fokina T.V., Dubin S.A., Vladimirov F.I., Yamatina S.V., Khaspekov D.V., Pasechnikov A.V., Vafina H.Y. Treatment of a child with extensive lymphovenous malformation in the head and neck area. Head and neck Russian Journal. 2019;7(1):29–41 (in Russian).
The authors are responsible for the originality of the data presented and the possibility of publishing illustrative material – tables, figures, photographs of patients.
Введение
Обширные лимфатические и лимфовенозные мальформации головы и шеи у детей являются тяжелыми пороками развития лимфатических и венозных сосудов. Тяжесть патологии обусловлена тотальным поражением тканей от кожи и подкожной жировой клетчатки до костей с формированием грубых деформаций последних. Порочные ткани могут занимать любые области головы и шеи. Данные образования могут приводить к резкому ограничению функций дыхания, зрения, приема пищи и речи. При локализации мальформации в области гортаноглотки, дна полости рта и языка существует высокий риск развития состояний, угрожающих жизни ребенка. Обширные лимфатические и лимфовенозные мальформации являются причиной обезображивания внешнего вида пациента, что отрицательно влияет на его психоэмоциональный статус. Все это подтверждают слова академика Ю.Ф. Исакова [1], опубликованные в 1974 г.: «Пороки развития периферических кровеносных и лимфатических сосудов относятся к мало изученным разделам детской ангиологии. Многие вопросы этиологии, патогенеза, клиники, диагностики и лечения этих пороков остаются неясными и требуют дальнейшего исследования. Пороки развития периферических сосудов являются тяжелыми врожденными заболеваниями. Возникая с рождением ребенка, они прогрессируют, вызывают значительные функциональные и анатомические расстройства. Прогрессирующее течение этих пороков приводит к возникновению необратимых изменений в тканях пораженного органа, что затрудняет проведение больным радикального лечения. Своевременная диагностика и операция являются единственными способами профилактики этих нарушений. Радикализм в хирургии пороков развития периферических сосудов находится в прямой зависимости от распространенности и локализации порока, степени вовлечения в процесс окружающих тканей». Все это ставит перед хирургом серьезные вопросы: когда, как и в каком объеме оперировать данного пациента.
На сегодняшний день доброкачественные образования из лимфатических сосудов по международной классификации болезней 10-го пересмотра (МКБ-10) носят название лимфангиома. Когда в патологическом образовании, которое клинически определяли, как лимфангиома, обнаруживали кровь, то оно носило название гемлимфангиома. В настоящее время в результате иммуногистохимических и генетических исследований доказано отсутствие маркеров опухоли у данных образований [2]. Для обозначения пороков развития лимфатических и кровеносных сосудов применяются термины мальформация или ангиодисплазия. Название сосудистая мальформация (vascular malformation) наиболее часто используется в американской литературе, тогда как европейское медицинское сообщество применяет термин ангиодисплазия (angiodysplasia). По классификации Международного общества по изучению сосудистых аномалий ISSVA (International Society for the Study of Vascular Anomalies) в редакции 2014 г. лимфатическая мальформация – это порок развития лимфатических сосудов, лимфовенозная мальформация – это комбинированный порок развития лимфатических и венозных сосудов.
В областях головы и шеи встречаются кистозные формы лимфатических мальформаций, которые подразделяются на мелкокистозные (при наличии полостей менее 1 см в диаметре), крупнокистозные (при наличии полостей более 1 см в диаметре) и смешанные (при наличии полостей разного диаметра) [3, 4].
По данным А.П. Малинина (1974) [5], лимфатические мальформации, занимающие одну или две смежные анатомические области, являются малораспространенными, а поражающие три и более – обширными. В зависимости от типа роста различают ограниченную и диффузную формы. Ограниченная мальформация имеет четко очерченные контуры и не прорастает в окружающие ткани. При диффузной форме патологические ткани локализуются в жировой клетчатке, мышцах, костях, фасциях, коже, слизистых оболочках, а в некоторых случаях – в близлежащих органах.
В связи с тем что в нашей стране статистика по заболеваниям ведется по номенклатуре МКБ-10, то статистические данные берутся по лимфангиомам. Лимфатическая мальформация составляет 6–18% от доброкачественных образований у детей [6, 7]. По данным J.L. Acevedo (2008) [8], заболеваемость лимфатическими мальформациями варьируется от 1:1000 до 1:16 000 среди новорожденных. Пороки развития лимфатических сосудов в области головы и шеи чаще всего определяются при рождении или в первые годы жизни ребенка. В возрасте до одного года образования диагностируются в 60–80% случаев [9–11]. В области головы и шеи мальформации встречаются в 50–75% случаев [12, 13]. По данным медицинской научной литературы, существует несколько основных методов лечения детей с обширными лимфатическими и лимфовенозными мальформациями в области головы и шеи. Их можно разделить на три группы: консервативные, хирургические и комбинированные. К консервативным методам относятся динамическое наблюдение, медикаментозное лечение, лучевая терапия. Хирургическими методами лечения являются традиционное хирургическое вмешательство [14–16], склерозирующая терапия [17–20], лазерная хирургия [21, 22], криохирургия [14, 23–25]. Комбинированный метод включает в себя сочетание тех или иных способов лечения. Такое число методов лечения говорит об отсутствии одного универсального метода лечения.
При анализе научных публикаций по теме лечения пациентов с данной патологией выявлены следующие нерешенные вопросы: в каком возрасте оперировать ребенка с обширным пороком лимфатических и венозных сосудов в области головы и шеи, в каком объеме удалять патологические ткани, какие методы лечения применять. Современная медицинская литература не дает ответов на поставленные вопросы в полном объеме.
Стоит отметить, что в зарубежных научных источниках имеются лишь единичные публикации по демонстрации полностью пролеченных детей с обширными формами лимфатических и лимфовенозных мальформаций в области головы и шеи. В них авторы указывают на возможности проведения тотального и субтотального удаления патологических тканей с получением хороших результатов лечения [26, 27]. В современной отечественной литературе таких данных мы не нашли.
В данной статье приведен пример лечения пациента с обширной диффузной лимфовенозной мальформацией в области головы и шеи, которому были выполнены все виды современных методов лечения.
Клинический пример
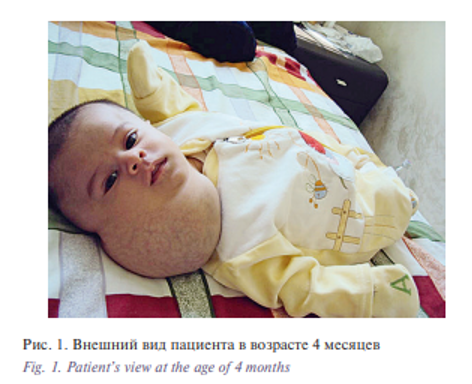
В 2014–2017 гг. в отделении челюстно-лицевой хирургии Российской детской городской клинической больницы святого Владимира, Москва (РДКБ) проводилось лечение пациента 4 лет (рост 98 см, масса тела 14 кг) из Иордании с диагнозом: обширная диффузная лимфовенозная мальформация лица, шеи, дна полости рта, глотки, языка (смешанная форма), сочетанная деформация челюстей; хроническое трахеальное канюленосительство, носитель гастростомы, задержка психоречевого развития. Стоит отметить, что ребенок родился у родителей из разных иорданских семей, у ближайших родственников врожденной сосудистой патологии не было. Из анамнеза известно, что в антенатальном периоде (6 месяцев, 23-я неделя беременности) при проведении ультразвукового исследования (УЗИ) у плода было выявлено объемное образование в области головы и шеи. Родителями было принято решение беременность не прерывать. Ребенок родился на 37-й неделе в результате оперативных родов (кесарево сечение) с объемным образованием в области головы и шеи справа. После проведения УЗИ, компьютерной томографии (КТ) и магнитно-резонансной томографии (МРТ) был установлен диагноз: обширная диффузная лимфатическая мальформация головы, шеи. В связи с выраженным нарушением дыхания пациенту была наложена трахеостома. Из-за невозможности приема пищи через рот ребенок находился на зондовом питании. В течение 1,5 месяца после рождения больному проводилась гормональная терапия (преднизолон) без положительного клинического эффекта. С целью уменьшения объема образования в 4 месяца (рис. 1) ребенку было проведено вскрытие, дренирование образования, получено и эвакуировано 200 мл серозно-геморрагической жидкости, однако через месяц вновь отмечалось увеличение объема патологических тканей.
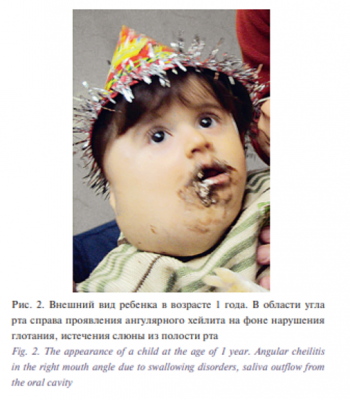
Далее в течение 3 лет проводилась склерозирующая терапия. Всего было выполнено 11 операций, которые были проведены по месту жительства в Иордании. В ходе лечения применялись следующие склерозирующие препараты: блеомицин (3 операции), доксициклин (1 операция), триамцинолон и дексаметазон (1 операция), кортизон (1 операция), пицибанил (ОК 432, 5 операций). На первом году жизни больной перенес аспирационную пневмонию. В возрасте 1 года 2 месяца ребенку была выполнена операция: открытая фундопликация по Ниссену (Nissen), гастростомия, а в 1 год 4 месяца (рис. 2) у пациента были удалены патологические ткани в области шеи справа.
Несмотря на все проведенные хирургические вмешательства у пациента сохранялись выраженная асимметрия лица и шеи за счет большого объема патологических тканей головы и шеи справа, макроглоссия. Ребенок дышал через трахеостому, питался через гастростому, не говорил (рис. 3 а, б). Больной был направлен в Россию для дальнейшего лечения.
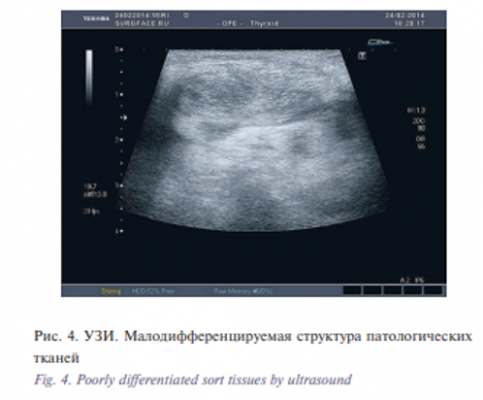
При поступлении в ДГКБ св. Владимира у пациента отмечалась выраженная деформация лица и шеи за счет большого массива патологических тканей, занимающих правую половину лица и шеи. Рот у ребенка был постоянно открыт, язык выступал из полости рта. Пациенту были проведены обследования: УЗИ (Toshiba Aplio MX), фиброларингоскопия (Olympus Exera II CLV 180), КТ с контрастированием (Toshiba Aquilion 16; Омнипак 350). При проведении УЗИ патологических тканей (рис. 4 а, б) последние были представлены малодифференцированной аваскулярной тканью, местами имеющей структуру мелких кист. Патологические ткани начинались от кожного покрова и продолжались до костей. Определить точные размеры образования с помощью УЗИ не представлялось возможным, т.к. линейные размеры мальформации во много раз были больше длины ультразвукового датчика. Во время проведения фиброларингоскопии в области гортаноглотки отмечалось выбухание правой стенки глотки. Патология структур гортани не выявлена.
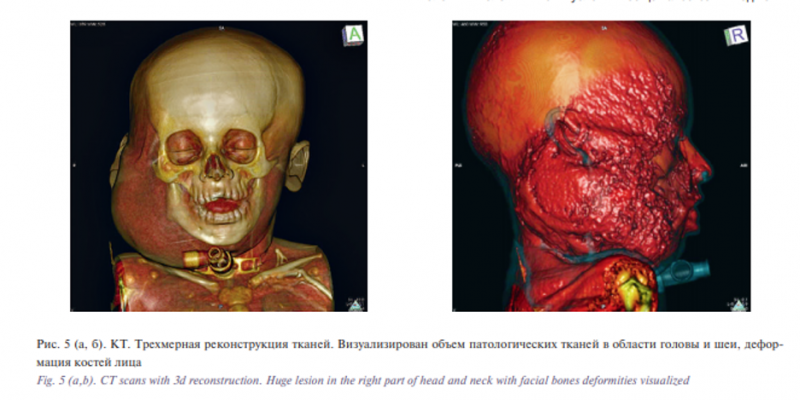
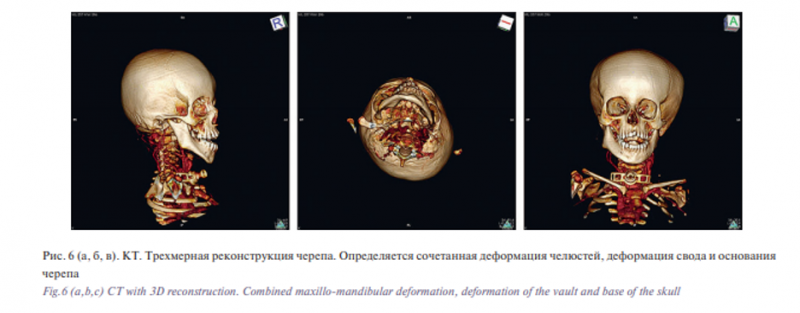
После проведения КТ с контрастированием сосудов были определены точные размеры и объем патологических тканей, их кровоснабжение, а также визуализирована деформация костей лицевого скелета. Порочные ткани располагались в околоушно-жевательной, височной, лобной, орбитальной, скуловой, подбородочной областях справа, поднижнечелюстной, подподбородочной областях справа, в окологлоточном пространстве и в области основания черепа, в области грудино-ключичнососцевидной мышцы, в височной, подвисочной и крылонебной ямках справа, в щечных областях, в области верхней и нижней губ, в области скатов носа (рис. 5).
Накопления контрастного препарата в патологических тканях выявлено не было. Деформация костей лица выражалась в следующем: сужение альвеолярных отростков верхних челюстей и альвеолярной части нижней челюсти, значительное увеличение ветви и тела нижней челюсти справа, вдавленная форма последних, вертикальная резцовая дизокклюзия (1,5 см). Также определялась деформация костей свода и основания черепа в виде асимметрии свода черепа за счет уплощения теменной и затылочной костей справа, увеличения правой нижнечелюстной ямки (рис. 6).
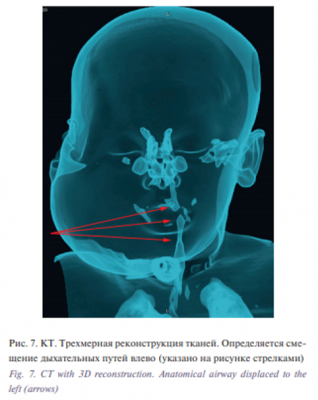
Верхние дыхательные пути были смещены влево за счет объема патологических тканей, которые располагались в окологлоточном пространстве (рис. 7). В данном клиническом случае МРТ не проводилась в связи с поломкой аппарата МРТ. Количество информации от вышеуказанных методов обследования для принятия решения о тактике лечения было достаточным. Больному был подтвержден диагноз: обширная диффузная лимфатическая мальформация головы и шеи, смешанная форма.
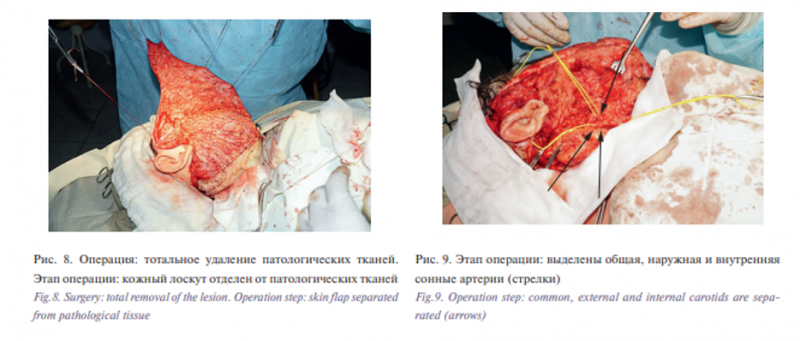
В связи с наличием большого объема патологических тканей, которые являлись причиной нарушения дыхания, самостоятельного приема пищи, а также выраженных косметических нарушений, в связи с отсутствием эффекта от малоинвазивных методов лечения больному были выставлены показания к хирургическому лечению. В возрасте 4 лет ребенку проведено тотальное удаление патологических тканей в области правой половины головы и шеи в условиях общей анестезии. Под комбинированным эндотрахеальным наркозом (севоран) из модифицированного разреза по Г.П. Ковтуновичу был сформирован кожный лоскут в височной, околоушно-жевательной, щечной и поднижнечелюстной областях (рис. 8).
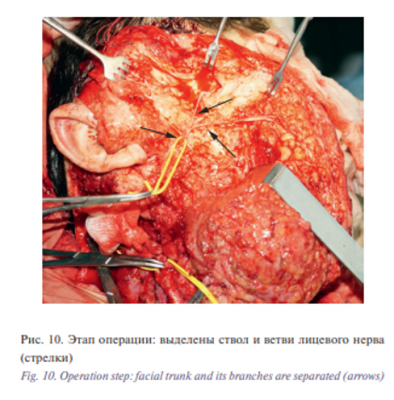
Выделение патологических тканей проводилось единым массивом. Околоушная и поднижнечелюстная слюнные железы не дифференцировались. В ходе операции были обнажены и сохранены общая, наружная и внутренняя сонные артерии, внутренняя яремная вена (рис. 9), с которыми были интимно спаяны ткани мальформации до входа и выхода сосудов из основания черепа. Из конгломерата удаляемых тканей хрящевой плотности с большими техническими трудностями были выделены и сохранены лицевой (рис. 10), языкоглоточный, блуждающий, добавочный, подъязычный нервы.
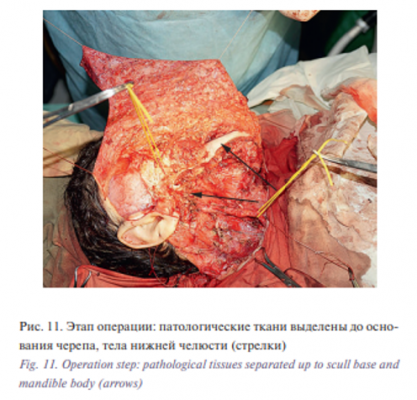
Патологические ткани также были интимно спаяны со слуховым проходом вплоть до наружного слухового отверстия, что потребовало кропотливого выделения последнего. Длительность операции составила 12 часов, кровопотеря – 400 мл. В ходе операции выявлены следующие особенности: патологические ткани имели хрящевую плотность из-за проведенной ранее склерозирующей терапии, располагались сразу под кожей и распространялись до костей лица и основания черепа, окутывая и смещая сосуды и нервы. В результате хирургического вмешательства все видимые глазу патологические ткани были удалены, рана ушита узловыми швами, установлены перчаточные дренажи (рис. 11).
Макропрепарат представлял собой малодифференцированную соединительную ткань с фрагментами мелких кист, которые были заполнены лимфой или лимфой с кровью (рис. 12).
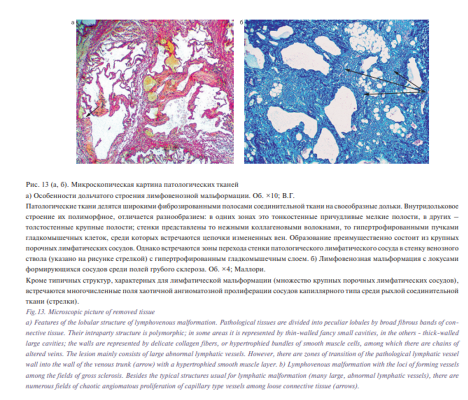
При патогистологическом исследовании было получено следующее описание удаленных тканей: в исследуемом материале множественные фрагменты соединительной ткани с включениями жировой ткани, большое количество лимфатических сосудов различных размеров и формы, разделенных перегородками разной толщины; поля склерозированной ткани с венами мелкого калибра; более крупные вены уродливой формы с утолщенными склерозированными стенками; имеются участки с расширенными полнокровными венозными сосудами с периваскулярными кровоизлияниями; встречаются дольки слюнных желез с расширенными выводными протоками. Заключение: порок развития лимфатических и венозных сосудов (рис. 13 а, б). На основании данного заключения больному был поставлен окончательный клинический диагноз: обширная диффузная лимфовенозная мальформация головы и шеи справа, смешанная форма.
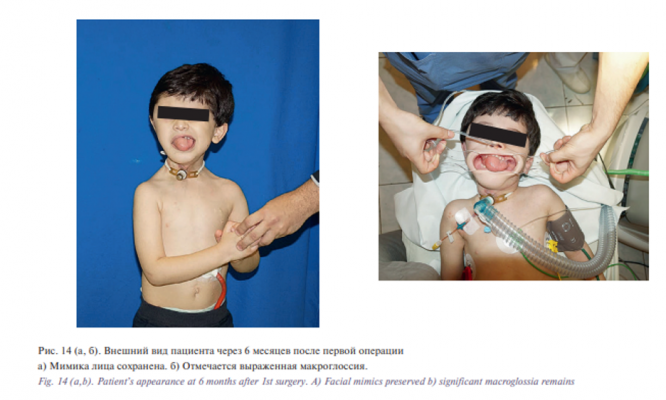
Послеоперационный период осложнился краевым некрозом кожного лоскута. Лимфореи не было. Рана зажила частично первичным натяжением. Вторичным натяжением заживление раны проходило в местах некроза лоскута. Швы сняты на 10-е сутки. Больной был выписан из отделения в удовлетворительном состоянии на 20-е сутки после операции. Трахеостома и гастростома были оставлены. При контрольном осмотре ребенка через 6 месяцев после операции жалоб у родителей на послеоперационную область не было, мимические мышцы функционировали в полном объеме. Однако у пациента отмечалась выраженная макроглоссия: язык не помещался в ротовой полости, выступая на 2 см (рис. 14).
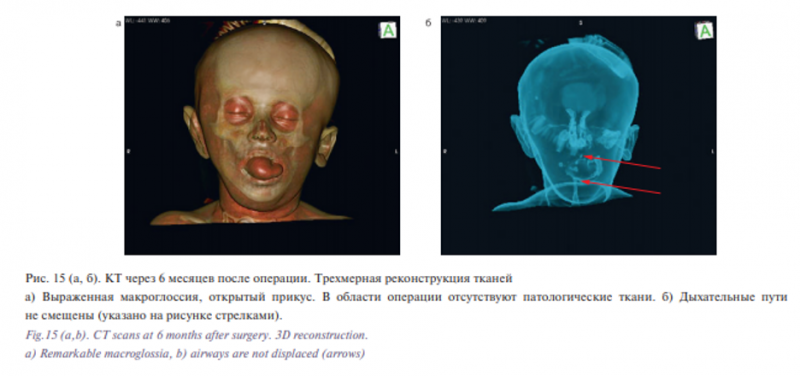
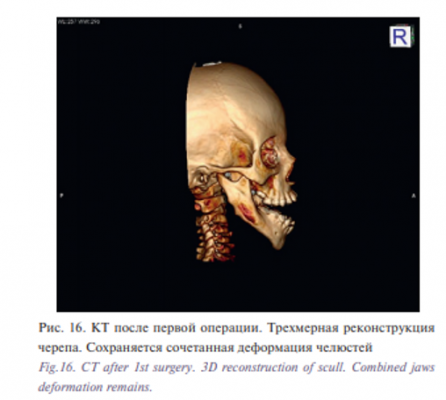
По данным контрольных КТ и УЗИ, патологических тканей в областях первой операции выявлено не были (рис. 15 а). Сохранялась сочетанная деформация челюстей, отмечалось увеличение вертикальной резцовой дизокклюзии (с 1,5 до 2,7 см) из-за выраженной макроглоссии (рис. 16). Смещения верхних дыхательных путей выявлено не было (рис. 15 б).
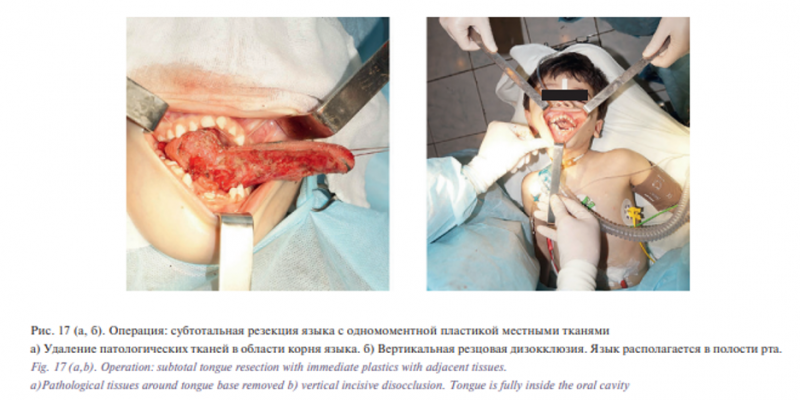
С целью уменьшения размеров языка и придания анатомической формы последнему больному была проведена субтотальная резекция языка с одномоментной пластикой местными тканями. В ходе операции язык был рассечен вдоль по средней линии на две половины до V-образно расположенных желобоватых сосочков, далее была иссечена правая, значительно увеличенная в размере часть языка, а также часть левой половины языка. При таком разрезе языка был получен доступ к патологическим тканям в области корня языка, которые представляли собой кисты разного диаметра, последние были удалены (рис. 17 а). В результате операции была сформирована анатомическая форма языка и он стал помещаться в полости рта (рис. 17 б). Послеоперационный период проходил без осложнений, рана зажила первичным натяжением, швы сняты на 14-е сутки.
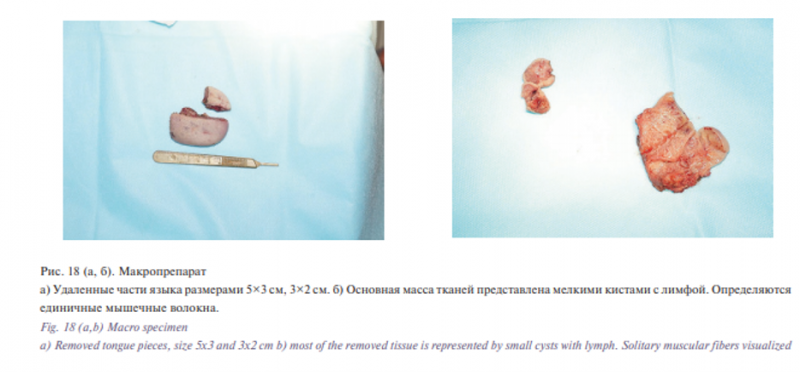
Удаленные ткани представляли собой конгломерат мелких кист, при вскрытии которых истекала лимфа. Поперечнополосатые мышцы языка были представлены единичными волокнами, расположенными между кистами (рис. 18).
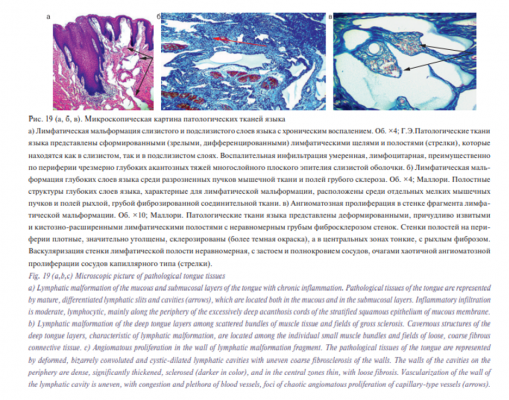
По результатам патогистологического исследования было получено следующее заключение: патологические ткани представлены сформированными (зрелыми, дифференцированными) лимфатическими щелями и полостями, стенки которых утолщены за счет повышенного фиброза, без гладкомышечных клеток. Ткани мальформации расположены местами очагово в толще слизистой оболочки, но преимущественно в широком подслизистом слое и среди мышечной ткани языка. Слизистая оболочка равномерно и диффузно гипертрофирована за счет акантозных разрастаний созревающего многослойного эпителия. Подслизистый слой чрезмерно широкий, в т.ч. из-за грубого фиброза. Также отмечается неравномерная васкуляризация стенок лимфатической полости с застоем и полнокровием последних, очагами хаотичной ангиоматозной пролиферации сосудов капиллярного типа (рис. 19 а, б, в).
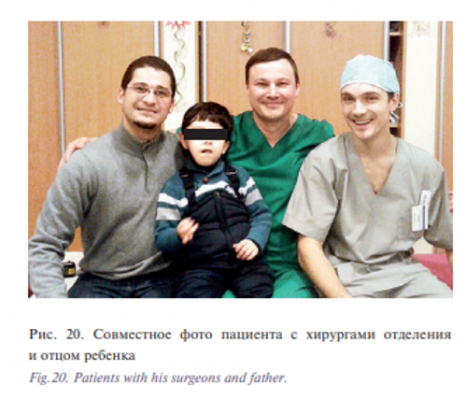
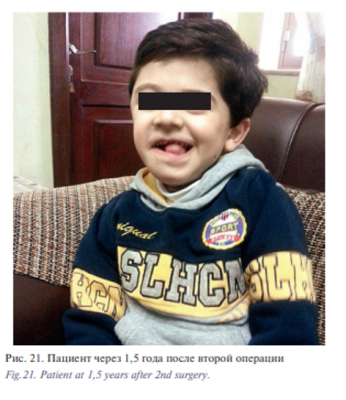
В связи с отсутствием нарушения самостоятельного дыхания, что было подтверждено данными контрольной фиброларингоскопии, на 14-е сутки после второй операции пациенту была проведена деканюляция. Несмотря на то что пациент начал самостоятельно питаться от закрытия гастростомы родители отказались. Ребенок был выписан из отделения с рекомендацией дальнейшего наблюдения в динамике. Закрытие гастростомы планировалось по месту жительства. При контрольном осмотре через 1,5 года после второй операции у ребенка симметрия лица не нарушена, патологические ткани в области правой половины головы и шеи не были выявлены, прикус нормализовался (вертикальная щель во фронтальном отделе уменьшилась), язык располагался в полости рта, мимические мышцы лица работали в полном объеме, пациент стал говорить (рис. 20, 21).
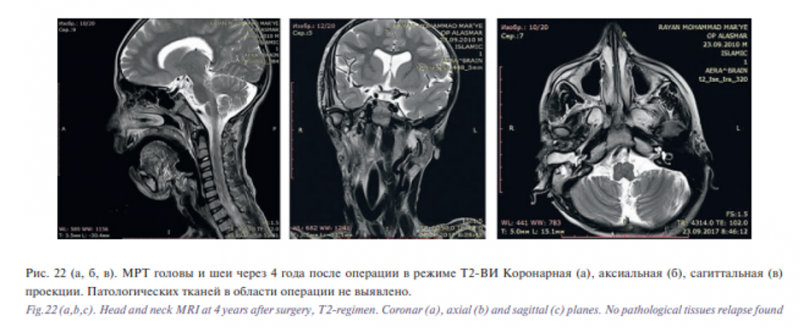
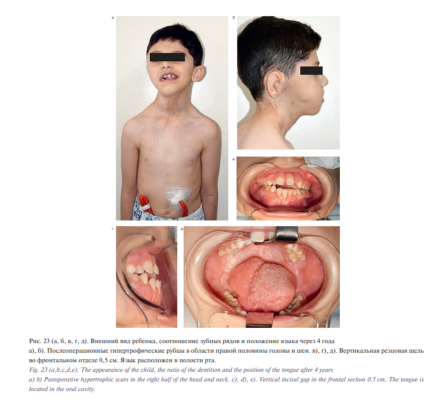
При поступлении в отделение через 4 года после первой операции больной продолжал находиться на питании через гастростому, несмотря на возможность самостоятельного приема пищи через рот. Конфигурация лица была асимметричной в связи с послеоперационной рубцовой деформацией тканей правой половины лица. Рубцы в области правой половины головы и шеи были гипертрофическими. Ортодонтическое лечение по месту жительства не проводилось. Однако смыкание зубных рядов стало более анатомически правильным. Вертикальная резцовая щель во фронтальном отделе значительно уменьшилась и составила 0,5 см. Язык полностью располагался в полости рта. Больному была проведена МРТ головы и шеи в режимах Т2-ВИ, Т1-ВИ (Т1-ВИ, Т2-ВИ – режимы МРТ: Т1-взвешенное изображение, Т2-взвешенное изображение). Патологических тканей в области первой операции не выявлено (рис. 22).
Верхняя и нижняя поверхности языка местами были покрыты мелкими пузырьками (до 0,2 см в диаметре) с прозрачным или с геморрагическим содержимым, которые являлись проявлением мелкокистозной формы лимфовенозной мальформации (рис. 23).
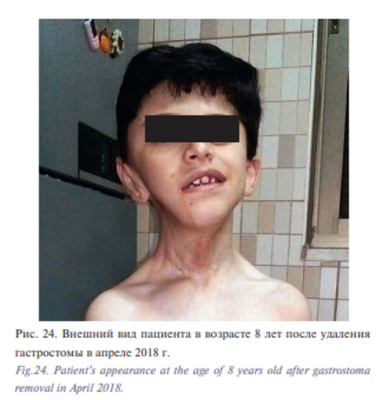
Данные элементы были удалены с помощью полупроводникового лазера IRE-Polus (режим непрерывный импульсный, длина волны 0,97 мкм, мощность 1–5 Вт) в условиях общей анестезии. После этой операции по месту жительства больному в возрасте 7 лет была удалена гастростома, ребенок стал самостоятельно питаться (рис. 24). В результате этапного хирургического лечения были достигнуты хорошие функциональный и косметический результаты: восстановлены самостоятельное дыхание, нормальная конфигурация лица, сохранены функции мимической мускулатуры, языка, полностью сохранен глотательный рефлекс, устранена макроглоссия, созданы условия для самостоятельного приема пищи и воды.
Заключение
Приведенный в статье клинический случай, во-первых, подчеркивает особенность данной патологии, при которой патологические ткани тотально поражают все ткани: кожу, подкожную жировую клетчатку, слизистые оболочки, мышцы, кости.
Во-вторых, патогистологическое исследование подтвердило наличие лимфовенозной мальформации как порока развития и лимфатических, и венозных сосудов. В-третьих, описанный клинический случай демонстрирует развитие выраженного рубцового процесса в патологических тканях после склерозирующей терапии, что значительно осложнило последующее хирургическое лечение. Отдельно стоит указать на отсутствие эффекта от проведенного многоэтапного малоинвазивного лечения (склерозирующей терапии). В-четвертых, этот пример демонстрирует невозможность излечения детей с обширной смешанной формой мальформации с применением только метода склерозирующей терапии. В сложных клинических случаях именно тотальное удаление патологических тканей может привести к положительному клиническому результату лечения. Отдельно стоит остановиться на вопросе социализации пациентов такой группы. А именно, можно отметить, что в результате длительного многоэтапного хирургического лечения ребенок стал социально адаптированным: научился самостоятельно дышать и есть, общаться и играть со сверстниками.
ЛИТЕРАТУРА
- Исаков Ю.Ф., Тихонов Ю.А. Врожденные пороки периферических сосудов у детей. М., 1974. 116 с.
- North P.E. Pediatric vascular tumors and malformations. Surgical pathology. 2010;3:455–94.
- Ravitch M.M., Rush Jr. B.F. In: Welch K.J., Randolph M. M., Ravitch M. M., et al. Cystic hygroma. Pediatric surgery. Chicago (III) 7 Year Book Medical. 1986. P. 533–9.
- Ogita S., Tsuno T., Deguchi E., et al. OK-432 therapy for unresectable lymphangioma in children. J. Pediatr. Surg. 1991;26:263–70.
- Малинин А.П. Лечение подкожных лимфангиом у детей. Дисс. канд. мед. наук. Научно-исследовательский институт онкологии им. проф. Н.Н. Петрова, Ленинградский педиатрический медицинский институт. 1974.
- Исаков Ю.Ф., Долецкий С.Я. Детская хирургия. М., 1978. 502 с.
- Coffin C.M., Dehner L.P. Vascular tumors in children and adolescents: a clinicopathologic study of 228 tumors in 222 patients. Pathol. Ann. 1993;23(1):97–120.
- Acevedo J.L., Shah R.K., Brietzke S.E. Nonsurgical therapies for lymphangiomas: a systematic review. J. Otolaryngol. Head Neck Surg. 2008;138(4):418–24.
- Приходченко В.В. Лимфангиомы у детей (клиника, диагностика, лечение). Дис. канд. мед. наук. Донецк. 1986.
- Гургенадзе А.П. Совершенствование методов диагностики и лечения лимфангиом челюстно-лицевой области у детей. Дисс. канд. мед. наук. М., 1996.
- Копарзова О.А. Комплексное лечение вторичных деформаций мягких тканей и костей лицевого скелета у детей с различной локализацией лимфангиомы. Дисс. канд. мед. наук. М., 2005.
- Исаков Ю.Ф. Детская хирургия. М. 3-е изд., перераб. и доп.. 1983. 620 с.
- Enjolras O., Wassef M., Chapot R. Color atlas of vascular tumors and vascular malformations. New-York: Oxford uneversity press. 2007. Р. 3–11.
- Топольницкий О.З., Васильев А.Ю. Атлас по детской хирургической стоматологии и челюстно-лицевой хирургии: учеб. Пособие. М., 2011. 264 с.
- Рогинский В.В., Надточий А.Г., Овчинников И.А., Гавеля Е.Ю., Павелко Г.А., Бабиченко И.И., Ломака М.А., Рыжов Р.В. Мальформации лимфатической системы головы и шеи у детей: диагностика и методы лечения. Материалы VI съезда онкологов с международным участием. М., 2015. С. 324.
- Komelyagin D.Ju., Petukhov A.V., Ivanov A.V., Dubin S.A., Khaspekov D.V., Topilin O.G., Dergachenko A.V., Vladimirov F., Dergachenko An.V., Striga E.V., Slipenko V.G., Strogonov I.A., Vafina H.Ya., Pasechnikov A.V., Paches O.A., Shafranov V.V., Topolnitsky O.Z., Romanov D.V., Schepin N.V., Vorobyov V.V. Treatment experience of a child with extensive lymphatic malformations in head and neck. 25th World Congress of Lymphology. San Francisco. Poster. 136–204..
- Комелягин Д.Ю., Романов Д.В., Петухов А.В., Дубин С.А., Пачес О.А., Вафина Х.Я., Солдатский Ю.Л. Малоинвазивный метод лечения детей с лимфатическими мальформациями головы и шеи. Рос. журн. детской онкологии и гематологии. 2014;2:110.
- Yura J. Bleomycin treatment for cystic hygroma in children. Nippon Geka Hokan. 1977;46(5):607–14.
- Ogita S. Intracystic Yura J., Hasshimoto T., Tsuruga N., Shibata K. injection of OK-432: a new sclerosing therapy for cystic hygroma in children. Br. J. Surg. 1987;74:690–1.
- Komelyagin D.Ju., Petukhov A.V., Dubin S.A., Dergachenko A.V., Vladimirov F., Yamatina S.V., Khaspekov D.V., Topilin O.G., Slipenko V.G., Striga E.V., Dergachenko An.V., Topolnitsky O.Z., Ivanov A.V., Pasechnikov A.V., Vafina H.Ya., Strogonov I.A. Indications for puncture method of treatment of children with lymphatic and lymphovenous malformations of head and neck area. 21st International workshop on vascular anomalies. ISSVA 2016. Argentina. Buenos Aires. 2016. Poster report №72. Р. 101.
- Kella N., Rathi P.K., Sheikh U., Qureshi M.A. Our experience of bleomycin sclerotherapy for peripheral lymphangioma in children and review of the literature. Pak J. Med. Sci. 2011;27(1):60–3.
- Zhou Q., Zheng J.W., Mai H.M., Luo Q.F., Fan X.D., Su L.X., Wang Y.A., Qin Z.P. Treatment guidelines of lymphatic malformations of the head and neck. Oral Oncol. J. Oraloncology. 2011;47(12):1105–9.
- Шаргородский А.Г., Руцкий Н.Ф. Доброкачественные и злокачественные опухоли мягких тканей и костей лица. М., 1999. 191 с.
- Suen J.Y., Waner M. Treatment of oral cavity vascular malformations using the neodymium: YAG laser. Arch. Otolaryngol. Head Neck Surg. 1989;115(11):1329–33.
- Balakrishnan A., Bailey C.M. Lymphangioma of the tongue. A review of pathogenesis, treatment and the use of surface laser photocoagulation. J. Laryngol. Otol. 1991;105(11):924–9.
- Riechelmann H., Muehlfay G., Keck T., Mattfeldt T., Rettinger G. Total, subtotal, and partial surgical removal of cervicofacial lymphangiomas. Arch. Otolaryngol. Head Neck Surg. 1999;125(6):643–8.
- Chen W.L., Zhang B., Wang J.G., Ye H.S., Zhang D.M., Huang Z.Q. Surgical excision of cervicofacial giant macrocystic lymphatic malformations in infants and children. Int. J. Pediatr. Otorhinolaryngol. 2009;73(6):833–7.
Поступила 16.09.18
Принята в печать 01.02.19
REFERENCES
- Isakov Yu.F., Tikhonov Yu.A. Congenital malformations of peripheral vessels in children. M .: Medicine, 1974. 116 p.
- North P.E. Pediatric vascular tumors and malformations. Surgical pathology. 2010;3:455–94.
- Ravitch M.M., Rush Jr. B.F. In: Welch K.J., Randolph M. M., Ravitch M. M., et al. Cystic hygroma. Pediatric surgery. Chicago (III) 7 Year Book Medical. 1986. p. 533–9.
- Ogita S, Tsuno T, Deguchi E., et al. OK-432 therapy for unresectable lymphangioma in children. J. pediatr. surg. 1991;26:263–70.
- Malinin A.P. Treatment of subcutaneous lymphangiomas in children: dis. … Cand. med. sciences. Research Institute of Oncology named after prof. N.N. Petrov, Leningrad Pediatric Medical Institute. 1974.
- Isakov Yu.F., Doletsky S.Ya. Pediatric surgery. M ., 1978. 502 p.
- Coffin C.M., Dehner L.P. Vascular tumors in children and adolescents: a clinicopathologic study of 228 tumors in 222 patients. Pathol. Ann. 1993;23(1):97–120.
- Acevedo J.L., Shah R.K., Brietzke S.E. Nonsurgical therapies for lymphangiomas: a systematic review. J. Otolaryngol. Head Neck Surg. 2008;138(4):418–24.
- Prikhodchenko V.V. Lymphangiomas in children (clinic, diagnosis, treatment): Dis. … Cand. med. sciences. Donetsk State Medical Institute. M. Gorky. 1986.
- Gurgenadze A.P. Improving the methods of diagnosis and treatment of lymphangiomas of the maxillofacial region in children: dis. … Cand. med. sciences. Moscow Medical Dental Institute. 1996.
- Koparzova O.A. Comprehensive treatment of secondary deformities of the soft tissues and bones of the facial skeleton in children with different lymphangioma localization: dis. … Cand. med. sciences. Moscow Medical Dental Institute. 2005.
- Isakov Yu.F. Pediatric surgery. M .: Medicine, 3rd Edition, 1983. 620 p.
- Enjolras O., Wassef M., Chapot R. Color atlas of vascular tumors and vascular malformations. New-York: Oxford uneversity press. 2007. Р. 3–11.
- Topolnitsky OZ, Vasilyev A.Yu. Atlas of Pediatric Surgical Dentistry and Maxillofacial Surgery: textbook. M., 2011. 264 p.
- Roginsky V.V., Nadtochy AG, Ovchinnikov I.A., Gavel E.Yu., Pavelko G.A., Babichenko I.I., Lomaka M.A., Ryzhov R.V. Malformations of the lymphatic
system of the head and neck in children: diagnosis and treatment methods. Materials of the VI Congress of Oncologists with international participation. M., 2015. p. 324.
- Komelyagin D.Ju., Petukhov A.V., Ivanov A.V., Dubin S.A., Khaspekov D.V., Topilin O.G., Dergachenko A.V., Vladimirov F., Dergachenko An.V., Striga E.V., Slipenko V.G., Strogonov I.A., Vafina H.Ya., Pasechnikov A.V., Paches O.A., Shafranov V.V., Topolnitsky O.Z., Romanov D.V., Schepin N.V., Vorobyov V.V. Treatment experience of a child with extensive lymphatic malformations in head and neck. 25th World Congress of Lymphology. San Francisco. 2015. Poster 136-204. № 2015-A-204-NLN.
- Komelyagin D.Yu., Romanov D.V., Petukhov A.V., Dubin S.A., Paces O.A., Vafina H.Y., Soldatsky Yu.L. Minimally invasive treatment of children with lymphatic malformations of the head and neck. Rus. J. Pediatr. Oncol. Hematol. 2014;2:110.
- Yura J. Bleomycin treatment for cystic hygroma in children. Nippon Geka Hokan. 1977;46(5):607–14.
- Ogita S. Intracystic Yura J., Hasshimoto T., Tsuruga N., Shibata K. injection of OK-432: a new sclerosing therapy for cystic hygroma in children. Br. J. Surg. 1987;74:690–1.
- Komelyagin D.Ju., Petukhov A.V., Dubin S.A., Dergachenko A.V., Vladimirov F., Yamatina S.V., Khaspekov D.V., Topilin O.G., Slipenko V.G., Striga E.V., Dergachenko An.V., Topolnitsky O.Z., Ivanov A.V., Pasechnikov A.V., Vafina H.Ya., Strogonov I.A. Indications for puncture method of treatment of children with lymphatic and lymphovenous malformations of head and neck area. 21st International workshop on vascular anomalies. ISSVA 2016. Argentina. Buenos Aires. 2016. Poster report №72. 101 р.
- Kella N., Rathi P.K., Sheikh U., Qureshi M.A. Our experience of bleomycin sclerotherapy for peripheral lymphangioma in children and review of the literature. Pak. J. Med. sci. 2011;27(1):60–3.
- Zhou Q., Zheng J.W., Mai H.M., Luo Q.F., Fan X.D., Su L.X., Wang Y.A., Qin Z.P. Treatment guidelines of lymphatic malformations of the head and neck. Oral Oncol. J. Oraloncology. 2011;47(12):1105–9.
- Шаргородский А.Г., Руцкий Н.Ф. Доброкачественные и злокачественные опухоли мягких тканей и костей лица. М.: ВУНМЦ МЗ РФ. 1999. 191 с. [Shargorodsky A.G., Rutsky N.F. Benign and malignant tumors of the soft tissues and bones of the face. M .: VUNMTS MZ RF. 1999. 191 p.].
- Suen J.Y., Waner M. Treatment of oral cavity vascular malformations using the neodymium: YAG laser. Arch. Otolaryngol. Head Neck Surg. 1989;115(11):1329–13.
- Balakrishnan A., Bailey C.M. Lymphangioma of the tongue. A review of pathogenesis, treatment and the use of surface laser photocoagulation. J. Laryngol. Otol. 1991;105(11):924–9.
- Riechelmann H., Muehlfay G., Keck T., Mattfeldt T., Rettinger G. Total, subtotal, and partial surgical removal of cervicofacial lymphangiomas. Arch. Otolaryngol. Head Neck Surg. 1999;125(6):643–8.
- Chen W.L., Zhang B., Wang J.G., Ye H.S., Zhang D.M., Huang Z.Q. Surgical excision of cervicofacial giant macrocystic lymphatic malformations in infants and children. Int. J. Pediatr. Otorhinolaryngol. 2009;73(6):833–7. Received 16.19.18 Accepted 01.02.19
Сведения об авторах:
Д.Ю. Комелягин – д.м.н., ведущий научный сотрудник НИИ хирургии детского возраста РНИМУ им. Н. И. Пирогова, зав. отделением челюстнолицевой хирургии ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия; e-mail: 1xo@cmfsurgery.ru.
А.В. Петухов – аспирант кафедры детской челюстно-лицевой хирургии МГМСУ им. А.И. Евдокимова, врач отделения челюстно-лицевой хирургии ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия; e-mail: Al.Petukhov.CFS@gmail.com.
А.В. Иванов – к.м.н., челюстно-лицевой хирург ДГКБ №13 им. Н.Ф. Филатова, Москва, Россия; e-mail: avivanoff67@mail.ru.
Е.И. Фокин – к.м.н., зав. патологоанатомическим отделением ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия.
Т.В. Фокина – к.м.н., старший научный сотрудник лаборатории патологии репродукции ФГБНУ «НИИ морфологии человека РАН», Москва, Россия.
С.А. Дубин – к.м.н., врач отделения челюстно-лицевой хирургии ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия.
Ф.И. Владимиров – аспирант кафедры детской челюстно-лицевой хирургии МГМСУ им. А.И. Евдокимова, врач отделения челюстно-лицевой хирургии ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия; е-mail: doctor.vladimirov@yandex.ru.
С.В. Яматина – врач отделения челюстно-лицевой хирургии ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия; e-mail: yam1992@mail.ru.
Д.В. Хаспеков – зав. отделением торакальной хирургии ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия; e-mail: khaspekov@mail.ru. А.В. Пасечников – врач-рентгенолог ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия.
Х.Я. Вафина – врач-рентгенолог ГБУЗ Детская городская клиническая больница святого Владимира, Москва, Россия.
About the authors:
D.Yu. Komelyagin – Doctor of Medical Sciences, Leading Researcher, Scientific Research Institute of Pediatric Surgery, NI Pirogov Russian National Research Medical University; Department of Maxillofacial Surgery, SBIH Children’s Municipal Clinical Hospital of St. Vladimir, Moscow, Russia; e-mail: 1xo@ cmfsurgery.ru.
A.V. Petukhov – postgraduate student of the Department of Pediatric Oral and Maxillofacial Surgery, Moscow State Medical University named after. A.I. Evdokimov, doctor of the Department of Maxillofacial Surgery, SBIH Children’s Municipal Clinical Hospital of St. Vladimir, Moscow, Russia; e-mail: Al.Petukhov.CFS@gmail.com.
A.V. Ivanov – MD, PhD, maxillofacial surgeon of CMCH №13 named after N.F. Filatov, Moscow, Russia; e-mail: avivanoff67@mail.ru.
E.I. Fokin – MD, PhD, head of pathomorphology department of SBIH Children’s Municipal Clinical Hospital of St.Vladimir, Moscow, Russia.
T.V. Fokina – PhD, Senior Researcher, Laboratory of Reproductive Pathology, FSBSI SRI of Human Morphology, RAS, Moscow, Russia.
S.A. Dubin – MD, PhD, doctor of the Department of Maxillofacial Surgery, SBIH Children’s Municipal Clinical Hospital of St. Vladimir, Moscow, Russia.
F.I. Vladimirov – Postgraduate Student, Department of Pediatric Oral and Maxillofacial Surgery, Moscow State Medical University named after A.I. Evdokimov, doctor of the Department of Maxillofacial Surgery, SBIH Children’s Municipal Clinical Hospital of St. Vladimir, Moscow, Russia; e-mail: doctor.vladimirov@yandex.ru.
S.V. Iamatina – SBHI «CMCH of St. Vladimir DHM», maxillofacial surgeon, Moscow, Russia; e-mail: yam1992@mail.ru. D.V. Khaspekov – SBHI «CMCH of St. Vladimir DHM», head of the Department of the thoracal surgery, Moscow, Russia; e-mail: khaspekov@mail.ru.
A.V. Pasechnikov – MD, radiologist of SBIH «CMCH of St. Vladimir DHM», Moscow, Russia. H.Ya. Vafina – MD, radiologist of SBIH «CMCH of St. Vladimir DHM», Moscow, Russia.